
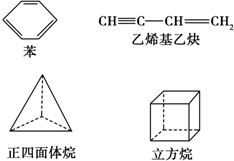
分析 ①同分异构体是分子式相同,结构不同的化合物;
②根据正四面体烷二氯代物的种类取决于一氯代物中氢原子的种类;立方烷的二氯代物取决于一氯代物中氢原子的种类.
解答 解:①苯的分子式为C6H6,立方烷的分子式为C8H8,乙烯基乙炔、正四面体烷的分子式均为C4H4,结构不同,互为同分异构体;
故答案为:乙烯基乙炔;正四面体烷;
②正四面体烷完全对称,只有一种氢原子,一氯代物只有1种,一氯代物中氢原子也只有1种,所以故二氯代物只有1种;
立方烷分子中只有一种氢原子,其一氯代物有1种,而一氯代物有3种氢原子,分为在 ,则立方烷的二氯代物有3种;
,则立方烷的二氯代物有3种;
故答案为:1;3.
点评 本题主要考查了同分异构体的判断,难度中等,注意同分异构体的种类确定.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含氧酸的酸性H3ZO4>H2YO4>HXO4 | |
| B. | HXO4、H2YO4、H3ZO4一定都是强酸 | |
| C. | 元素的负化合价的绝对值按X、Y、Z减小 | |
| D. | 气态氢化物的稳定性按X、Y、Z的顺序减弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二次电池的放电与充电属于可逆反应 | |
| B. | 碱金属单质在空气中燃烧都生成过氧化物 | |
| C. | 在周期表中,族序数都等于该族元素的最外层电子数 | |
| D. | 在周期表过渡元素中寻找催化剂恒和耐腐蚀、耐高温的合金材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素 | 结构、性质等信息 |
| A | 是短周期中(除稀有气体外)原子半径最大的元素,该元素的 某种合金是原子反应堆的导热剂 |
| B | B与A同周期,其最高价氧化物的水化物呈两性 |
| C | 元素的气态氢化物极易溶于水,可用作制冷剂 |
| D | 是海水中除氢、氧元素外含量最多的元素,其单质或化合物也是自水生产过程中常用的消毒杀菌剂 |
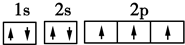 ,其原子核外有3个未成对电子,能量最高的电子为p轨道上的电子,其轨道呈纺锤形.
,其原子核外有3个未成对电子,能量最高的电子为p轨道上的电子,其轨道呈纺锤形.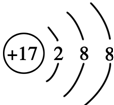 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 序号 | 实验方案 | 实验现象 |
| ① | 向盛有少量溴化钠溶液的试管中滴加少量新制的氯水,振荡,再注入少量四氯化碳,振荡后静置 | 液体分为两层,下层呈橙红色 |
| ② | 向盛有少量碘化钾溶液的试管中滴加少量溴水,振荡,再注入少量四氯化碳,振荡后静置 | 液体分为两层,下层呈紫红色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com