
下列有关卤族元素及其化合物的表示正确的是( )
A. 氟离子的结构示意图: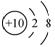 B. 次氯酸的结构式:H-Cl-O
B. 次氯酸的结构式:H-Cl-O
C. 溴化铵的电子式: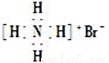 D. 质子数为53,中子数为78的碘原子:
D. 质子数为53,中子数为78的碘原子: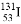
科目:高中化学 来源: 题型:选择题
| A. | 可以用铜丝或铁丝代替铂丝 | |
| B. | 用固体样品或配成的溶液进行实验,现象相同 | |
| C. | 每次实验前,铂丝要先用硫酸洗涤 | |
| D. | 焰色反应实验所用火焰,无论何种燃料均可 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南省高二上第三次月考化学卷(解析版) 题型:选择题
下列设计的实验方案能达到实验目的是
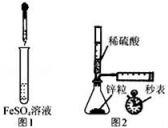
A.制备Fe(OH)2:用图1所示装置,向试管中加入NaOH溶液,振荡
B.测定H2的生成速率:用图2所示装置,制取一定体积的H2,记录时间
C.除去苯中少量苯酚:向苯和苯酚的混合液中加入浓溴水,过滤
D.检验淀粉是否水【解析】
取0.5 g淀粉于洁净的试管中,先加入5 mL稀硫酸,水浴加热,一段时间后再加入少量新制氢氧化铜悬浊液,水浴加热,观察实验现象
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省高二上10月月考化学试卷(解析版) 题型:填空题
今有①CH3COOH;②HCl;③H2SO4三种溶液,选择填空:
A①>②>③ B①<②<③ C①=②=③ D①=③>②
E①>②=③ F①<②=③ G①=②<③ H①=②>③
(1)当它们pH相同时,其物质的量浓度关系是 。
(2)当它们的物质的量浓度相同时,其pH的关系是 。
(3)中和等体积、等物质的量浓度的烧碱溶液,需同物质的量浓度的三种酸溶液的体积关系为 。
(4)体积和物质的量浓度相同的①、②、③三溶液,分别与同浓度的烧碱溶液反应,要使反应后的溶液呈中性,所需烧碱溶液的体积关系为 。
(5)当它们pH相同、体积相同时,分别加入足量锌,相同状况下产生气体体积关系为 。
(6)当它们pH相同、体积相同时,同时加入锌,则开始时反应速率 ,若产生相同体积的气体(相同状况),所需时间 。
(7)将pH相同的三种酸均稀释10倍后,pH关系为 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省高二上10月月考化学试卷(解析版) 题型:选择题
常温下Ksp(AgCl)=1.8×10-10,Ksp(AgI)=1.0×10-16,将等体积的AgCl和AgI的饱和溶液 的清液混合,再向其中加入一定量的AgNO3固体,下列说法正确的是( )
的清液混合,再向其中加入一定量的AgNO3固体,下列说法正确的是( )
A.两溶液混合,AgCl和AgI都沉淀
B.若AgNO3足量,AgCl和AgI都可沉淀,但以AgCl为主
C.向AgI清液加入AgNO3,c(Ag+)增大,KSp(AgI)也增大
D.若 取0.1435克AgCl固体放入100mL水(忽略体积变化),c(Cl-)为0.01mol/L
取0.1435克AgCl固体放入100mL水(忽略体积变化),c(Cl-)为0.01mol/L
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南省高二上第一次月考化学卷(解析版) 题型:填空题
到目前为止,由化学能转变的热能或电能仍然是人类使用的最主要的能源.
(1)在25℃、101kPa下,16g的甲醇(CH3OH)完全燃烧生成CO2和液态水时放出352kJ的热量,则表示甲醇燃烧热的热化学方程式为_____________________。
(2)化学反应中放出的热能(焓变,△H)与反应物和生成物的键能(E)有关.
已知:H2(g)+Cl2(g)=2HCl(g)△H=﹣185kJ/mol,
E(H﹣H)=436kJ/mol,E(Cl﹣Cl)=243kJ/mol则E(H﹣Cl)=_____________
(3)纳米级Cu2O由于具有优良的催化性能而受到关注.已知:
2Cu(s)+ O2(g)═Cu2O(s)△H=﹣169kJ•mol﹣1,
O2(g)═Cu2O(s)△H=﹣169kJ•mol﹣1,
C(s)+ O2(g)═CO(g)△H=﹣110.5kJ•mol﹣1,
O2(g)═CO(g)△H=﹣110.5kJ•mol﹣1,
2Cu(s)+O2(g)═2CuO(s)△H=﹣314kJ•mol﹣1
则工业上用炭粉在高温条件下还原CuO制取Cu2O和CO的热化学方程式_____________。
(4)如图是N2和H2反应生成2molNH3过程中能量变化示意图:

①请计算每生成1molNH3放出热量为:_________.
②若起始时向容器内放入1molN2和3molH2达平衡后N2的为20%,则反应放出的热量为Q1kJ,则Q1的数值为_________.
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com