

分析 (1)依据装置和试剂分析,硫酸和样品中的碳酸钠反应,仪器b是加入液体的仪器可以控制加入的量,是分液漏斗;反应过程中含有水蒸气,可以利用浓硫酸干燥二氧化碳气体;
(2)①使用注射器改变瓶内气体的多少而改变瓶内压强;当将针筒活塞向内推压时,瓶内气体被压缩,压强增大,瓶内液体则会被压入长颈漏斗内,b下端玻璃管中液面上升,可以说明装置气密性良好;
②装置中 加入硫酸和碳酸钠反应生成二氧化碳,注射器活塞被向外推出,可以测定二氧化碳的体积;
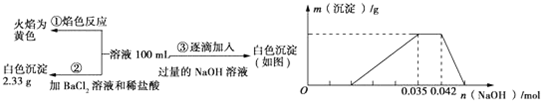
(3)依据流程分析可知,加入氢氧化钡溶液和碳酸钠 反应生成碳酸钡沉淀,通过过滤得到沉淀,洗涤后称重得到沉淀碳酸钡质量;
(4)依据CO2+2KOH═K2CO3+H2O CO2+KOH═KHCO3,n(CO2):n(KOH)=1:2,产物为K2CO3,n(CO2):n(KOH)=1:1,产物为KHCO3,以此计算.
解答 解:(1)依据装置和试剂分析,硫酸和样品中的碳酸钠反应,仪器b是加入液体的仪器可以控制加入的量,是分液漏斗;反应过程中含有水蒸气,可以利用浓硫酸干燥二氧化碳气体,
故答案为:Na2CO3;分液漏斗;除去CO2中的水蒸气;
(2)①使用注射器改变瓶内气体的多少而改变瓶内压强;当将针筒活塞向内推压时,瓶内气体被压缩,压强增大,瓶内液体则会被压入长颈漏斗内,b下端玻璃管中液面上升,可以说明装置气密性良好,故答案为:液面;
②在实验完成时,反应后可以利用注射器读取生成气体的体积,能直接测得的数据是CO2的体积,故答案为:体积;
(3)流程分析可知,加入氢氧化钡溶液和碳酸钠 反应生成碳酸钡沉淀,通过过滤得到沉淀,洗涤后称重得到沉淀碳酸钡质量,
故答案为:过滤;称量;
(4)CO2+2KOH═K2CO3+H2O CO2+KOH=KHCO3,n(CO2):n(KOH)=1:2,产物为K2CO3,n(CO2):n(KOH)=1:1,产物为KHCO3,标准状况下,将672mL CO2气体物质的量=$\frac{0.672L}{22.4L/mol}$=0.03mol;通入50mL 1mol/L KOH溶液中,n(KOH)=0.05L×1mol/L=0.05mol,n(CO2):n(KOH)=0.03:0.05=3:5,所以1:2<3:5<1:1,二氧化碳和氢氧化钾全部反应生成碳酸钾和碳酸氢钾,利用直平法写出反应的化学方程式为:3CO2+5KOH═KHCO3+2K2CO3+2H2O,则n(K2CO3):n(KHCO3)=2:1,
故答案为:2:1.
点评 本题考查了物质性质的实验验证和含量测定方法分析判断,混合物中物质质量分数的计算方法和应用,题目难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:多选题
| A. | 盐酸 | B. | KHS溶液 | C. | NaOH溶液 | D. | Na2S溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该溶液只能由等物质的量浓度、等体积的氢氧化钠溶液和醋酸溶液混合而成 | |
| B. | 该溶液一定由pH=3的醋酸溶液与pH=11的氢氧化钠溶液等体积混合而成 | |
| C. | 该溶液中离子浓度一定为c(Na+)>c(CH3COO-)>c(OH-)>c(H+) | |
| D. | 加入一定冰醋酸,c(CH3COO-)可能大于、等于或小于c(Na+) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
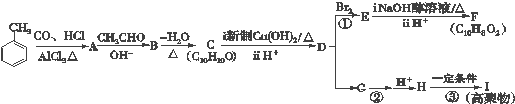
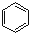 $→_{AlCl_{3}△}^{CO、HCl}$
$→_{AlCl_{3}△}^{CO、HCl}$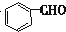
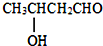 $→_{△}^{-H_{2}O}$CH3CH=CHCHO
$→_{△}^{-H_{2}O}$CH3CH=CHCHO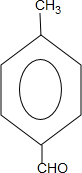 .
. +2Cu(OH)2$\stackrel{△}{→}$
+2Cu(OH)2$\stackrel{△}{→}$ +Cu2O↓+2H2O.
+Cu2O↓+2H2O. $\stackrel{一定条件下}{→}$
$\stackrel{一定条件下}{→}$ +nH2O.
+nH2O.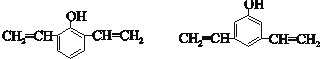 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| n(SO32-):n(HSO3-) | 91:9 | 1:1 | 9:91 |
| pH | 8.2 | 7.2 | 6.2 |
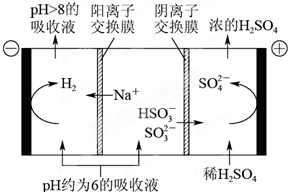
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2CO3比NaHCO3易溶于水 | |
| B. | Na2CO3比NaHCO3稳定 | |
| C. | Na2CO3溶液比NaHCO3溶液碱性强 | |
| D. | 碳酸钠与盐酸反应放出二氧化碳的剧烈程度强于碳酸氢钠 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,17 g NH3中含有的电子总数为10NA | |
| B. | 常温常压下,14g的C2H4和C3H6混合气体含有的氢原子数为2NA | |
| C. | 常温常压下,22.4 L氯气与足量镁粉充分反应,转移的电子数为2NA | |
| D. | 标准状况下,22.4 L 的N2O和CO2混合气体中含有的电子总数为22NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com