
| A、只滴加氨水鉴别NaCl、AlCl3、MgCl2、Na2SO4四种溶液 |
| B、用湿润的淀粉碘化钾试纸鉴别Br2(g)和NO2 |
| C、用CO2鉴别NaAlO2溶液和CH3COONa溶液 |
| D、用KOH溶液鉴别SO3(g)和SO2 |


科目:高中化学 来源: 题型:
| A、室温下,pH=11的氨水与pH=3的盐酸等体积混合:c(Cl-)=c(NH4+)>c(OH-)=c(H+) |
| B、醋酸与醋酸钠的pH=7的混合溶液中:c(CH3COO-)+c(CH3COOH)<c(Na+) |
| C、相同物质的量浓度的NaClO和NaHCO3混合溶液中:c(HClO)+c(ClO-)=c(HCO3-)+c(H2CO3)+c(CO32-) |
| D、c(NH4+)相等的(NH4)2SO4、NH4HSO4、NH4Cl溶液中:c(NH4HSO4)>c[(NH4)2SO4]>c(NH4Cl) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、PM2.5是指氮、硫的氧化物溶于水形成的酸性液体造成的空气污染 |
| B、氯气是塑料、合成橡胶、合成纤维、农药、染料及药品的重要原料 |
| C、硅陶瓷和碳纤维复合制成的材料是一种新型无机非金属材料 |
| D、用浸泡过高锰酸钾溶液的硅藻土吸收水果产生的乙烯以达到保鲜目的 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、分馏、蒸馏、煤的液化都是物理变化,干馏、裂化、裂解都是化学变化 |
| B、乙烯和聚乙烯均能和溴水发生加成反应而使溴水褪色 |
| C、需要加热的反应不一定是吸热反应 |
| D、根据是否具有丁达尔效应,将分散系分为溶液、浊液和胶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、 加热烧杯,可用来分离NaCl和NH4Cl |
B、 石蜡油分解实验 |
C、 比较MnO2、Cl2、S的氧化性 |
D、 收集干燥的氨气 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、 验证化学能转化为电能 |
B、 比较硫、碳、硅三种元素的非金属行强弱 |
C、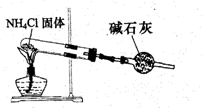 实验室制取NH3 |
D、 分离沸点不同且互溶的液体混合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、若混合后呈中性,测混合后的溶液中一定存在:c(Na+)=c(CH3COO-)>c(OH-)=c(H+) |
| B、若混合后呈酸性,则混合后的溶液中可能存在:c(CH3COO-)>c(Na+)>c(CH3COOH)>c(H+)>c(OH-) |
| C、若混合后呈碱性,则混合后的溶液中可能存在:c(Na+)>c(OH-)>c(CH3COO-)>c(CH3COOH) |
| D、若混合后的溶液中存在c(CH3COO-)+c(CH3COOH)=2c(Na+),则也一定存在c(OH-)+c(CH3COO-)=c(CH3COOH)+c(H+)等式 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com