
| A. | pH=5.5溶液中:c(CH3COOH)>c(CH3COO-)>c(H+)>c(OH-) | |
| B. | W点表示溶液中:c(Na+)═c(CH3COO-)+c(CH3COOH) | |
| C. | pH=3.5溶液中:c(Na+)+c(H+)-c(OH-)+c(CH3COOH)=0.1mol•L-1 | |
| D. | 向W点所表示的1.0L溶液中通入0.05molHCl气体(溶液体积变化可忽略):c(H+)═c(CH3COOH)+c(OH-) |
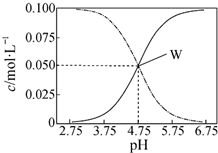
分析 A.醋酸、醋酸钠混合溶液,由图可知,溶液显酸性,则开始电离大于水解,W点c(CH3COO-)=c(CH3COOH),W点后,水解大于电离,c(CH3COO-)<c(CH3COOH);
B.由图可知,W点所表示的溶液中c(CH3COOH)=c(CH3COO-)=0.05mol/L,根据W点溶液的pH进行判断;
C.由电荷守恒及c(CH3COOH)+c(CH3COO-)=0.1mol•L-1分析;
D.W点为等量的醋酸和醋酸钠的混合液,溶液中通入0.05 mol HCl气体后,溶液呈电中性,根据物料守恒和电荷守恒判断.
解答 解:A.由图可知,pH=5.5 的溶液,显酸性,且c(CH3COO-)<c(CH3COOH),显性离子大于隐性离子,则c(CH3COOH)>c(CH3COO-)>c(H+)>c(OH-),故A正确;
B.溶液存在电荷守恒,应为c(Na+)+c(H+)=c(CH3COO-)+c(OH-),W点时c(CH3COOH)=c(CH3COO-),而氢离子浓度较小,则c(H+)<<c(CH3COOH),故c(Na+)+c(H+)<c(CH3COO-)+c(CH3COOH),故B错误;
C.由电荷守恒及c(CH3COOH)+c(CH3COO-)=0.1mol•L-1可知,c(Na+)+c(H+)-c(OH-)+c(CH3COOH)=c(CH3COO-)+c(CH3COOH)=0.1mol/L,故C正确;
D.向W点所表示溶液中通入0.05molHCl气体,原有平衡被打破,建立起了新的平衡,溶液中电荷守恒关系为:c(Na+)+c(H+)=c(CH3COO-)+c(OH-)+c(Cl-);物料守恒关系为:2c(Cl-)=c(CH3COO-)+c(CH3COOH)=0.1mol•L-1,得2c(Na+)+2c(H+)=3c(CH3COO-)+2c(OH-)+c(CH3COOH)
,c(Na+)=0.05mol/L,c(CH3COOH)+c(CH3COO-)=0.1mol/L,所以得c(H+)═c(CH3COO-)+c(OH-),故D错误;
故选AC.
点评 本题考查离子浓度大小比较,为高频考点,溶液中存在水解与电离两个过程的离子浓度大小比较似乎是考试热点内容,再结合守恒思想分析解答,题目难度不大.


 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源: 题型:解答题
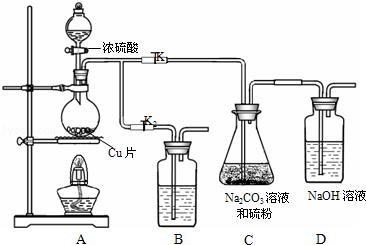
| 编 号 | 1 | 2 | 3 | 4 |
| 消耗Na2S2O3标准溶液的体积/mL | 18.02 | 17.98 | 18.00 | 20.03 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在中毒过程中血红蛋白被氧化 | B. | 解毒时血红蛋白被还原 | ||
| C. | 维生素C应具有还原性 | D. | 中毒时亚硝酸盐发生氧化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
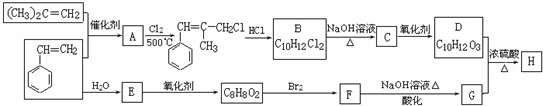
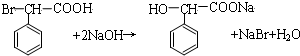 .
.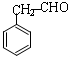 .
.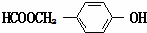 (写结构简式).
(写结构简式).查看答案和解析>>
科目:高中化学 来源: 题型:解答题
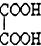
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 目前城市空气质量恶化原因之一是机动车尾气和燃煤产生的烟气.NO和CO均为汽车尾气的成分,这两种气体在催化转换器中发生如下反应:
目前城市空气质量恶化原因之一是机动车尾气和燃煤产生的烟气.NO和CO均为汽车尾气的成分,这两种气体在催化转换器中发生如下反应:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu2+、Cl-、K+、SO42- | B. | CO32-、Na+、K+、SO42- | ||
| C. | Mg2+、Cl-、K+、NO3- | D. | Ag+、NO3-、K+、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
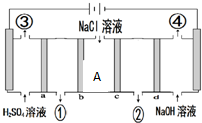
| A. | a和c为阳离子交换膜,b和d为阴离子交换膜 | |
| B. | ③与④两种气体体积比为1:1 | |
| C. | ①处生成的物质为氢氧化钠 | |
| D. | 当转移2mol e-时,A处减少离子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 28g乙烯所含共用电子对数目为4NA | |
| B. | 1 mol甲基(-CH3)所含的电子总数为9NA | |
| C. | 0.5 mol1,3-丁二烯分子中含有C=C双键数为NA | |
| D. | 标准状况下,11.2 L己烷所含分子数为0.5 NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com