
°æƒø°øA°´F¡˘÷÷‘™Àÿ÷–£¨≥˝CÕ‚∆‰À˚æ˘Œ™∂Ã÷Ð∆⁄‘™Àÿ£¨À¸√«µƒ‘≠◊”Ω·ππªÚ–‘÷ »Áœ¬±ÌÀ˘ æ°£
‘™Àÿ | ‘≠◊”Ω·ππªÚ–‘÷ |
A | ‘≠◊”◊ÓÕ‚≤„µÁ◊” ˝ «ƒ⁄≤„µÁ◊”◊Ð ˝µƒ1/5 |
B | –Œ≥…ªØ∫œŒÔ÷÷¿ý◊Ó∂ýµƒ‘™Àÿ£¨∆‰µ•÷ Œ™πÃà|
C | …˙ªÓ÷–≥£º˚µƒΩ Ù£¨À¸”–¡Ω÷÷≥£º˚µƒ¬»ªØŒÔ£¨«“œý∂‘∑÷◊”÷ ¡øœý≤Ó35.5 |
D | µÿø«÷–∫¨¡ø◊Ó∂ýµƒ‘™Àÿ |
E | ”ÎDÕ¨÷˜◊ |
F | ”ÎEÕ¨÷Ð∆⁄£¨«“◊ÓÕ‚≤„µÁ◊” ˝µ»”⁄µÁ◊”≤„ ˝ |
«Îªÿ¥œ¬¡–Œ £∫£®”√∂‘”¶µƒªØ—ß”√”Ôªÿ¥£©
£®1£©B‘⁄‘™Àÿ÷Ð∆⁄±Ì÷–µƒŒª÷√ «__________£ª”√µÁ◊” Ω±Ì æA∫ÕE–Œ≥…µƒªØ∫œŒÔµƒ–Œ≥…π˝≥à °£
£®2£©A°¢ D °¢E°¢ F¿Î◊”∞Îæ∂”…¥ÛµΩ–°µƒÀ≥–ÚŒ™________________________________°£
£®3£©Cµƒƒ≥÷÷¬»ªØŒÔµƒ≈®»Ð“∫ø…“‘∏Ø ¥”°À¢µÁ¬∑∞Â…œµƒΩ ÙÕ≠£¨¥À∑¥”¶µƒ¿Î◊”∑Ω≥Ã Ω «__________________£ª
£®4£©Bµƒµ•÷ ”ÎDµƒ«‚ªØŒÔ‘⁄“ª∂®Ãıº˛œ¬∑¥”¶…˙≥…BD∫Õ¡Ì“ª≤˙ŒÔµƒªØ—ß∑Ω≥Ã Ω «____________________°£∏√∑¥”¶Œ™ ∑¥”¶°££®ÃÓ°∞Œ¸»»°±ªÚ°∞∑≈»»°±£©
£®5£©Fµƒ◊Ó∏þº€—ıªØŒÔ”ÎEµƒ◊Ó∏þº€—ıªØŒÔµƒÀƪ،Ô∑¥”¶µƒ¿Î◊”∑Ω≥Ã ΩŒ™ °£
£®6£©»ÁÕº£∫Ω´A∫ÕFµƒµ•÷ ”Î…’ºÓ“∫ππ≥…‘≠µÁ≥ÿ£¨∏∫º´µƒµÁº´∑¥”¶ ΩŒ™ £ªÕ‚µÁ¬∑÷–µÁ◊”¥” µÁº´¡˜œÚ µÁº´ °£
°æ¥∞∏°ø£®1£©∂˛÷Ð∆⁄°¢¢ÙA◊ £ª
£®2£©S2-£æO2-£æMg2+£æAl3+
£®3£©2Fe3+£´Cu£Ω2Fe2£´+ Cu2+£®4£© C£´H2O (g)![]() CO£´H2°£ Œ¸»»£ª
CO£´H2°£ Œ¸»»£ª
£®5£©Al2O3+6H+=2Al3++3H2O £®6£©Al£≠3e-+4OH-£ΩAlO2-+2H2O £ªAl Mg£®π≤2∑÷£©
°æΩ‚Œˆ°ø
A‘≠◊”◊ÓÕ‚≤„µÁ◊” ˝ «ƒ⁄≤„µÁ◊”◊Ð ˝µƒ1/5£¨‘ÚA «Mg£ªB–Œ≥…ªØ∫œŒÔ÷÷¿ý◊Ó∂ýµƒ‘™Àÿ£¨∆‰µ•÷ Œ™πÃ㨑ÚB «C‘™Àÿ£ªC‘™Àÿ…˙ªÓ÷–≥£º˚µƒΩ Ù£¨À¸”–¡Ω÷÷≥£º˚µƒ¬»ªØŒÔ£¨«“œý∂‘∑÷◊”÷ ¡øœý≤Ó35.5£¨‘ÚC «Fe‘™Àÿ£ªD‘™Àÿ «µÿø«÷–∫¨¡ø◊Ó∂ýµƒ‘™Àÿ£¨‘ÚD «O‘™Àÿ£ªE‘™Àÿ”ÎDÕ¨÷˜◊µƒ∂Ã÷Ð∆⁄‘™Àÿ£¨‘ÚE «S‘™Àÿ£ªF”ÎEÕ¨÷Ð∆⁄£¨«“◊ÓÕ‚≤„µÁ◊” ˝µ»”⁄µÁ◊”≤„ ˝£¨‘ÚF «Al‘™Àÿ°£
£®1£© B‘⁄‘™Àÿ÷Ð∆⁄±Ì÷–µƒŒª÷√ «µ⁄∂˛÷Ð∆⁄°¢¢ÙA◊£ª”√µÁ◊” Ω±Ì æA∫ÕE–Œ≥…µƒªØ∫œŒÔµƒ–Œ≥…π˝≥ÃŒ™£∫ £ª
£ª
£®2£© ∂‘”⁄µÁ◊”≤„Ω·ππœýÕ¨µƒ¿Î◊”¿¥Àµ£¨∫ÀµÁ∫… ˝‘Ω¥Û£¨¿Î◊”∞Îæ∂‘Ω–°£ª∂‘”⁄µÁ◊”≤„Ω·ππ≤ªÕ¨µƒ¿Î◊”£¨µÁ◊”≤„ ˝‘Ω∂ý£¨¿Î◊”∞Îæ∂‘Ω¥Û°£‘ÚA°¢ D °¢E°¢ F¿Î◊”∞Îæ∂”…¥ÛµΩ–°µƒÀ≥–ÚŒ™S2-£æO2-£æMg2+£æAl3+°£
£®3£©Cµƒƒ≥÷÷¬»ªØŒÔµƒ≈®»Ð“∫FeCl3”–«øµƒ—ıªØ–‘£¨ø…“‘”ÎCu∑¢…˙∑¥”¶£¨“Ú¥Àø…“‘∏Ø ¥”°À¢µÁ¬∑∞Â…œµƒΩ ÙÕ≠£¨¥À∑¥”¶µƒ¿Î◊”∑Ω≥Ã Ω «2Fe3+£´Cu£Ω2Fe2£´+ Cu2+£ª
£®4£© Bµƒµ•÷ C”ÎDµƒ«‚ªØŒÔH2O‘⁄“ª∂®Ãıº˛œ¬∑¥”¶…˙≥…CO∫Õ¡Ì“ª≤˙ŒÔH2£¨∑¥”¶µƒªØ—ß∑Ω≥Ã Ω «C£´H2O (g)![]() CO£´H2£¨∏√∑¥”¶Œ™Œ¸»»∑¥”¶£ª
CO£´H2£¨∏√∑¥”¶Œ™Œ¸»»∑¥”¶£ª
£®5£©Fµƒ◊Ó∏þº€—ıªØŒÔAl2O3 «¡Ω–‘—ıªØŒÔ£¨ø…“‘”ÎEµƒ◊Ó∏þº€—ıªØŒÔµƒÀƪ،ÔH2SO4∑¢…˙∑¥”¶°£∑¥”¶µƒ¿Î◊”∑Ω≥Ã ΩŒ™Al2O3+6H+=2Al3++3H2O°£
£®6£©Ω´Mg∫ÕAlµƒµ•÷ ”Î…’ºÓ“∫ππ≥…‘≠µÁ≥ÿ£¨”…”⁄Alø…“‘”ΫøºÓ»Ð“∫∑¢…˙∑¥”¶£¨∂¯Mg≤ªƒÐ∑¥”¶£¨À˘“‘MgŒ™’˝º´£¨AlŒ™∏∫º´°£∏∫º´µƒµÁº´∑¥”¶ ΩŒ™Al£≠3e-+4OH-£ΩAlO2-+2H2O£ªÕ‚µÁ¬∑÷–µÁ◊”¥”∏∫º´AlµΩ’˝º´Mg°£


 æ´”¢ø⁄À„ø®œµ¡–¥∞∏
æ´”¢ø⁄À„ø®œµ¡–¥∞∏ ”¶”√µ„≤¶œµ¡–¥∞∏
”¶”√µ„≤¶œµ¡–¥∞∏ ◊¥‘™º∞µ⁄œµ¡–¥∞∏
◊¥‘™º∞µ⁄œµ¡–¥∞∏
| ƒÍº∂ | ∏þ÷–øŒ≥à | ƒÍº∂ | ≥ı÷–øŒ≥à |
| ∏þ“ª | ∏þ“ª√‚∑—øŒ≥ÃÕ∆ºˆ£° | ≥ı“ª | ≥ı“ª√‚∑—øŒ≥ÃÕ∆ºˆ£° |
| ∏þ∂˛ | ∏þ∂˛√‚∑—øŒ≥ÃÕ∆ºˆ£° | ≥ı∂˛ | ≥ı∂˛√‚∑—øŒ≥ÃÕ∆ºˆ£° |
| ∏þ»˝ | ∏þ»˝√‚∑—øŒ≥ÃÕ∆ºˆ£° | ≥ı»˝ | ≥ı»˝√‚∑—øŒ≥ÃÕ∆ºˆ£° |
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°ø∂‘º◊ÕÈ∫Õ CO2 µƒ∏þ–ß¿˚”√≤ªΩˆƒÐª∫Ω‚¥Û∆¯±‰≈Ø£¨∂¯«“∂‘»’“ÊøðΩþµƒ Ø”Õ◊ ‘¥“≤”–“ª∂®µƒ≤π≥‰◊˜”√£¨º◊ÕÈ¡Ÿ—ıÒÓ∫œ CO2 ÷ÿ’˚∑¥”¶”–£∫
∑¥”¶(i)£∫2CH4(g)£´O2(g)2CO(g)£´4H2(g) °˜ H=£≠71.4kJmol-1
∑¥”¶(ii)£∫CH4(g)£´CO2(g)2CO(g)£´2H2(g) °˜ H=+247.0 kJmol-1
(1)–¥≥ˆ±Ì æ CO »º…’»»µƒ»»ªØ—ß∑Ω≥Ã Ω£∫_____°£
(2)‘⁄¡Ω∏ˆÃª˝æ˘Œ™ 2L µƒ∫„»ð√б’»ð∆˜÷–£¨∆ º ±∞¥±Ì÷–œý”¶µƒ¡øº”»ÎŒÔ÷ £¨‘⁄œýÕ¨Œ¬∂»œ¬Ω¯––∑¥”¶(ii)£∫CH4(g)£´CO2(g)2CO(g)£´2H2(g) (≤ª∑¢…˙∆‰À¸∑¥”¶)£¨CO2µƒ∆Ω∫‚◊™ªØ¬ »Á±ÌÀ˘ æ£∫
»ð∆˜ | ∆ ºŒÔ÷ µƒ¡ø(n) / mol | CO2µƒ∆Ω∫‚◊™ªØ¬ | |||
CH4 | CO2 | CO | H2 | ||
¢Ò | 0.1 | 0.1 | 0 | 0 | 50£• |
¢Ú | 0.1 | 0.1 | 0.2 | 0.2 | / |
¢Ÿœ¬¡–Ãıº˛ƒÐÀµ√˜∑¥”¶¥ÔµΩ∆Ω∫‚◊¥Ã¨µƒ «_____°£
A.v’˝(CH4) =2vƒÊ(CO)
B.»ð∆˜ƒ⁄∏˜ŒÔ÷ µƒ≈®∂»¬˙◊„c(CH4)°§c(CO2)=c2(CO)°§c2(H2)
C.»ð∆˜ƒ⁄ªÏ∫œ∆¯Ãµƒ◊Зπ«ø≤ª‘Ÿ±‰ªØ
D.»ð∆˜ƒ⁄ªÏ∫œ∆¯ÃÂ√Ð∂»±£≥÷≤ª±‰
¢⁄¥ÔµΩ∆Ω∫‚ ±£¨»ð∆˜¢Ò°¢¢Úƒ⁄ CO µƒŒÔ÷ µƒ¡øµƒπÿœµ¬˙◊„£∫2n(CO)¢Ò_____n(CO)¢Ú(ÃÓ°∞£æ°±°¢°∞£Ω°±ªÚ°∞£º°±)
(3)Ω´“ª∂®¡øµƒº◊ÕÈ∫Õ—ı∆¯ªÏ∫œÕÍ≥…∑¥”¶(i)£¨∆‰À˚Ãıº˛œýÕ¨£¨‘⁄º◊°¢““¡Ω÷÷≤ªÕ¨¥þªØº¡◊˜”√œ¬£¨ œýÕ¨ ±º‰ƒ⁄≤‚µ√ CH4 ◊™ªØ¬ ”ÎŒ¬∂»±‰ªØπÿœµ»ÁÕºÀ˘ æ°£c µ„_____(ÃÓ°∞ø…ƒÐ°±°¢°∞“ª∂®°±ªÚ°∞“ª∂®Œ¥°±)¥ÔµΩ∆Ω∫‚◊¥Ã¨£¨¿Ì”… «_____°£

(4)CO2 “≤ø…Õ®π˝¥þªØº”«‚∫œ≥…““¥º£¨∆‰∑¥”¶‘≠¿ÌŒ™£∫2CO2(g)+6H2(g)C2H5OH(g)+3H2O(g) H<0°£…Ë m Œ™∆ º ±µƒÕ∂¡œ±»£¨º¥ m= n(H2)/ n(CO2)°£Õ®π˝ µ—ȵ√µΩœ¬¡–ÕºœÛ£∫
Õº1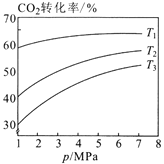 Õº2
Õº2 Õº3
Õº3
¢ŸÕº 1 ÷–Õ∂¡œ±»œýÕ¨£¨Œ¬∂»¥”∏þµΩµÕµƒÀ≥–ÚŒ™_________°£
¢⁄Õº 2 ÷– m1°¢m2°¢m3 ¥”¥ÛµΩ–°µƒÀ≥–ÚŒ™_________°£
¢€Õº 3 ±Ì æ‘⁄◊Ð—πŒ™ 5 MPa µƒ∫„—πÃıº˛œ¬£¨«“ m=3 ±£¨∆Ω∫‚◊¥Ã¨ ±∏˜ŒÔ÷ µƒŒÔ÷ µƒ¡ø∑÷ ˝”ÎŒ¬∂»µƒπÿœµ°£T4 Œ¬∂» ±£¨∏√∑¥”¶—π«ø∆Ω∫‚≥£ ˝KPµƒº∆À„ ΩŒ™_________(”√∆Ω∫‚∑÷—π¥˙ÃÊ∆Ω∫‚≈®∂»º∆À„£¨∑÷—π=◊Ð—π°¡ŒÔ÷ µƒ¡ø∑÷ ˝£¨¥˙»Î ˝æð£¨≤ª”√º∆À„)°£
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°ø∏˘æ𜬡– µ—ÈªÚ µ—È≤Ÿ◊˜∫Õœ÷œÛ£¨À˘µ√Ω·¬€’˝»∑µƒ «
µ—ÈªÚ µ—È≤Ÿ◊˜ | œ÷œÛ | µ—ÈΩ·¬€ | |
A | ”√¥Û¿Ì Ø∫Õ—ŒÀ·∑¥”¶÷∆»°CO2∆¯Ã£¨¡¢º¥Õ®»Î“ª∂®≈®∂»µƒNa2SiO3»Ð“∫÷– | ≥ˆœ÷∞◊…´≥¡µÌ | H2CO3µƒÀ·–‘±»H2SiO3µƒÀ·–‘«ø |
B | œÚƒ≥»Ð“∫œ»µŒº”œıÀ·À·ªØ£¨‘ŸµŒº”BaCl2»Ð“∫ | ≥ˆœ÷∞◊…´≥¡µÌ | ‘≠»Ð“∫÷–∫¨”–SO42-°¢SO32-°¢HSO3-÷–µƒ“ª÷÷ªÚº∏÷÷ |
C | Ω´¥øZn∆¨”Î¥øCu∆¨”√µºœþ¡¨Ω”£¨Ω˛»ÎµΩœ°¡ÚÀ·»Ð“∫÷– | Cu∆¨±Ì√Ê≤˙…˙¥Û¡ø∆¯≈ð | Ω Ù–‘£∫Zn£æCu |
D |
| ◊Û±þ√Þ«Ú±‰Œ™≥»…´£¨”“±þ√Þ«Ú±‰Œ™¿∂…´ | —ıªØ–‘£∫Cl2£æBr2£æI2 |
A. A B. B C. C D. D
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°ø¿˚”√ªØ—ß‘≠¿Ìø…“‘∂‘π§≥ß≈≈∑≈µƒ∑œÀÆ°¢∑œ‘¸µ»Ω¯––”––ߺÏ≤‚”Î∫œ¿Ì¥¶¿Ì°£ƒ≥π§≥ß∂‘÷∆∏Ô𧓵Œ€ƒý÷–Cr£®¢Û£©µƒ¥¶¿Ì𧓒¡˜≥ûÁœ¬£∫
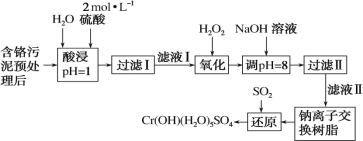
“—÷™£∫¢Ÿ¡ÚÀ·Ω˛»°“∫÷–µƒΩ Ù¿Î◊”÷˜“™ «Cr3£´£¨∆‰¥Œ «Fe3£´°¢Al3£´°¢Ca2£´∫ÕMg2£´°£
¢⁄Cr2O72-+H2O2CrO42-+2H+
¢€≥£Œ¬œ¬£¨≤ø∑÷—Ù¿Î◊”“‘«‚—ıªØŒÔ–Œ Ω≥¡µÌ ±»Ð“∫µƒpH»Áœ¬£∫
—Ù¿Î◊” | Fe3+ | Mg2+ | Al3+ | Cr3+ |
≥¡µÌÕÍ»´ ±µƒpH | 3.7 | 11.1 | 5.4£®>8»ÐΩ‚£© | 9£®>9£©»ÐΩ‚ |
£®1£© µ—È “”√18.4mol°§L-1µƒ≈®¡ÚÀ·≈‰÷∆480mL2mol°§L-1µƒ¡ÚÀ·£¨≈‰÷∆ ±À˘”√≤£¡ß“«∆˜≥˝…’±≠°¢≤£¡ß∞Ù∫ÕΩ∫Õ∑µŒπÐÕ‚£¨ªπ–Ë_______°£
£®2£©H2O2µƒ◊˜”√ «Ω´¬À“∫¢Ò÷–µƒCr3£´◊™ªØŒ™Cr2O72-£¨–¥≥ˆ¥À∑¥”¶µƒ¿Î◊”∑Ω≥Ã Ω£∫_______°£
£®3£©º”»ÎNaOH»Ð“∫ π»Ð“∫≥ ºÓ–‘£¨º»ø…“‘≥˝»•ƒ≥–©‘”÷ ¿Î◊”£¨Õ¨ ±”÷ø…“‘Ω´Cr2O72£≠◊™ªØŒ™______£®ÃÓŒ¢¡£µƒªØ—ß Ω£©°£
£®4£©ƒ∆¿Î◊”Ωªªª ˜÷¨µƒ∑¥”¶‘≠¿ÌŒ™Mn£´£´nNaR=MRn£´nNa£´£¨‘Ú¿˚”√ƒ∆¿Î◊”Ωªªª ˜÷¨ø…≥˝»•¬À“∫¢Ú÷–µƒΩ ٗٿÎ◊””–_____°£
£®5£©–¥≥ˆ…œ ˆ¡˜≥Ã÷–”√SO2Ω¯––ªπ‘≠ ±∑¢…˙∑¥”¶µƒ¿Î◊”∑Ω≥Ã Ω£∫_____°£
£®6£©≥¡µÌµŒ∂®∑® «≤‚∂®¡£◊”≈®∂»µƒ∑Ω∑®÷Æ“ª£¨Œ™¡À≤‚∂®ƒ≥∑œÀÆ÷–SCN-µƒ≈®∂»£¨ø…”√0.1000mol°§L£≠1AgNO3±Í◊º»Ð“∫µŒ∂®¥˝≤‚“∫£¨“—÷™£∫
¢ŸµŒ∂® ±ø…—°Œ™µŒ∂®÷∏ 溡µƒ «_______£®ÃÓ±ý∫≈£©£¨µŒ∂®÷’µ„µƒœ÷œÛ «_______°£
A£ÆNaCl°°°°B£ÆK2CrO4°°°°°°C£ÆKI°°°°°°D£ÆNaCN
¢⁄»°ƒ≥∑œÀÆ25.00ml,µŒ∂®÷’µ„ ±œ˚∫ƒAgNO3±Í◊º»Ð“∫10.00ml,‘Ú∑œÀÆ÷–SCN£≠µƒŒÔ÷ µƒ¡ø≈®∂»Œ™_______°£
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°øNa3OCl «“ª÷÷¡º∫√µƒ¿Î◊”µºÃ£¨æþ”–∑¥∏∆Ó—øÛæßÃÂΩ·π𰣪ÿ¥œ¬¡–Œ £∫
£®1£©Ca–°”⁄Tiµƒ «_______£®ÃÓ±Í∫≈£©°£
A£Æ◊ÓÕ‚≤„µÁ◊” ˝ B£ÆŒ¥≥…∂‘µÁ◊” ˝ C£Æ‘≠◊”∞Îæ∂ D£Æµ⁄»˝µÁ¿ÎƒÐ
£®2£©”…O°¢Cl‘™Àÿø…◊È≥…≤ªÕ¨µƒµ•÷ ∫ÕªØ∫œŒÔ£¨∆‰÷–Cl2O2ƒÐ∆∆ªµ≥Ù—ı≤„°£
¢Ÿ Cl2O2µƒ∑–µ„±»H2O2µÕ£¨‘≠“Ú «___________________________________°£
¢⁄ O3∑÷◊”÷––ƒ‘≠◊”‘”ªØ¿ý–ÕŒ™_______£ªO3 «º´–‘∑÷◊”£¨¿Ì”… «___________________°£
£®3£©Na3OClø…”…“‘œ¬¡Ω÷÷∑Ω∑®÷∆µ√£∫
∑Ω∑®¢Ò Na2O + NaCl![]() Na3OCl
Na3OCl
∑Ω∑®II 2Na + 2NaOH + 2NaCl![]() 2Na3OCl + H2°¸
2Na3OCl + H2°¸
¢Ÿ Na2OµƒµÁ◊” ΩŒ™____________°£
¢⁄ ‘⁄∑Ω∑®¢Úµƒ∑¥”¶÷–£¨–Œ≥…µƒªØ—ߺ¸”–_______£®ÃÓ±Í∫≈£©°£
A£ÆΩ Ùº¸ B£Æ¿Î◊”º¸°° C£Æ≈‰Œªº¸°° D£Æº´–‘º¸ E£Æ∑«º´–‘º¸
£®4£©Na3OClæßàٔ⁄¡¢∑Ωæßœµ£¨∆‰æß∞˚Ω·ππ»Á”“À˘ æ°£“—÷™£∫æß∞˚≤Œ ˝Œ™a nm£¨√Ð∂»Œ™d g°§cm£≠3°£
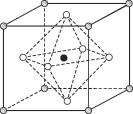
¢ŸNa3OClæß∞˚÷–£¨ClŒª”⁄∏˜∂•µ„Œª÷√£¨NaŒª”⁄_________Œª÷√£¨¡Ω∏ˆNa÷ƺ‰µƒ◊Ó∂Ãæý¿ÎŒ™________nm°£
¢⁄”√a°¢d±Ì æ∞¢∑¸º”µ¬¬Þ≥£ ˝µƒ÷µNA=__________________£®¡–º∆À„ Ω£©°£
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°ø µ—È “÷∆»°SO2µƒ∑¥”¶‘≠¿ÌŒ™£∫Na2SO3£´H2SO4£®≈®£©![]() Na2SO4£´SO2°¸£´H2O°£«Î”√œ¬¡–◊∞÷√…˺∆“ª∏ˆ µ—È£¨“‘≤‚∂®SO2◊™ªØŒ™SO3µƒ◊™ªØ¬ £∫
Na2SO4£´SO2°¸£´H2O°£«Î”√œ¬¡–◊∞÷√…˺∆“ª∏ˆ µ—È£¨“‘≤‚∂®SO2◊™ªØŒ™SO3µƒ◊™ªØ¬ £∫

£®1£©◊∞÷√µƒ¡¨Ω”À≥–Ú£®∞¥∆¯ÃÂ◊Û”“µƒ∑ΩœÚ£© «____°˙_____°˙_____°˙_____°˙_______°˙_____°˙_____°˙_____£®ÃÓ∏˜Ω”ø⁄µƒ±ý∫≈£©°£
£®2£©¥”““¥¶æ˘‘»Õ®»ÎO2£¨Œ™ πSO2”–Ωœ∏þµƒ◊™ªØ¬ £¨ µ—È ±¢Ò¥¶µŒ»Î≈®¡ÚÀ·”΢ڥ¶º”»»¥þªØº¡µƒœ»∫ÛÀ≥–Ú «__________________________________________________°£
£®3£©¢Ù¥¶π€≤ÏµΩµƒœ÷œÛ «___________________________________________°£
£®4£©»ÙII÷–∑¥”¶‘⁄ µ±µƒ∑¥”¶◊¥øˆœ¬£¨∑¥”¶¥Ô◊Ó¥ÛœÞ∂»“‘∫Û£¨œ¬¡–Àµ∑®’˝»∑µƒ «__________°£
A£ÆSO2≈®∂»±ÿ∂®µ»”⁄O2≈®∂»µƒ¡Ω±∂
B£ÆSO2°¢O2°¢SO3µƒ∑÷◊” ˝÷Ʊ» «2°√1°√2
C£ÆSO2”ÎO2≤ª‘ŸªØ∫œ…˙≥…SO3
D£Æ∑¥”¶ªÏ∫œŒÔ∏˜≥…∑÷µƒ∞Ÿ∑÷◊È≥…≤ª‘Ÿ±‰ªØ
£®5£©‘⁄¢Ò¥¶”√¥Ûªº”»»…’∆ø ±£¨SO2µƒ◊™ªØ¬ ª·_______£®ÃÓ°∞‘ˆ¥Û°±°∞≤ª±‰°±ªÚ°∞ºı–°°±£©°£
£®6£©”√nmol Na2SO3∑€ƒ©”Î◊„¡ø≈®¡ÚÀ·Ω¯––¥À µ—È£¨µ±∑¥”¶Ω· ¯ ±£¨ºÃ–¯Õ®»ÎO2“ª∂Œ ±º‰∫Û£¨≥∆µ√III¥¶‘ˆ÷ÿmg£¨‘Ú±æ µ—È÷–SO2µƒ◊™ªØ¬ Œ™______________________°££®”√n°¢m±Ì 棩
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°øœ¬¡–Àµ∑®’˝»∑µƒ «![]()
A.CO°¢NO°¢![]() ∂º «¥Û∆¯Œ€»æ∆¯Ã£¨‘⁄ø’∆¯÷–∂ºƒÐŒ»∂®¥Ê‘⁄
∂º «¥Û∆¯Œ€»æ∆¯Ã£¨‘⁄ø’∆¯÷–∂ºƒÐŒ»∂®¥Ê‘⁄
B.√˜∑Ø‘⁄ÀÆ÷–…˙≥…µƒ![]() Ω∫Ô–Œ¸∏Ω–‘£¨“Ú¥À≥£”√√˜∑Ø∂‘ÀÆΩ¯––œ˚∂æ
Ω∫Ô–Œ¸∏Ω–‘£¨“Ú¥À≥£”√√˜∑Ø∂‘ÀÆΩ¯––œ˚∂æ
C.![]() °¢
°¢![]() ªÚ
ªÚ![]() ∂ºª·µº÷¬À·”͵ƒ–Œ≥…
∂ºª·µº÷¬À·”͵ƒ–Œ≥…
D.ªÓ–‘Ãø°¢![]() °¢
°¢![]() ∂ºƒÐ π∆∑∫ϻГ∫Õ …´£¨‘≠¿Ì≤ªÕ¨
∂ºƒÐ π∆∑∫ϻГ∫Õ …´£¨‘≠¿Ì≤ªÕ¨
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°ø∏˘æðœ¬√ʵƒ∑¥”¶¬∑œþº∞À˘∏¯–≈œ¢ÃÓø’°£
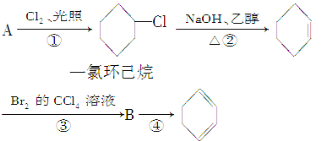
£®1£©AµƒΩ·ππºÚ Ω «______£¨√˚≥∆ «______°£
£®2£©¢Ÿµƒ∑¥”¶¿ý–Õ «______£¨¢⁄µƒ∑¥”¶¿ý–Õ «______°£
£®3£©∑¥”¶¢ÐµƒªØ—ß∑Ω≥Ã Ω «__________________________________
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°ø◊‘¥”1902ƒÍµ¬π˙ªØ—ߺ“π˛≤Æ—–æø≥ˆ∫œ≥…∞±µƒ∑Ω∑®“‘¿¥£¨µ™µƒπÃ∂®µƒœýπÿ—–æøªÒµ√¡À≤ª∂œµƒ∑¢’π°£
£®1£©œ¬±Ì¡–柡À≤ªÕ¨Œ¬∂»œ¬¥Û∆¯πõ™µƒ≤ø∑÷∆Ω∫‚≥£ ˝K÷µ°£
∑¥”¶ | ¥Û∆¯πõ™N2(g)+O2(g) | |
Œ¬∂»/°Ê | 27 | 2260 |
K | 3.84°¡10-31 | 1 |
¢Ÿ∑÷Œˆ ˝æðø…÷™£∫¥Û∆¯πõ™∑¥”¶ Ù”⁄______£®ÃÓ°∞Œ¸»»°±ªÚ°∞∑≈»»°±£©∑¥”¶°£
¢⁄2260°Ê ±£¨œÚ2 L√б’»ð∆˜÷–≥‰»Î0.3mol N2∫Õ0.3mol O2£¨20 s ±∑¥”¶¥Ô∆Ω∫‚°£‘Ú¥À ±µ√µΩNO____mol£¨”√N2±Ì 浃∆Ωæ˘∑¥”¶ÀŸ¬ Œ™____°£
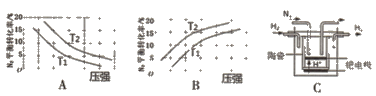
£®2£©“—÷™π§“µπõ™∑¥”¶£∫N2(g)+3H2(g) ![]() 2NH3 (g) °˜H<0£¨‘⁄∆‰À˚Ãıº˛œýÕ¨ ±£¨∑÷±≤‚∂®¥À∑¥”¶÷–N2µƒ∆Ω∫‚◊™ªØ¬ ÀÊ—π«ø∫ÕŒ¬∂»(T)±‰ªØµƒ«˙œþ»Áœ¬ÕºA°¢BÀ˘ 棨∆‰÷– ’˝»∑µƒ «_____£®ÃÓ°∞A°±ªÚ°∞B°±£©£¨T1______T2£®ÃÓ°∞>°±ªÚ°∞<°±£©°£
2NH3 (g) °˜H<0£¨‘⁄∆‰À˚Ãıº˛œýÕ¨ ±£¨∑÷±≤‚∂®¥À∑¥”¶÷–N2µƒ∆Ω∫‚◊™ªØ¬ ÀÊ—π«ø∫ÕŒ¬∂»(T)±‰ªØµƒ«˙œþ»Áœ¬ÕºA°¢BÀ˘ 棨∆‰÷– ’˝»∑µƒ «_____£®ÃÓ°∞A°±ªÚ°∞B°±£©£¨T1______T2£®ÃÓ°∞>°±ªÚ°∞<°±£©°£
£®3£©20 ¿ºÕƒ©£¨ø∆—ߺ“≤…”√∏þ÷ ◊”µºµÁ–‘µƒSCYÃ’¥…£®ƒÐ¥´µðH+£©Œ™ΩÈ÷ £¨”√Œ¸∏Ω‘⁄À¸ ƒ⁄Õ‚±Ì√Ê…œµƒΩ ÙÓŸ∂ýæß±°ƒ§◊ˆµÁº´£¨Õ®π˝µÁΩ‚ µœ÷∏þŒ¬≥£—πœ¬µƒµÁªØ—ß∫œ≥…∞±°£∆‰ æ“‚Õº»ÁCÀ˘ 棨“ıº´µƒµÁº´∑¥”¶ ΩŒ™______°£
£®4£©Ω¸ƒÍ£¨”÷”–ø∆—ߺ“÷≥ˆ‘⁄≥£Œ¬°¢≥£—π°¢¥þªØº¡µ»Ãıº˛œ¬∫œ≥…∞±µƒ–¬Àº¬∑£¨∑¥”¶‘≠¿ÌŒ™£∫2N2(g)+6H2O(l)![]() 4NH3 (aq) +3O2(g) °˜H°£
4NH3 (aq) +3O2(g) °˜H°£
“—÷™£∫¢ŸN2(g)+3H2(g) ![]() 2NH3(g) °˜H1
2NH3(g) °˜H1
¢⁄2H2(g) +O2(g) ![]() 2H2O£®1£© °˜H2
2H2O£®1£© °˜H2
¢€NH3(g) ![]() NH3(aq) °˜H3
NH3(aq) °˜H3
‘Ú°˜H= ________£®”√∫¨°˜H1°¢°˜H2°¢°˜H3µƒ Ω◊”±Ì 棩°£
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
∞Ÿ∂»÷¬–≈ - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com