
����Ŀ�����ֶ�����Ԫ��A��B��C��D��E��F��G��ԭ��������������A��Eͬ�壬D��Fͬ�壬C���ӡ�D���Ӻ�E���Ӿ�����ͬ�ĵ��Ӳ�ṹ��A���E�����Ԫ�ؾ����γɹ����ͻ����A��C�γɵĻ�������ˮ�гʼ��ԣ�C��D���ڣ�B���γɻ�������������Ԫ�ء�
�ش��������⣺
��1������Ԫ���У�ԭ�Ӱ뾶������_____����Ԫ�ط��ţ�����Ԫ�������ڱ��е�λ��_______
��2����A��D��E��Ԫ����ɵĻ�����û����ﺬ�еĻ�ѧ������Ϊ__________��
��3��A��B�γɵ�10���ӻ�����û�����Ŀռ乹��Ϊ__________
��4����A��C��D����Ԫ���γɵĻ�����Ⱥ������Ӽ��ֺ��й��ۼ����û�����Ļ�ѧʽΪ________
��5��������Ԫ����ɵ�����дһ����Ӧ����ʽ��Ҫ���ܹ�֤���ǽ�����G>F___
��6��A��D��D��E�γɵĻ����ﶼ����������ȡ����D���������ڹ��ۻ���������ȡ����D�ķ�Ӧ����ʽΪ___________
���𰸡�Na ��������IA�� ���Ӽ��������ԣ����ۼ� �������� NH4NO3 Cl2��H2S=2HCl��S�� 2H2O2 ![]() 2H2O��O2��
2H2O��O2��
��������
A��C�γɵĻ�������ˮ�гʼ��ԣ��û�����ΪNH3����AΪH��CΪN��C��D���ڣ��Ƴ�DΪO��B���γɻ�������������Ԫ�أ���BΪC����Ϊ�Ƕ�����Ԫ�أ���ԭ��������������A��Eͬ�壬��EΪNa��D��Fͬ���壬��FΪS��GΪCl��������
A��C�γɵĻ�������ˮ�гʼ��ԣ��û�����ΪNH3����AΪH��CΪN��C��D���ڣ��Ƴ�DΪO��B���γɻ�������������Ԫ�أ���BΪC����Ϊ�Ƕ�����Ԫ�أ���ԭ��������������A��Eͬ�壬��EΪNa��D��Fͬ���壬��FΪS��GΪCl��
��1������ͬ������ϵ��£�ԭ�Ӱ뾶����ͬ���ڴ�������ԭ�Ӱ뾶��С��������ֶ�������ԭ�Ӱ뾶������Na��λ�ڵ�������IA�壻
��2��A��D��E����Ԫ����ɵĻ�������NaOH��NaOH�������ӻ�����������Ӽ���(����)���ۼ���
��3��A��B�γ�10���ӻ�������CH4����ռ乹��Ϊ���������Σ�
��4���������Ӽ����û�����Ϊ���ӻ������H��N��O��ɵĻ�����Ϊ��Σ���ѧʽΪNH4NO3��
��5��֤���ǽ�����Clǿ��S�����Բ����û���Ӧ����Cl2��H2S=2HCl��S����
��6��A��D���ɵĻ�������H2O��H2O2��D��E�γɵĻ�����Na2O��Na2O2��������ȡ����O2��ǰ��ΪH2O2������ΪNa2O2�����ڹ��ۻ��������H2O2������Ӧ����ʽΪ2H2O2 ![]() 2H2O��O2����
2H2O��O2����


 ��������ܸ�ϰϵ�д�
��������ܸ�ϰϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���л���G(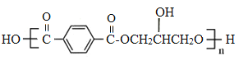 )��һ����Ҫ���л��߷��Ӳ��ϣ�ʵ�������л���A�Ʊ�G��һ�ֺϳ�·�����£�
)��һ����Ҫ���л��߷��Ӳ��ϣ�ʵ�������л���A�Ʊ�G��һ�ֺϳ�·�����£�

�ش��������⣺
��1��D��������________B�����к��еĹ����ŵ�������___________________________��
��2��A��B��B��C�ķ�Ӧ���ͷֱ�Ϊ_____________________��_________________________��
��3������˵����ȷ����_____________________������ĸ��ţ���
a��A���Ӵ���˳���칹
b��������NaHCO3����D��F
c��E�����������14��ԭ��λ��ͬһƽ����
��4��д��D+F��G�Ļ�ѧ����ʽ________________________��
��5��H��F��ͬϵ�����Է���������F��28��H�ĺ˴Ź�������������壬�������Ϊ3�U1�U1������ϸ�������H��ͬ���칹�干��______�֣�д������H��һ�ֽṹ��ʽ___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�����ʹ����ƽ��H2O![]() H++OH�������ƶ�����ʹҺ������Ե��ǣ�������
H++OH�������ƶ�����ʹҺ������Ե��ǣ�������
A. ��ˮ�м�����������������
B. ��ˮ�м��������������ƹ���
C. ��ˮ�м�������̼���ƹ���
D. ��ˮ���ȵ�100�棬ʹˮ��pH=6
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪ij��Һ��ֻ����OH����H����NH4����Cl���������ӣ�ijͬѧ�Ʋ�������Ũ�ȴ�С˳��������������ֹ�ϵ��
��c(Cl��)>c(NH4��)>c(H��)>c(OH��) ��c(NH4��)>c(OH��)>c(Cl��)>c(H��)
��c(NH4��)>c(Cl��)>c(OH��)>c(H��) ��c(Cl��)>c(H��)>c(NH4��)>c(OH��)
��д���пհף�
��1������Һ��ֻ����һ�����ʣ����������______��������������Ũ�ȵĴ�С˳��Ϊ________(�����)��
��2�����������ӵĹ�ϵ���Ϣۣ�������Ϊ____________________________��
���������ӵĹ�ϵ���Ϣܣ�������Ϊ____________________________��
��3����pH��ͬ��NH4Cl��Һ��HCl��Һϡ����ͬ�ı�����������ͼ����ȷ����________(��ͼ�����)��

��4��������Һ���������ȵ�ϡ����Ͱ�ˮ��϶��ɣ���ǡ�ó����ԣ�����ǰc(HCl)________c(NH3��H2O)(����ڡ�����С�ڡ����ڡ�����ͬ)�����ǰ����c(H��)�ͼ���c(OH��)�Ĺ�ϵΪc(H��)________c(OH��)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧС�鹹�뽫����β��(NO��NO2)ת��Ϊ��Ҫ�Ļ���ԭ��HNO3����ԭ����ͼ��ʾ������A��BΪ�������ϡ�����˵��һ����ȷ���ǣ� ��

A. �õ�ع���ʱ�����ӵ��������·��A��B���ڵ�·��B��A�γɱպϻ�·
B. �缫B������HNO3Ũ������
C. A�缫�ķ�ӦΪ��NO2��e����H2O==NO3-��2H�� NO��3e����2H2O===NO3-��4H��
D. �õ�ع���ʱ��ÿ����11.2LO2(��״����)�����Գ�ȥ��1molNO��NO2�Ļ��β��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1200ʱ����Ȼ���������лᷢ�����з�Ӧ��
H2S(g)+3/2O2(g)=SO2(g)+H2O(g) ��H1
2H2S(g)+SO2(g)=3/2S2(g)+2H2O(g) ��H2
H2S(g)+1/2O2(g)=S(g)+H2O(g) ��H3
2S(g)=S2(g) ��H4
����H4����ȷ����ʽΪ
A. ��H4= 2/3(��H1+��H2- 3��H3) B. ��H4= 2/3(3��H3-��H1-��H2)
C. ��H4= 3/2(��H1+��H2- 3��H3) D. ��H4= 3/2(��H1-��H2- 3��H3)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Cu�۷���ϡH2SO4�У����Ⱥ�����������һ���κ�Cu���������٣�����Һ������ͬʱ���������ɣ�������
A.�Ȼ���B.������C.������D.̼����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ö��Ե缫���һ����������ͭ��Һ��ʵ��װ����ͼ�����������е�ʵ��������ͼ�����������ʾ��������ת�Ƶ��ӵ����ʵ������������ʾ�������в�����������������״������������˵����ȷ���ǣ� ��

A���������У�b�缫�������к�ɫ�����������������ݲ���
B��a�缫�Ϸ����ķ�Ӧ����ʽΪ��2H+ +2e- = H2���� 4OH-��4e- = 2H2O + O2��
C����P��Q��ʱ�ռ����Ļ�������ƽ��Ħ������Ϊ12g��mol-1
D������0��P�α�ʾH2��O2������������仯������P��Q�α�ʾO2������仯
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и�������ȷ����( )
A. ��֪H��(aq)��OH��(aq) == H2O(l) ��H����57.3 kJ��mol-1����H2SO4��Ba(OH)2��Ӧ�ķ�Ӧ�� ��H��2��(��57.3) kJ��mol-1
B. ��֪CH3OH(g)��1/2O2(g) == CO2(g)��2H2(g)����H����192.9 kJ��mol-1����CH3OH(g)��ȼ����Ϊ192.9 kJ��mol-1
C. H2(g)��ȼ������285.8 kJ��mol-1 ����2H2O(g) == 2H2(g)��O2(g)����H����571.6 kJ��mol-1
D. �����ǵ�ȼ������2800 kJ��mol-1����1/2C6H12O6(s)��3O2(g) == 3CO2(g)��3H2O(l) ��H����1400 kJ��mol-1
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com