
| A. | 只有非金属原子间才能形成共价键 | |
| B. | 有化学键断裂的变化属于化学变化 | |
| C. | 由共价键形成的物质-定是共价化合物分子 | |
| D. | 离子化合物中可能含有共价键,而共价化合物中一定不含离子键 |
分析 含有离子键的化合物是离子化合物,离子化合物中可能含有共价键,只含共价键的化合物是共价化合物,共价化合物中一定不含离子键,共价键可存在于非金属性单质和化合物中,以此解答.
解答 解:A.金属性较弱的金属与非金属也可形成共价键,如氯化铝是由金属元素形成的共价键,故A错误;
B.化学变化的实质是旧化学键的断裂和新化学键的形成,有化学键的断裂不一定是化学变化,如HCl溶于水H-Cl键断裂,属于物理变化,故B错误;
C.由共价键形成的分子也可能为单质,如氧气等,故C错误;
D.部分离子化合物中也可能存在共价键,如NaOH等,共价化合物中只有共价键,故D正确.
故选D.
点评 本题考查了化学键和物质的关系,题目难度不大,明确共价键和离子键的区别,易错选项是A,注意并不是只有非金属原子间才能形成共价键,为易错点.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,11.2 L的戊烷所含的分子数为0.5NA | |
| B. | 0.5mol C3H8分子中含C-H共价键2NA | |
| C. | 11.2 L二氯甲烷所含分子数为0.5NA | |
| D. | 现有乙烯、丙烯、丁烯的混合气体共14 g,其原子数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 (或
(或
 ).
).查看答案和解析>>
科目:高中化学 来源: 题型:解答题
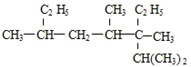 2,3,4,6-四甲基-3-乙基辛烷
2,3,4,6-四甲基-3-乙基辛烷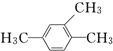 1,2,4-三甲苯
1,2,4-三甲苯查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在气体发生装置上直接点燃甲烷气体必须先检验甲烷的纯度 | |
| B. | 制备乙酸乙酯时,将乙醇和乙酸依次加入浓硫酸中 | |
| C. | 给试管中的液体加热,不时移动试管或加人碎瓷片,以免液体暴沸伤人 | |
| D. | 实验时不慎打破温度计水银球,应立即用滴管将水银吸出,放如水封的小瓶中,残破的温度计插人装有硫粉的广口瓶中 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
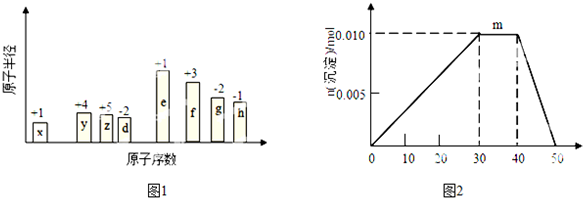
| 元素 | 有关信息 |
| X | 最外层电子数是次外层的2倍 |
| Y | 元素主要化合价为-2价 |
| Z | 其单质及化合物的焰色为黄色 |
| M | 与X同主族,其单质为半导体材料 |
| N | 其单质在Y单质中燃烧,发出明亮的蓝紫色火焰 |
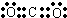 ;
;
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②过程中都只发生了物理变化 | |
| B. | 石油主要是由各种烷烃、环烷烃、芳香烃组成的混合物 | |
| C. | 石油的分馏产品中不能得到汽油、柴油 | |
| D. | ③是加成反应,产物名称是1,2-溴乙烷 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com