���㣺λ�ýṹ���ʵ����ϵӦ��,���ʵ�����Ũ����ʱ��ı仯����
ר�⣺Ԫ����������Ԫ�����ڱ�ר��,��ѧƽ��ר��
������BԪ�صĻ���������࣬��Ŀ�Ӵ�BΪCԪ�أ�C��D����Ԫ���γɵĵ����ǿ����к����������ʣ�ΪO
2��N
2������ԭ����������������CΪNԪ�أ�DΪOԪ�أ�D��E��Ԫ�ؿ����������ֲ�ͬ�����ӻ������EΪNaԪ�أ�����ԭ�Ӻ���ĵ��Ӳ���֮��Ϊ10����Aԭ�ӵ��Ӳ���=10-2-2-2-3=1����AΪHԪ�أ�
��1��A��D��Ԫ���γ��䳣��������ΪH
2O��E�ĵ�����Na���ƺ�ˮ��Ӧ�����������ƺ�������
��2��A��C��D��Ԫ�����γɳ�����A
4C
2D
3��ӦΪNH
4NO
3��笠�����ˮ���ʹ����Һ�����ԣ�
��3��B����Է���������С���⻯��ΪCH
4��������ȫȼ�����ɶ�����̼��ˮ��
��4����X��Y�Ǿ���C��D��Ԫ����ɵĻ������C��D��X��Y�еļ�̬��ͬ��������������NO
2��N
2O
4������X��YŨ�ȱ仯ȷ�����������ʷֱ���ʲô��
�ڻ�ѧ��Ӧ�ﵽƽ��״̬ʱ���������ʵ�Ũ�Ȳ��䣻
�ۻ�ѧƽ�ⳣ��K=
��
�ܸ���ͼ��֪X��YŨ���Ƿ�仯��ȷ���ı�������
���
�⣺BԪ�صĻ���������࣬��Ŀ�Ӵ�BΪCԪ�أ�C��D����Ԫ���γɵĵ����ǿ����к����������ʣ�ΪO
2��N
2������ԭ����������������CΪNԪ�أ�DΪOԪ�أ�D��E��Ԫ�ؿ����������ֲ�ͬ�����ӻ������EΪNaԪ�أ�����ԭ�Ӻ���ĵ��Ӳ���֮��Ϊ10����Aԭ�ӵ��Ӳ���=10-2-2-2-3=1����AΪHԪ�أ�
��1��A��D��Ԫ���γ��䳣��������ΪH
2O��E�ĵ�����Na���ƺ�ˮ��Ӧ�����������ƺ����������ӷ�Ӧ����ʽΪ��2Na+2H
2O=2Na
++2OH
-+H
2�����ʴ�Ϊ��2Na+2H
2O=2Na
++2OH
-+H
2����
��2��A��C��D��Ԫ�����γɳ�����A
4C
2D
3��ӦΪNH
4NO
3��笠�����ˮ���ʹ����Һ�����ԣ�ˮ�����ӷ���ʽΪNH
4++H
2O=NH
3?H
2O+H
+���ʴ�Ϊ���NH
4++H
2O=NH
3?H
2O+H
+��
��3��B����Է���������С���⻯��ΪCH
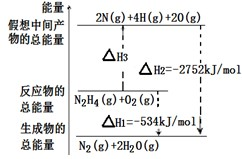
4��������ȫȼ�����ɶ�����̼��ˮ����ȼ���Ȼ�ѧ����ʽΪCH
4��g��+2O
2��g����CO
2��g��+2H
2O��l����H=-890.3KJ/mol���ʴ�Ϊ��CH
4��g��+2O
2��g����CO
2��g��+2H
2O��l����H=-890.3KJ/mol��
��4����X��Y�Ǿ���C��D��Ԫ����ɵĻ������C��D��X��Y�еļ�̬��ͬ��������������NO
2��N
2O
4��
��Y��Ũ�ȼ���0.2mol/Lʱ��X��Ũ������0.4mol/L��ͬһʱ��Ρ�ͬһ��ѧ��Ӧ�У����ʵ���Ũ�ȵı仯��֮�ȵ����������֮�ȣ�����X�ļ�������2��Y�ļ�������1����X�Ļ�ѧʽΪNO
2���ʴ�Ϊ��NO
2��
�ڻ�ѧ��Ӧ�ﵽƽ��״̬ʱ���������ʵ�Ũ�Ȳ��䣬����ͼ��֪��b���ʾƽ��״̬���ʴ�Ϊ��b��
�۸���ͼ��֪��Y�Ƿ�Ӧ�X��������䷴Ӧ����ʽΪN
2O
4��g��?2NO
2��g������ѧƽ�ⳣ��K=
=
=0.8���ʴ�Ϊ��0.8��
�ܸ���ͼ��֪��t
2ʱ�̣�XŨ������YŨ�Ȳ��䣬���Ըı������������NO
2��Ũ�ȣ��ʴ�Ϊ������NO
2��Ũ�ȣ�
���������⿼����λ�ýṹ���ʵ����ϵ��Ӧ�ã��漰��ѧƽ�⡢�Ȼ�ѧ��Ӧ����ʽ����д������ˮ���֪ʶ�㣬����ԭ�ӽṹ��Ԫ�صĺ�����֪ʶ����ȷ��Ԫ�أ��ٽ���ε�����ȷ����Һ����ԡ���������Ի�ѧƽ���Ӱ�졢��ѧƽ�ⳣ���ļ����֪ʶ�������������Ŀ�ѶȲ���

 ����������Ԫ��A��B��C��D��E��ԭ�����������������ǵ�ԭ�Ӻ������֮��Ϊ10��B�Ļ���������࣬��Ŀ�Ӵ�C��D�ǿ����к�����������Ԫ�أ�D��E�����ʿ����������ֲ�ͬ�����ӻ����
����������Ԫ��A��B��C��D��E��ԭ�����������������ǵ�ԭ�Ӻ������֮��Ϊ10��B�Ļ���������࣬��Ŀ�Ӵ�C��D�ǿ����к�����������Ԫ�أ�D��E�����ʿ����������ֲ�ͬ�����ӻ����