
10℃时加热饱和NaHCO3溶液,测得该溶液的pH发生如表所示的变化。
温度/℃ | 10 | 20 | 30 | 加热煮沸后冷却到50℃ |
pH | 8.3 | 8.4 | 8.5 | 8.8 |
甲同学认为,该溶液pH增大的原因是HCO 的水解程度增大,故碱性增强,有关反应的离子方程式为__________________________。乙同学认为,溶液pH增大的原因是NaHCO3受热分解生成了Na2CO3,并推断Na2CO3的水解程度________(填“大于”或“小于”)NaHCO3的水解程度,该分解反应的化学方程式为______________________________。
的水解程度增大,故碱性增强,有关反应的离子方程式为__________________________。乙同学认为,溶液pH增大的原因是NaHCO3受热分解生成了Na2CO3,并推断Na2CO3的水解程度________(填“大于”或“小于”)NaHCO3的水解程度,该分解反应的化学方程式为______________________________。
丙同学认为,甲、乙的判断都不充分,他进行如下探究来验证他们的判断是否正确。
(1)在加热煮沸的溶液中加入足量的试剂X,若产生沉淀,则________(填“甲”或“乙”)的判断正确,试剂X是________(填序号)。
A.Ba(OH)2溶液 B.BaCl2溶液
C.NaOH溶液 D.澄清石灰水
(2)将加热后的溶液冷却到10℃,若溶液的pH________(填“大于”“小于”或“等于”)8.3,则________(填“甲”或“乙”)的判断正确。
(3)丙同学查阅资料后发现,NaHCO3的分解温度为150℃,他断言________(填“甲”或“乙”)的判断是错误的,原因是________________________________________________。
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源:2014年高考化学题型冲刺练习 化学基本概念、解决化学与STSE问题(解析版) 题型:选择题
下列实验或生产过程中发生的变化是物理变化的是( )
①在鸡蛋白溶液中加入(NH4)2SO4后形成沉淀;
②用渗析的方法除去混在Fe(OH)3胶体中的FeCl3;
③NO2经加压凝聚成无色的液体;
④溴水滴入植物油中振荡褪色;
⑤水泥、沙子和水混合后硬化;⑥照相底片感光。
A.①②③ B.②④⑥ C.①② D.③⑤
查看答案和解析>>
科目:高中化学 来源:2014年高考化学苏教版一轮复习专练2 阿伏加德罗常数的判断练习卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值。下列叙述正确的是 ( )。
A.25 ℃,1 L pH=1的稀硫酸中含有的H+数为0.1 NA
B.标准状况下,224 mL水含有的电子数为0.1 NA
C.常温常压下,0.56 L甲烷中含有的共价健数为0.1 NA
D.0.15 mol NO2与水完全反应时转移的电子数为0.15 mol NA
查看答案和解析>>
科目:高中化学 来源:2014年高考化学苏教版一轮复习专练2 阿伏加德罗常数的判断练习卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的数值,下列说法正确的是( )。
A.常温下,4 g CH4含有NA个C—H共价键
B.1 mol Fe 与足量的稀HNO3反应,转移2NA个电子
C.1 L 0.1 mol·L-1 NaHCO3溶液中含有0.1NA 个HCO3-
D.常温常压下,22.4 L的NO2和CO2混合气体含有2NA个O原子
查看答案和解析>>
科目:高中化学 来源:2014年高考化学苏教版一轮复习专练1 化学实验仪器的创新使用练习卷(解析版) 题型:选择题
用如图所示装置制取表格中的四种干燥、纯净的气体(必要时可以加热;a、b、c、d表示相应仪器中加入的试剂)。其中正确的是 ( )。
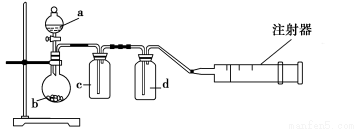
选项 | 气体 | a | b | c | d |
A | SO2 | 浓硫酸 | Cu | H2O | 浓硫酸 |
B | Cl2 | 浓盐酸 | MnO2 | NaOH溶液 | 浓硫酸 |
C | NH3 | 饱和NH4Cl溶液 | 消石灰 | 空集气瓶 | 固体NaOH |
D | NO | 稀硝酸 | 铜屑 | H2O | 浓硫酸 |
查看答案和解析>>
科目:高中化学 来源:2014年高中化学鲁科版选修四第3章 物质在水溶液中的行为练习卷(解析版) 题型:选择题
Mg(OH)2在水中达到溶解平衡:Mg(OH)2(s) Mg2++2OH-,下列哪种情况可使Mg(OH)2(s)的量减少( )
Mg2++2OH-,下列哪种情况可使Mg(OH)2(s)的量减少( )
A.加入MgCl2溶液 B.加入少量NaOH
C.加入NH4NO3溶液 D.加入K2S溶液
查看答案和解析>>
科目:高中化学 来源:2014年高中化学鲁科版选修四第3章 物质在水溶液中的行为练习卷(解析版) 题型:选择题
在25℃时,将pH=11的NaOH溶液与pH=3的CH3COOH溶液等体积混合后,下列关系式中正确的是( )
A.[Na+]=[CH3COO-]+[CH3COOH]
B.[H+]=[CH3COO-]+[OH-]
C.[Na+]>[CH3COO-]>[OH-]>[H+]
D.[CH3COO-]>[Na+]>[H+]>[OH-]
查看答案和解析>>
科目:高中化学 来源:2014年高中化学鲁科版选修四第1章 化学反应与能量转化练习卷(解析版) 题型:选择题
燃料电池是燃料(如CO、H2、CH4)等跟O2(或空气)起反应将化学能转变为电能的装置,电解质溶液是强碱(如KOH)溶液,下列关于甲烷燃料电池的说法中不正确的是( )
A.通入氧气的一极发生还原反应,通入甲烷的一极发生氧化反应
B.负极的电极反应式为CH4+10OH--8e-=CO32—+7H2O
C.随着反应的进行,电解质溶液的pH保持不变
D.甲烷燃料电池的能量利用率比甲烷燃烧的大
查看答案和解析>>
科目:高中化学 来源:2014年高中化学苏教版选修四专题3 溶液中的离子反应练习卷(解析版) 题型:选择题
室温下,将1.000 mol·L-1盐酸滴入20.00 mL 1.000 mol·L-1氨水中,溶液pH和温度随加入盐酸体积变化曲线如图所示。
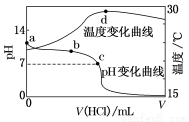
下列有关说法正确的是( )
A.a点由水电离出的c(H+)=1.0×10-14 mol·L-1
B.b点:c(NH )+c(NH3·H2O)=c(Cl-)
)+c(NH3·H2O)=c(Cl-)
C.c点:c(Cl-)=c(NH )
)
D.d点后,溶液温度略下降的主要原因是NH3·H2O电离吸热
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com