
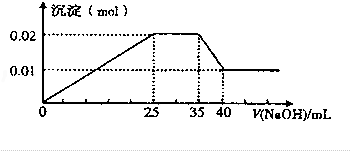
 现有一无色溶液含有以下离子(忽略由水电离产生的H+、OH-):NH4+、Mg2+、Al3+、NO3-,取100mL该溶液并逐滴滴加NaOH溶液,测得沉淀的物质的量与NaOH溶液的体积关系如图所示,则NO3-的物质的量是( )
现有一无色溶液含有以下离子(忽略由水电离产生的H+、OH-):NH4+、Mg2+、Al3+、NO3-,取100mL该溶液并逐滴滴加NaOH溶液,测得沉淀的物质的量与NaOH溶液的体积关系如图所示,则NO3-的物质的量是( )| A. | 0.08mol | B. | 0.07mol | C. | 0.06mol | D. | 0.05mol |
分析 无色溶液逐滴滴加NaOH 溶液,由图可知,开始加入氢氧化钠溶液有沉淀生成,说明一定不含有H+;沉淀最大时,继续滴加氢氧化钠溶液,沉淀部分溶解,推断一定含有Al3+;图象中有一段平台,说明加入OH-时无沉淀生成,有NH4+,NH4++OH-=NH3•H2O,说明含有铵根离子,最后溶液中有沉淀,说明溶液中含Mg2+,由此结合溶液中的电荷守恒分析解答.
解答 解:由图可知,开始加入氢氧化钠溶液有沉淀生成,说明不含有H+;沉淀最大时,继续滴加氢氧化钠溶液,沉淀部分溶解,推断一定含有Al3+;图象中有一段平台,说明加入OH-时无沉淀生成,有NH4+,NH4++OH-=NH3•H2O,说明含有铵根离子,最后沉淀不能完全溶液,说明溶液中含Mg2+,由则生成的0.01mol沉淀为Mg(OH)2,n(Mg(OH)2)=0.01mol,铝离子和NaOH溶液反应生成Al(OH)3沉淀为0.01mol,即n(Al3+)=0.01mol,Al(OH)3和NaOH反应生成NaAlO2需要NaOH溶液的体积是5mL,则铝离子和NaOH溶液反应生成Al(OH)3沉淀时需要NaOH溶液的体积是15mL,则生成氢氧化镁需要NaOH溶液的体积是10mL,所以c(NaOH)=$\frac{0.02mol}{0.01L}$=2.00mol/L,铵根离子消耗10mL的氢氧化钠,根据NH4++OH-=NH3•H2O,得到:n(NH4+)=2.00mol/L×0.01L=0.02mol,根据电荷守恒,硝酸根离子物质的量n=0.02mol+0.01mol×3+0.01mol×2=0.07mol,
故选B.
点评 本题考查了离子共存、离子反应的计算等知识点,定性分析离子共存、定量分析离子的物质的量是解本题的关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | c(Na+)>c(CO32-)>c(HCO3-) | |
| B. | c(Na+)+c(H+)=c(HCO3-)+2c(CO32-)+c(OH-) | |
| C. | c(Na+)>c(HCO3-)>c(H+)>c(OH-) | |
| D. | c(HCO3-)+2c(CO32-)+c(H2CO3)=1 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④ | B. | 只有②④ | C. | 只有①②③ | D. | 只有④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
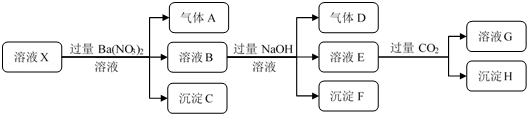
| A. | 根据上述连续实验不能确定溶液X中是否含有Fe3+ | |
| B. | 沉淀H为Al(OH)3 | |
| C. | 溶液中一定含有H+、Al3+、NH4+、Fe2+、SO42-、Cl- | |
| D. | 若溶液X为100 mL,产生的气体A为112 mL(标况),则X中c(Fe2+)=0.15 mol•L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 将足量CO2通入100mLKOH和Ca(OH)2的混合溶液中,生成沉淀的物质的量(n)和通入标况下CO2体积(V)的关系如图所示,则混合溶液中KOH的物质的量浓度为( )
将足量CO2通入100mLKOH和Ca(OH)2的混合溶液中,生成沉淀的物质的量(n)和通入标况下CO2体积(V)的关系如图所示,则混合溶液中KOH的物质的量浓度为( )| A. | 10(b-a)/22.4 mol/L | B. | 20(b-a)/22.4 mol/L | ||
| C. | 10b/22.4 mol/L | D. | 10a/22.4 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
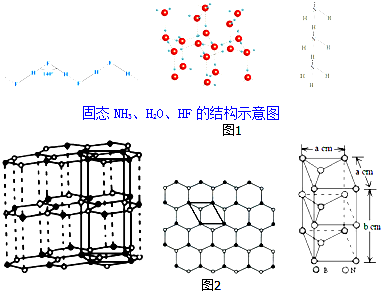
 .
.| 物质 | 氢键X-H…Y | 键能/kJ•mol-1 |
| (HF)n | F-H…F | 28.1 |
| 冰 | O-H…O | 18.8 |
| (NH3)n | N-H…N | 5.4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com