
【题目】下列保存试剂的方法中,错误的是( )
A.漂粉精保存在烧杯中B.新制的氯水保存在棕色瓶中,避光
C.氢氧化钠溶液保存在带木塞的试剂瓶D.碘单质保存在棕色瓶中
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】高炉炼铁过程中发生的主要反应为 ![]() Fe2O3(s)+CO(g)=
Fe2O3(s)+CO(g)= ![]() Fe(s)+CO2(g)已知该反应在不同温度下的平衡常数如下:
Fe(s)+CO2(g)已知该反应在不同温度下的平衡常数如下:
温度/℃ | 1000 | 1150 | 1300 |
平衡常数 | 4.0 | 3.7 | 3.5 |
请回答下列问题:
(1)该反应的平衡常数表达式K= , △H0(填“>”、“<”或“=”);
(2)在一个容积为10L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0mol,反应经过10min后达到平衡.求该时间范围内反应的平均反应速率v(CO2)=、CO的平衡转化率=:
(3)欲提高(2)中CO的平衡转化率,可采取的措施是 .
A.减少Fe的量
B.增加Fe2O3的量
C.移出部分CO2
D.提高反应温度
E.减小容器的容积
F.加入合适的催化剂.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】完成下列化学方程式,并标明反应类型.
(1)CH4+Cl2![]() _______________,______________;
_______________,______________;
(2)CH2=CH2+Br2→_______________,______________;
(3)![]() _______________,______________。
_______________,______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(多选)在一定温度下,容器内某一反应中M,N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( ) 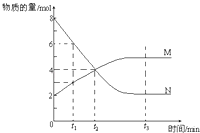
A.反应的化学方程式为:2 NM
B.t2时,正逆反应速率相等,达到平衡
C.t3时,正反应速率大于逆反应速率
D.t1时,N的浓度是M浓度的2倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由金红石(TiO2)制取单质Ti涉及的步骤为:TiO2→TiCl4![]()
已知:①C(s)+O2(g)=CO2(g) △H1=-393.5kJ·mol-1
②2CO(g)+O2(g)=2CO2(g) △H2=-566 kJ·mol-1
③TiO2(s)+2Cl2(g)=TiCl4(s)+O2(g) △H3=+141 kJ·mol-1
则TiO2(s) +2Cl2(g)+2C(s)=TiCl4(s)+2CO(g)的△H是
A. -80 kJ·mol-1 B. -160 kJ·mol-1 C. +160 kJ·mol-1 D. +80kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,反应 2CH3OH(g) ![]() CH3OCH3(g)+H2O(g)的平衡常数为400.此温度下,在容积一定的密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
CH3OCH3(g)+H2O(g)的平衡常数为400.此温度下,在容积一定的密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
物质 | CH3OH | CH3OCH3 | H2O |
浓度/(molL﹣1) | 0.44 | 0.6 | 0.6 |
下列说法正确的是( )
A.CH3OH的起始浓度为1.04mol/L
B.此时逆反应速率大于正反应速率
C.平衡时CH3OH的浓度为0.04mol/L
D.平衡时CH3OH的转化率小于80%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下的密闭容器中:4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g) ΔH=-905.9 kJ·mol-1,下列叙述正确的是
4NO(g)+6H2O(g) ΔH=-905.9 kJ·mol-1,下列叙述正确的是
A. 平衡后升高温度,混合气体中NO含量增大
B. 平衡后降低压强,混合气体平均摩尔质量增大
C. 4molNH3和5molO2反应,达到平衡时放出热量为905.9kJ
D. 平衡时,将水蒸气移除部分,此时逆反应速率降低,正反应速率不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究NOx、SO2、CO等大气污染气体的处理方法具有重要意义。
(1)氮氧化物是造成光化学烟雾和臭氧层损耗的主要气体。已知:
①CO(g)+NO2(g)=NO(g)+CO2(g) △H=-a KJ·mol-1 (a>0)
②2CO(g)+2NO(g)=N2(g)+2CO2(g) △H=-b KJ·mol-1 (b>0)
若用标准状况下3.36LNO2氧化CO至CO2(NO2完全反应)的整个过程中转移电子的物质的量为_____mol,放出的热量为_________ kJ(用含有a和b的代数式表示)。
(2)己知下列反应的反应热:
①CH3COOH(1)+2O2(g)=2CO2(g)+2H2O(1) △H=-870.3kJ/mo1
②C(s)+O2(g) =CO2(g) ΔH=-393.5kJ/mo1
③2C(s)+2H2(g)+O2(g) =CH3COOH(1) ΔH=-488.3kJ/mo1
请写出H2燃烧热的热化学方程式______________________________________。
(3)在101kPa下,CH4(g)、H2(g)、C(s) 的燃烧热分别为890.3kJ/mol、285.8kJ/mol 和393.5kJ/mol,则CH4(g)分解为H2(g)、C(s)的热化学方程式_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为证明铜丝与稀硝酸反应生成的确实是NO,某同学设计了一套装置(如图1所示),有关该实验叙述不正确的是

A. 为保证实验效果,反应开始前,稀硝酸可加到与两侧胶塞相平的位置。
B. 利用该装置可控制反应随时停止或继续反应
C. 生成的气体可利用图2装置来收集
D. 长玻璃管的作用可防止稀硝酸溢出
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com