
| 化学式 | AgCl | Ag2CrO4 | CH3COOH | HClO | H2CO3 |
| KSP或Ka | KSP=1.8×10-10 | KSP=2.0×10-12 | Ka=1.8×10-5 | Ka=3.0×10-8 | Ka1=4.1×10-7 Ka2=5.6×10-11 |
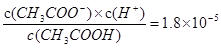 ,由于c(CH3COOH):c(CH3COO-)=5:9,所以氢离子的浓度是10-5mol/L,则pH=5,故C正确;当溶液中氯离子和CrO42-浓度均为0.001mol/L时,要生成相应的沉淀,则需要银离子的浓度分别是
,由于c(CH3COOH):c(CH3COO-)=5:9,所以氢离子的浓度是10-5mol/L,则pH=5,故C正确;当溶液中氯离子和CrO42-浓度均为0.001mol/L时,要生成相应的沉淀,则需要银离子的浓度分别是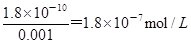 、
、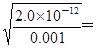 4.47×10-5mol/L,所以首先析出的沉淀是氯化银,选项D不正确,答案选C。
4.47×10-5mol/L,所以首先析出的沉淀是氯化银,选项D不正确,答案选C。

科目:高中化学 来源:不详 题型:单选题
| A.相同浓度的两溶液中c(H+)相同 |
| B.100mL0.1mol/L的两溶液能中和等物质的量的氢氧化钠 |
| C.pH=3的两溶液都稀释10倍,盐酸的pH大于醋酸的PH |
| D.两溶液中分别加人少量对应的钠盐,c(H+)均明显减小 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| 温度(℃) | 10 | 20 | 30 | 50 | 70 | 80 | 100 |
| pH | 8.3 | 8.4 | 8.5 | 8.9 | 9.4 | 9.6 | 10.1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.已知0.1 mol·L-1的醋酸溶液中存在电离平衡:CH3COOH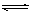 CH3COO-+H+,加少量烧碱溶液可使溶液中 CH3COO-+H+,加少量烧碱溶液可使溶液中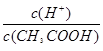 值增大。 值增大。 |
B.25℃时,向水中加入少量固体CH3COONa,水的电离平衡:H2O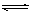 H++OH-逆向移动,c(H+)降低 H++OH-逆向移动,c(H+)降低 |
| C.取c(H+)="0.01" mol·L-1的盐酸和醋酸各100 mL,分别稀释2倍后,再分别加入0.03 g锌粉,在相同条件下充分反应,醋酸与锌反应的速率大 |
| D.向硝酸钠溶液中滴加稀盐酸得到的pH=5的混合溶液中:c(Na+)<c(NO3-) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.电离常数(K)越小,表示弱电解质电离能力越弱 |
| B.电离常数(K)与温度无关 |
| C.不同浓度的同一弱电解质,其电离常数(K)不同 |
| D.多元弱酸各步电离常数相互关系为:K1<K2<K3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.白醋中滴入石蕊试液呈红色 | B.白醋具有杀菌消毒作用 |
| C.蛋壳浸泡在白醋中有气体放出 | D.pH试纸显示醋酸的pH为2~3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com