
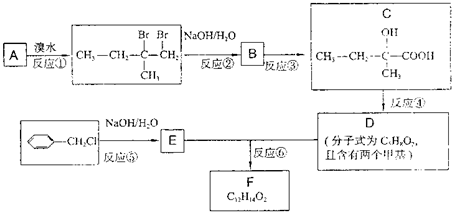
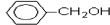
 ����Ӧ��ΪE��Dͨ��������Ӧ����F����F�Ľṹ��ʽΪ
����Ӧ��ΪE��Dͨ��������Ӧ����F����F�Ľṹ��ʽΪ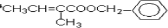 ���ݴ˷������
���ݴ˷������ ����Ӧ��ΪE��Dͨ��������Ӧ����F����F�Ľṹ��ʽΪ
����Ӧ��ΪE��Dͨ��������Ӧ����F����F�Ľṹ��ʽΪ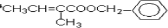 ����1���������Ϸ�����AΪCH2=C��CH3��CH2CH3����H2�����ӳɷ�Ӧ����CH3CH��CH3��CH2CH3������Ϊ2-�����飬�ʴ�Ϊ��2-�����飻
����1���������Ϸ�����AΪCH2=C��CH3��CH2CH3����H2�����ӳɷ�Ӧ����CH3CH��CH3��CH2CH3������Ϊ2-�����飬�ʴ�Ϊ��2-�����飻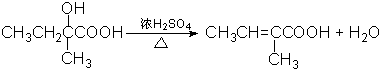 ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
�� ���ڷ����廯�����ͬ���칹��Ϊ
���ڷ����廯�����ͬ���칹��Ϊ ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| 50ml���� | 50ml���� | 50ml���� | |
| M������ | 9.2g | 15.7g | 27.6g |
| V����״���� | 2.24L | 3.36L | 3.36L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ���뷽��ʽ | ���볣�� |
| H2C2O4?H++HC2O4- | K1=5.4��10-2 |
| HC2O4-?H++C2O42- | K2=5.4��10-5 |
| NH3?H2O?NH4++OH- | K=1.8��10-5 |
| Na2CO3 |
| ���� |
| 75%�ƾ� |
| ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
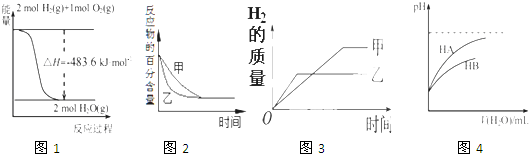
| A��ͼ1��ʾH2��O2������Ӧ�����е������仯����H2��ȼ����Ϊ241.8 kJ?mol-1 |
| B��ͼ2��ʾѹǿ�Կ��淴Ӧ2A��g��+2 B��g��?3C��g��+D��s����Ӱ�죬�ҵ�ѹǿ�ȼ�ѹǿ�� |
| C��ͼ3��ʾ�������ļء��Ʒֱ�������ˮ��Ӧ�����Ϊ�� |
| D��ͼ4��ʾ�����£�ϡ��HA��HB�������ϡ��Һʱ����ҺpH���ˮ���ı仯������ͬ������NaA��Һ��pH����ͬŨ�ȵ�NaB��Һ��pH |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
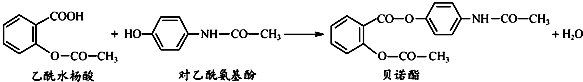
| A������ˮ����Ͷ����������Ӿ�����NaHCO3 ��Һ��Ӧ |
| B������FeCl3 ��Һ��������ˮ����ͱ�ŵ�� |
| C����ŵ����������2�ֺ��������� |
| D����ŵ��������NaOH ��Һ���ȣ���������ˮ�����ƺͶ������������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| A����A����ͬ������ͬ���칹��ֻ��2�� |
| B��A��һ�������¿���4 mol H2�����ӳɷ�Ӧ |
| C��A����������������һ�������²��ܷ���ˮ�ⷴӦ |
| D����������A���ӽṹ�������л���ֻ��1�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�������к������ۡ��������̵� |
| B����ש�������չ����и�����̿�ڣ���ש���������˺�ɫ����Ⱦ�� |
| C�������к��е�ͭԪ�ؾ�����ͬ�������գ��ֱ������˺�ɫCuO�ͺ�ɫCu��Cu2O |
| D�������к��е���Ԫ�ؾ�����ͬ�������գ��ֱ������˺�ɫFe304��FeO�ͺ�ɫFe2O3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��t��ʱ��AgBr��ˮ�еij����ܽ�ƽ��������ͼ��ʾ����֪t��ʱAgCl��Ksp=4��10-10������˵������ȷ���ǣ�������
��t��ʱ��AgBr��ˮ�еij����ܽ�ƽ��������ͼ��ʾ����֪t��ʱAgCl��Ksp=4��10-10������˵������ȷ���ǣ�������| A����ͼ��a���Ӧ����AgBr�IJ�������Һ |
| B����t��ʱ��Ksp��AgBr��=4.9��10-13 |
| C����t��ʱ��AgCl��s��+Br-��aq��?AgBr��s��+Cl-��aq����ƽ�ⳣ��K��816 |
| D����AgBr�ı�����Һ�м���NaBr���壬��ʹ��Һ��b�㵽��c�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��ʹ���ȱ�����Һ��K+��Na+��SO42-��CO32- |
| B��pH=7����Һ�У�Fe3+��K+��SO42-��Br- |
| C��c��H+��/c ��OH-���T104����Һ��K+��Ba2+��NO3-��Cl- |
| D��ˮ�������c��H+���T1.0��10-13 mol?L-1����Һ�У�SO42-��K+��Cl-��Fe3+ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com