
| A. | v(A)=0.02 mol/(L•s) | B. | v(B)=0.6 mol/(L•min) | ||
| C. | v(C)=0.5 mol/(L•min) | D. | v(D)=0.01 mol/(L•s) |
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 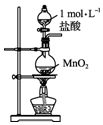 用装置甲制取氯气 | B. | 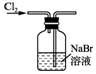 用装置乙氧化溴离子 | ||
| C. | 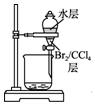 用装置丙分离出溴的CCl4溶液 | D. | 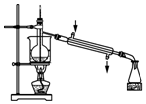 用装置丁获得单质溴 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
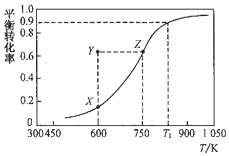 甲醇脱氢可制取甲醛:CH3OH(g)?HCHO(g)+H2(g),甲醇的平衡转化率随温度变化的曲线如图所示(已知反应在IL 的密闭容器中进行).下列有关说法正确的是( )
甲醇脱氢可制取甲醛:CH3OH(g)?HCHO(g)+H2(g),甲醇的平衡转化率随温度变化的曲线如图所示(已知反应在IL 的密闭容器中进行).下列有关说法正确的是( )| A. | 平衡常数:K600K>K750K | |
| B. | 从Y到Z点可通过增大压强实现 | |
| C. | 在Tl点K时,该反应的平衡常数为8.1 | |
| D. | 若工业上利用此反应进行生产,为了提高经济效益将反应温度升高至1050K以上 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 少量SO2 通入漂白粉溶液中:SO2+H2O+Ca2++3C1O-═CaSO4↓+2HC1O+Cl- | |
| B. | 石灰水与过量小苏打溶液反应:Ca2++OH-+HCO3-═CaCO3↓+H2O | |
| C. | FeCl2溶液中通入 C12:Fe2++Cl2═Fe3++2Cl- | |
| D. | NaAlO2 溶液中通入过量CO2:AlO2-+4CO2+2H2O═A13++4HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 弱酸 | 电离常数 | 弱酸 | 电离常数 |
| H2CO3 | Ka1=4.4×10-7 | H2C2O4 | Ka1=5.4×10-2 |
| Ka2=4.7×10-11 | Ka2=5.4×10-5 |
| A. | 2 | B. | 4 | C. | 6 | D. | 8 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属钠着火时立即用沙子盖灭 | |
| B. | 制取有毒气体时需在通风橱中进行 | |
| C. | 将过期的化学药品直接倒入下水道 | |
| D. | 给试管中液体加热时试管口要避开人 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com