
【题目】汾酒是山西特产,有着4000年左右的历史,被誉为“最早国酒”。酿酒的工艺流程如下:

请回答下列问题:
(1)上述流程中用于混合物分离的操作名称是___。
(2)“粉碎”的目的是___,“发酵”过程中发生的反应的类型属于:___。
(3)如图是实验室进行蒸馏操作的装置图,仪器a的名称是___,冷凝水的进水口是___(填字母),为保证实验的安全,蒸馏操作中需注意的一项操作是____。

【答案】过滤、蒸馏 增大反应物的接触面积,加快反应 氧化还原反应 圆底烧瓶 c 在圆底烧瓶中加入碎瓷片
【解析】
(1)根据流程图,结合常见的用于混合物分离的操作分析判断;
(2)将麦芽“粉碎”可以增大反应物的接触面积;“发酵”过程中发生的是葡萄糖转化为了乙醇和二氧化碳,据此分析判断反应类型;
(3)根据蒸馏操作注意事项分析解答。
(1)根据流程图,可以用于混合物分离的操作有过滤和蒸馏,故答案为:过滤、蒸馏;
(2)将麦芽“粉碎”可以增大反应物的接触面积,使反应速率加快;“发酵”过程中葡萄糖转化为了乙醇和二氧化碳,存在元素化合价的变化,属于氧化还原反应,故答案为:增大反应物的接触面积,加快反应;氧化还原反应;
(3)根据蒸馏操作的装置图,仪器a是圆底烧瓶,冷凝水应该下进上出,进水口是c,为保证实验的安全,防止蒸馏时液体暴沸,需要在圆底烧瓶中加入碎瓷片,故答案为:圆底烧瓶;c;在圆底烧瓶中加入碎瓷片。


 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案科目:高中化学 来源: 题型:
【题目】设NA代表阿伏加德罗常数的值,下列说法正确的是( )
A.1 molNa在空气中完全燃烧,转移的电子数为2NA
B.常温下,2.7g铝与足量NaOH溶液反应,消耗0.1NA个水分子
C.0.1molFe与足量水蒸气反应生成H2的分子数为0.1NA
D.11.2LCl2含有的原子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一个容积为V的密闭容器,中间有一可自由滑动的隔板(厚度不计)将容器分成两部分,当左边充入1molN2,右边充入一定量的CO时,隔板处于如图位置(保持温度不变),下列说法正确的是( )

A.右边与左边分子数之比为4:1
B.右侧CO的质量为5.6g
C.右侧气体密度是相同条件下氢气密度的14倍
D.若改变右边CO的充入量而使隔板处于容器正中间,保持温度不变,则应充入0.2molCO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中,对可逆反应A+3B![]() 2C(g),平衡时C的体积分数与温度和压强的关系如图所示,下列判断错误的是
2C(g),平衡时C的体积分数与温度和压强的关系如图所示,下列判断错误的是

A.若正反应方向Q<0,则T1>T2
B.A可能为气体
C.压强增大时,混合气体的平均相对分子质量增大
D.B不一定为气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列说法正确的是()
A.2g氢气中的原子数为NA
B.1mol/LCaCl2溶液中Cl- 数为2NA
C.标准状况下22.4LCO2中原子数为3NA
D.2L2mol/LC2H5OH溶液中分子数为4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某酯的合成路线如下图所示

(1)反应Ⅰ反应类型为___________________; D中含氧官能团为_____________写名称)。
(2)反应Ⅱ的反应条件为:_________________。
(3)C→D的化学反应方程式为________________________________________。
(4)写出一种满足下列条件的E的同分异构体的结构简式为__________________________。
①能发生银镜反应 ②含苯环且苯环上一溴代物两种 ③不能与钠反应
(5)写出B合成![]() 的合成路线。合成路线常用的表示方式为:_______________
的合成路线。合成路线常用的表示方式为:_______________
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】制烧碱所用的盐水需进行两次的精制。
(1)第一次精制主要是用沉淀法除去粗盐水中Ca2+、Mg2+、SO42-等离子,过程如下:
I.向粗盐水中加入过量X,过滤。
II.向所得滤液中加入过量Y,过滤。
III.滤液用盐酸调节pH,获得一次精制盐水。
请回答下列问题:
①X是__________。
②Y是___________,加入Y的主要目的_______________。
③经检测,II中过滤所得的沉淀中还含有Mg2(OH)2CO3,生成该沉淀的离子方程式是________。
(2)第二次精制要除去一次精制盐水中微量的IO3-、NH4+、Ca2+、Mg2+,流程示意图如下:

①IV中除去的离子是____________(填化学式),判断的理由是_______。
②V中得到的溶液颜色呈棕黄色,由此说明Na2S2O3将IO3-还原为______(填化学式),同时Na2S2O3被氧化为SO42-。此反应中体现了Na2S2O3的_________性。假设Na2S2O3已完全反应,则证明盐水b中含有SO42-的方法是__________,观察到的现象是____________。
③有同学提出,该流程中的过程IV可直接加入NaOH溶液除去NH4+和Mg2+,你认为是否可行?_______(填“是”或“否”,提示NH3极易溶于水),理由是_______(答一点)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇是重要的化工原料,又可作为燃料。利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主反应如下:
①CO(g)+2H2(g)![]() CH3OH(g)ΔH1
CH3OH(g)ΔH1
②CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)ΔH2
CH3OH(g)+H2O(g)ΔH2
③CO2(g)+H2(g)![]() CO(g)+H2O(g)ΔH3
CO(g)+H2O(g)ΔH3
回答下列问题:已知反应①中的相关的化学键键能数据如表:
化学键 | H—H | C—O |
| H—O | C—H |
E/(kJ·mol-1) | 436 | 343 | 1076 | 465 | 413 |
(1)由此计算ΔH1=__kJ·mol-1,已知ΔH2=-58kJ·mol-1,则ΔH3=__kJ·mol-1。
(2)在一定条件下,向2L恒容密闭容器中冲入1molCO2和3molH2发生反应②,5min时测得生成了0.4molH2O,求5min的反应速率v(H2)=__,写出一种能加快反应速率的措施___
(3)甲醇是电动汽车的理想燃料,工作原理如图所示:
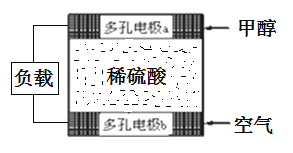
多孔电极b为燃料电池的__极(填“正”或“负”),多孔电极a发生的电极反应式为:____
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在给定条件下,下列选项中所示的物质间转化均能实现的是
A. NaOH(aq) ![]() Cu(OH)2悬浊液
Cu(OH)2悬浊液![]() Cu2O
Cu2O
B. NH3![]() NO
NO![]() HNO3
HNO3
C. MgC12(aq)![]() 无水MgC12
无水MgC12![]() Mg
Mg
D. CaCl2(aq)![]() CaCO3
CaCO3![]() CaO
CaO
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com