
【题目】【化学──物质结构与性质】(15分)某钙钛型复合氧化物(如图),以A原子为晶胞的顶点,A位可以是Ca、Sr、Ba或Pb,当B位是V、Cr、Mn、Fe时,这种化合物的电阻率在有外磁场作用时较之无外磁场作用时存在巨大变化(巨磁电阻效应)。

(1)用A、B、O表示这类特殊晶体的化学式 。在图中,与A原子配位的氧原子数目为 。
(2)基态Cr原子的核外电子排布式为 ,其中电子的运动状态有 种。
(3)某些钙钛型复合氧化物能够催化NO直接分解为N2和O2,N和O的基态原子中,未成对的电子数目比为 。
(4)下表是几种碳酸盐的热分解温度和阳离子半径
碳酸盐 | CaCO3 | SrCO3 | BaCO3 |
热分解温度/℃ | 900 | 1172 | 1360 |
阳离子半径/pm | 99 | 112 | 135 |
请解释碳酸钙热分解温度最低的原因:___________________________________。
(5)用晶体的X射线衍射法可以测得阿伏伽德罗常数。对金属钙的测定得到以下结果:晶胞为面心立方最密堆积,边长为558pm。又知钙的密度为1.54g·cm-3,则1cm3钙晶体中含有 个晶胞,阿伏伽德罗常数为 (列式计算)。
【答案】(15分)
(1)ABO3(2分),12 (2分)
(2)1s22s22p63s23p63d54s1(2分), 24(2分)
(3)3∶2(1分)
(4)碳酸盐的热分解是由于晶体中的阳离子结合碳酸根中的氧离子,使碳酸根分解为二氧化碳分子的结果。钙离子由于半径小和氧离子结合更为容易,氧化钙晶格能大,所以碳酸钙分解温度低。(2分)
(5)5.76×1021(2分),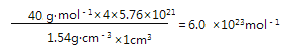 (2分)
(2分)
【解析】试题分析:(1)1个晶胞中含有A原子1个,B原子1个,O原子3个,该晶体的化学式ABO3。在图中,与A原子配位的氧原子处于面对角线的中点,距离相等的共有12个。
(2)Cr是24号元素,基态Cr原子的核外电子排布式为1s22s22p63s23p63d54s1,每个电子的运动状态都不一样。
(3)N的核外电子排布式为1s22s22p3,未成对的电子数为3,,O的核外电子排布式为1s22s22p4,未成对的电子数为2;
(4)碳酸盐的热分解是由于晶体中的阳离子结合碳酸根中的氧离子,使碳酸根分解为二氧化碳分子的结果。钙离子由于半径小和氧离子结合更为容易,氧化钙晶格能大,所以碳酸钙分解温度低。
(5)晶胞的边长是558pm,所以1个晶胞的体积是(5.58×10—8cm)3=1.74×10—22cm3。因此1cm3钙晶体中含有的晶胞数目=![]() 个=5.76×1021个,根据密度看着1cm3钙晶体的质量=1.54g·cm-3×1cm3,由于钙晶胞中含有的钙原子数是8×1/8+6×1/2=4,则1cm3晶体中含有钙原子的数目为5.76×1021×4,阿伏伽德罗常数个钙原子的质量为40g,因此NA=
个=5.76×1021个,根据密度看着1cm3钙晶体的质量=1.54g·cm-3×1cm3,由于钙晶胞中含有的钙原子数是8×1/8+6×1/2=4,则1cm3晶体中含有钙原子的数目为5.76×1021×4,阿伏伽德罗常数个钙原子的质量为40g,因此NA=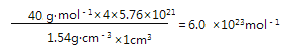 。
。


 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案科目:高中化学 来源: 题型:
【题目】某研究性学习小组拟从盐卤液(含Na+、Cl-、Mg2+、Ca2+、I-、SO42-),来制取较纯净的氯化钠晶体及单质碘(I2),他们设计了如下实验:
第一步:提取碘
(1)在盐卤液中通入Cl2可使I-氧化为碘单质(I2),反应的离子方程式为_____________________
(2)要将此反应后的溶液中的碘单质分离出来,先加入一种试剂可以得到一种紫红色液体,这种试剂是___________(填字母编号)
A.盐酸 B.四氯化碳 C.氢氧化钠溶液 D.酒精
该分离方法称为___________。
(3)要从紫红色液体中再分离出单质碘,还需要采取下图的分离操作,该分离方法称为___________。(填分离操作名称)
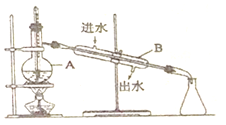
①指出图中的两处明显错误_________________;___________________。
②写出仪器名称:A_____________,B________________。
第二步:粗盐提纯
(4)提取碘后,溶液中主要含有Na+、Cl-、Ca2+、Mg2+、SO42-,为了得到纯净的NaCl,然后在下列操作中选取必要的步骤和正确的操作顺序______________(有多少选多少)
①过滤②加过量NaOH溶液③加适量盐酸④加过量Na2CO3溶液⑤加过量BaCl2溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图所示是验证氯气性质的微型实验,a、b、d、e是浸有相关溶液的滤纸。向KMnO4晶体滴加一滴浓盐酸后,立即用另一培养皿扣在上面。已知:2KMnO4+16HCl―→2KCl+5Cl2↑+2MnCl2+8H2O

对实验现象的“解释或结论”正确的是 ( )
选项 | 实验现象 | 解释或结论 |
A | a处变蓝,b处变红棕色 | 氧化性:Cl2>Br2>I2 |
B | c处先变红,后褪色 | 氯气与水生成了酸性物质 |
C | d处立即褪色 | 氯气与水生成了漂白性物质 |
D | e处变红色 | 还原性:Fe2+>Cl- |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式正硫的是
A. 硫化钠的水解反应:S2-+H3O+![]() HS-+H2O
HS-+H2O
B. 用铜做阳极电解氯化铜溶液:Cu2++2Cl-![]() Cu+Cl2↑
Cu+Cl2↑
C. 在硫酸亚铁溶液中通入氧气:4Fe2++O2+4H+=4Fe3++2H2O
D. 泡沫灭火器工作时化学反应:2Al3++3CO32-+6H2O=Al(OH)3↓+3CO2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在T ℃时,将a g NH3完全溶于水,得到V mL溶液,假设该溶液的密度为ρ g·cm-3,溶质的质量分数为w,物质的量浓度为c mol·L-1,则下列选项不正确的是( )
A. 溶质的质量分数为w=![]()
B. 用水稀释该溶液,OH-的物质的量增加
C. 该溶液中共有6种微粒
D. 上述溶液中再加入V mL水后,所得溶液溶质的质量分数大于0.5w
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室可以用高锰酸钾和浓盐酸反应制取氯气,反应的化学方程式如下:
2KMnO4+16HCl (浓)= 2KCl+2MnCl2+5Cl2↑+8H2O
(1)用双线桥法标出电子转移的方向和数目______________________。
(2)该反应中氧化剂与氧化产物物质的量之比是_____________。
(3)由该反应判断,KMnO4的氧化性比Cl2的氧化性(选填“强”或“弱”)_______________。
(4)如反应中转移了2mol电子,则产生的Cl2在标准状况下体积为___________L。
(5)某同学欲用KMnO4固体配制100mL0.5mol/L的溶液。回答下列问题:
①配制KMnO4溶液时需用的主要仪器有托盘天平、药匙、烧杯、玻璃棒、量筒、_________,________。
②下列对容量瓶及其使用方法的描述中正确的是(请填序号)________。
A.容量瓶上标有容积、温度和刻线
B.容量瓶用蒸馏水洗净后,必须50℃烘干
C.配制溶液时,把量好的KMnO4固体小心放入容量瓶中,加入蒸馏水到接近刻度线1~2cm处,改用胶头滴管加蒸馏水至刻度线
D.使用前要检査容量瓶是否漏水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数的值,下列说法正确的是
A. 27g铝中加入lmol/L的NaOH溶液,转移电子数是3NA
B. 56gN2与CO混合物中原子总数是4NA
C. 标准状况下,44.8LNO与22.4LO2反应后的分子数是2NA
D. 常温下,lLpH=1的H2SO4溶液中的H+为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组将一定浓度Na2CO3溶液滴入CuSO4溶液中得到蓝色沉淀。
甲同学认为两者反应生成只有CuCO3一种沉淀;乙同学认为这两者相互促进水解反应,生成Cu(OH)2一种沉淀;丙同学认为生成CuCO3和Cu(OH)2两种沉淀。(查阅资料知:CuCO3和Cu(OH)2均不带结晶水)请你一起参与实验探究并回答下列问题:
Ⅰ.在探究沉淀物成分前,须将沉淀从溶液中分离并净化。具体操作为①_______________、
②_______________、
③________________。
II.请用下图所示装置,选择必要的试剂,定性探究生成物的成分。

⑴各装置连接顺序为_____ →_____ → _____ 。
⑵装置C中装有试剂的名称是_________________。
⑶能证明生成物中有CuCO3的实验现象是________________________。
Ⅲ.若蓝色沉淀中CuCO3和Cu(OH)2两者都有,可通过下列所示装置的连接,进行定量分析来测定其中CuCO3组成:
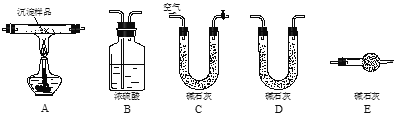
⑴ 实验开始时先要将空气通过碱石灰的目的是____________________;
实验中持续通入过量空气的作用是______________。
⑵若沉淀样品的质量为m克,装置B质量增加了n克,则沉淀中CuCO3的质量分数为:_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关阿伏加德罗常数(NA)的说法错误的是( )
A. 25℃、101KPa条件下22克CO2所含的原子数目为1.5NA
B. 标准状况下0.1molH2O含有的分子数目为0.1NA
C. 0℃、101KPa条件下03NA氧气的体积是6.72升
D. 58.5克NaCl固体中含有的离子数目为NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com