
����Ŀ��ij����ˮ�к�5.00��10-3mol��L-1��![]() ���䶾�Խϴ�ij�о���ѧϰС��Ϊ�˱��Ϊ��������ˮ�����õ����Բ���
���䶾�Խϴ�ij�о���ѧϰС��Ϊ�˱��Ϊ��������ˮ�����õ����Բ���![]() ��
��![]() �Ļ��ϼ�����Ϊ+3��+2�������������ʵ�����̣�
�Ļ��ϼ�����Ϊ+3��+2�������������ʵ�����̣�
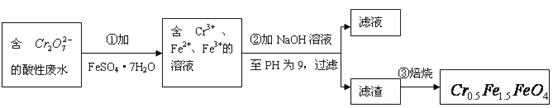
��1����������Ӧ�����ӷ���ʽ��_________________________________________________��
��2������������pH��ֽ�ⶨ��ҺpH�IJ����ǣ�
______________________________________________________________________________��
��3�����������˵õ�����������Ҫ�ɷֳ�Cr��OH��3�⣬����______________________��
��4����ʹ1L�÷�ˮ�е�![]() ��ȫת��Ϊ
��ȫת��Ϊ![]() ����������Ҫ����__________g FeSO4��7H2O��
����������Ҫ����__________g FeSO4��7H2O��
���𰸡�Cr2O72-+ 6Fe2��+ 14H��![]() 2Cr3+ + 6Fe3��+ 7H2O ��һС��pH��ֽ���ڱ������ϣ��ò�����պȡ��������Һ������pH��ֽ�ϣ��������ɫ������ Fe(OH)3��Fe(OH)2 13.9
2Cr3+ + 6Fe3��+ 7H2O ��һС��pH��ֽ���ڱ������ϣ��ò�����պȡ��������Һ������pH��ֽ�ϣ��������ɫ������ Fe(OH)3��Fe(OH)2 13.9
��������
(1)Cr2O72-�н�ǿ�����ԣ�FeSO47H2O��Fe2+��һ���Ļ�ԭ�ԣ������Խ����з���������ԭ��Ӧ����ʵ�����̿�֪���ڢٲ���Ӧ��Cr2O72-�����������½�Fe2+����ΪFe3+����������ԭΪCr3+�������غ�Ԫ���غ㼰����������֪����Ӧ��ˮ���ɣ���Ӧ���ӷ���ʽΪCr2O72-+14H++6Fe2+=2Cr3++6Fe3++7H2O���ʴ�Ϊ��Cr2O72-+14H++6Fe2+=2Cr3++6Fe3++7H2O��
(2)��һС��pH��ֽ���ڱ������ϣ��ò�����պȡ��������Һ������pH��ֽ�ϣ��ʴ�Ϊ����һС��pH��ֽ���ڱ������ϣ��ò�����պȡ��������Һ������pH��ֽ�ϣ��������ɫ�����գ�
(3)�������ͼ�ɵã�Fe2+��������NaOHʱ������Cr(OH)3��Fe(OH)3��Fe(OH)2���ֳ�����ʴ�Ϊ��Fe(OH)3��Fe(OH)2��
(4)1 L��ˮ�к�n(Cr2O72-)=5.00��10-3 mol������Crԭ�ӡ�Feԭ���غ㣬�ɵã�Cr2O72-������4Cr0.5Fe1.5FeO4������10FeSO47H2O������������n(FeSO47H2O)=10n(Cr2O72-)=5.00��10-3 mol��10=0.05 mol������m(FeSO47H2O)=0.05 mol��278 g/mol=13.9 g���ʴ�Ϊ��13.9g��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij���л�������ģ����ͼ(ͼ�й���ʾ������˫��������)�����ڸ��л����˵����ȷ���ǡ�
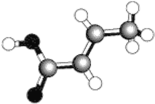
A.�����ģ�ͱ�ʾ�Ļ�ѧʽΪC6H6
B.���л���ֻ�ܷ���ȡ����Ӧ�ͼӳɷ�Ӧ���ַ�Ӧ
C.���л����ʹ��ˮ��ɫ,������ʹ���Ը��������Һ��ɫ
D.���л��ﲻ�������ͬϵ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����л�ѧ�������ر�������ȷ����
A. ��H+(aq) +OH- (aq)==H2O(l) ��H=-akJ��mol-1����1molNaOH������������ϡ���ᷴӦ���ų�������ΪakJ
B. ��CuSO4��5H2O(s)==CuSO4(s)+5H2O(1)��H=+bkJ��mol-1����1molCuSO4(s)����ˮʱ���ų�������ΪbkJ
C. ��������ȼ����Ϊc kJ��mol-1����ˮ�����Ȼ�ѧ����ʽΪ2H2O (l)==2H2(g)+O2(g) ��H=+c kJ��mol-1
D. ��N2(g)+3H2(g)![]() 2NH3(g) ��H=-d kJ��mol-1������ij������ͨ��1molN2��3molH2��ַ�Ӧ�ų�������С��dkJ
2NH3(g) ��H=-d kJ��mol-1������ij������ͨ��1molN2��3molH2��ַ�Ӧ�ų�������С��dkJ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijѧ������֪���ʵ���Ũ�ȵ��������ⶨδ֪���ʵ���Ũ�ȵ�NaOH��Һʱ��ѡ�������ָʾ��������д���пհס�
��1���ñ�������ζ������NaOH��Һʱ����������ʽ�ζ��ܵĻ���������ҡ����ƿ���۾�ע��____��ֱ�������һ���������Һ��______ɫ��Ϊ____ɫ����____Ϊֹ��
��2�����в����п���ʹ����NaOH��Һ��Ũ����ֵƫ�͵���__________��
A.��ʽ�ζ���δ�ñ�������ϴ��ֱ��ע�������
B.�ζ�ǰʢ��NaOH��Һ����ƿ������ˮϴ����û�и���
C.��ʽ�ζ����ڵζ�ǰ�����ݣ��ζ���������ʧ
D.��ȡ�������ʱ����ʼ���Ӷ������ζ�����ʱ���Ӷ���
��3�����ζ���ʼ�ͽ���ʱ����ʽ�ζ����е�Һ����ͼ��ʾ������ʼ����Ϊ_____mL������������Һ�����Ϊ_____mL��

��4��ijѧ������3��ʵ��ֱ��¼�й����������
�ζ� ���� | ����NaOH��Һ�����/mL | 0.1000mol��L��1��������/mL | ||
�ζ�ǰ���� | �ζ������ | ��Һ���/mL | ||
��һ�� | 25.00 | 0.00 | 25.11 | 25.11 |
�ڶ��� | 25.00 | 1.56 | 30.30 | 28.74 |
������ | 25.00 | 0.22 | 25.31 | 25.09 |
���ݱ���������ʽ�����NaOH��Һ�����ʵ���Ũ��_____��������λС������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NaClO2��Ư��������Ư�۵�4��5���� NaClO2�㷺������ֽ��ҵ����ˮ�����ȡ���ҵ������NaClO2�Ĺ����������£�

(1)ClO2�������еķ�ӦΪ��2NaClO3��SO2��H2SO4===2ClO2��2NaHSO4��ʵ�ʹ�ҵ�����У�������ơ�Ũ�������ԭ���е�SO2����ԭ��Ϊ_____________(�û�ѧ����ʽ��ʾ)��
(2)��Ӧ��������ClO2��������ͨ��һ����������Ŀ�ģ�________________________��
(3)������������NaClO2�����ӷ�Ӧ����ʽΪ___________________________________��
(4)ij��ѧ��ȤС��������ͼ��ʾװ���Ʊ�SO2��̽��SO2��Na2O2�ķ�Ӧ��

��ʢ��ŨH2SO4��������Ϊ_____��C����Һ��������____________��
��D���ռ����������ʹ�������ľ����ȼ��B�з����ķ�Ӧ����Ϊ__________��Na2O2��SO2=Na2SO4��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������Ҫ�ɷ���![]() ����
����![]() ��
��![]() ��MgO�����ʣ�����ȡ���ֹ���Ʒ���������£�
��MgO�����ʣ�����ȡ���ֹ���Ʒ���������£�

��ش��������⣺
��1�����̼������������Al3+�ķ���ʽΪ_________.
��2�������Ҽ����ռ������SiO32-�����ӷ���ʽΪ________.
��3����֤��ҺB��![]() ����ȡ������Һ������________�����Լ����ƣ���
����ȡ������Һ������________�����Լ����ƣ���
��4����ҺE��K�����ʵ���Ҫ�ɷ���________(�ѧʽ)��д������Һ��һ����;________
��5����֪298Kʱ��![]() ���ݶȻ�����
���ݶȻ�����![]() =5.6��
=5.6��![]() ,ȡ��������ҺB,����һ�������ռ�ﵽ������Һƽ�⣬���PH=13.00������¶��²�������Һ�е�
,ȡ��������ҺB,����һ�������ռ�ﵽ������Һƽ�⣬���PH=13.00������¶��²�������Һ�е�![]() =_______.
=_______.
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����е�Ũ�ȵ�������Һ�������ᣬ�����ӣ��������ƣ���̼�ᣬ��̼���ƣ���̼�����ơ�����ҺpH��С����������ȷ����
![]()
![]() A. �ܢ٢ڢݢޢ� B. �ܢ٢ڢޢݢ�
A. �ܢ٢ڢݢޢ� B. �ܢ٢ڢޢݢ�
![]()
![]() C. �٢ܢڢޢۢ� D. �٢ܢڢۢޢ�
C. �٢ܢڢޢۢ� D. �٢ܢڢۢޢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����25��ʱ���ܱ�������X��Y��Z��������ij�ʼŨ�Ⱥ�ƽ��Ũ�����������˵���������ǣ��� ��
���� | X | Y | Z |
��ʼŨ��/ | 0.1 | 0.2 | 0 |
ƽ��Ũ��/ | 0.05 | 0.05 | 0.1 |
A.��Ӧ�ﵽƽ��ʱ��X��ת����Ϊ50��
B.��Ӧ�ɱ�ʾΪX+3Y![]() 2Z����ƽ�ⳣ��Ϊ1600
2Z����ƽ�ⳣ��Ϊ1600
C.�ı��¶ȿ��Ըı�˷�Ӧ��ƽ�ⳣ��
D.��ѹʹƽ��������Z�ķ����ƶ���ƽ�ⳣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ij�ܱ������м��� 0.3 mol A��0.1 mol C ��һ������ B �������壬 һ�������·������·�Ӧ�� 3A(g) ![]() B(g)��2C(g)�������ʵ�Ũ����ʱ��仯��ͼ��ʾ[t0��t1 �ε� c(B)�仯δ����]������˵������ȷ����( )
B(g)��2C(g)�������ʵ�Ũ����ʱ��仯��ͼ��ʾ[t0��t1 �ε� c(B)�仯δ����]������˵������ȷ����( )

A. �� t1��15 s������ A ��Ũ�ȱ仯��ʾ t0��t1�ε�ƽ����Ӧ����Ϊ 0.004 mol��L��1��s��1
B. t1ʱ�÷�Ӧ�ﵽƽ�⣬ A ��ת����Ϊ 60%
C. ���������ݻ�Ϊ2 L��B����ʼ�����ʵ���Ϊ 0.02 mol
D. t0��t1 �Σ� �˹����������������Ƚ�������Ϊ a kJ���÷�Ӧ���Ȼ�ѧ����ʽΪ 3A(g)![]() B(g)��2C(g) ��H����50a kJ��mol��1
B(g)��2C(g) ��H����50a kJ��mol��1
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com