
实验操作 | 时间/s | 电子天平读数/g |
烧杯+水 |
| 370.000 |
烧杯+水+样品 | 0 | 377.640 |
30 | 376.920 | |
60 | 376.400 | |
90 | 376.200 | |
120 | 376.200 |
试计算样品中的质量分数,并估算最后溶液的pH。?

图2-3
w (Na2O2)=91.9% pH=14
解析:由表中数据可知,所取样品的质量为377.640 g-370.000 g=7.640 g,样品投入水中,放出氧气,随着反应的进行,电子天平的读数逐渐减少,至90 s开始读数不变,说明此时过氧化钠已反应完全,此时的质量减少量即为反应生成的氧气的质量377.640 g-376.200 g=1.440 g。设样品中Na2O2的质量为 x,生成的NaOH的物质的量为y,则有
2Na2O2+2H2O![]() 4NaOH+O2↑?
4NaOH+O2↑?
x?? y?
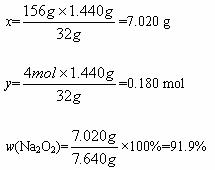
m(Na2O)=
设与水反应生成的NaOH的物质的量为z,则有?
Na2O+H2O![]() 2NaOH?
2NaOH?
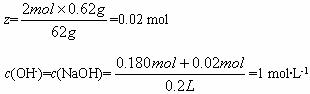
c(H+)=10-14mol·L-1 pH=14。


 口算能手系列答案
口算能手系列答案科目:高中化学 来源: 题型:
| ||
| ||
| 11200 |
| V |
| 11200 |
| V |
查看答案和解析>>
科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
物质 | A | B | CO | H2 |
燃烧热/kJ·mol-1 | 725 | 5518 | 283 | 286 |
A、B按不同比例混合的燃料91.
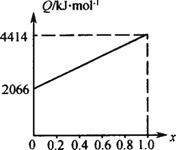
图9-8
(1)A、B的相对分子质量为A____________,B____________。
(2)等物质的量的A、B相混合的燃料
N(C):N(H):N(O)=____________,A的分子式为____________,B的分子式为____________。
(3)1mol由A、B等物质的量混合而成的燃料在一定量的氧气中燃烧,放出2908kJ热量,则反应中生成CO____________mol。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com