
(14分)电化学原理在现代生产生活中有着重要应用。
⑴燃料电池是目前发展势头强劲的优秀绿色环保电池。某新型氢氧燃料电池以H2为燃料,O2为氧化剂,H2SO4溶液为电解液),写出该电池的总反应方程式: 。
⑵铝电池性能优越,Al—AgO电池可用作水下动力电源,该电池反应的原理为:
Al+3AgO+2NaOH=2NaAlO2+3Ag+H2O。
①该电池反应的负极电极反应式 。
②图中隔膜为阴离子交换膜,溶液中OH-通过向 极移动(选填“正”或“负”)。
用Al—AgO电池作为电源,使用Pt电极电解500mL饱和NaCl溶液,电解一段时间后,恢复至室温,所得溶液pH=13(假设NaCl溶液足量且电解前后体积不变)。
③使用Pt电极电解NaCl溶液的离子方程式 ;
电解过程中放出氢气的体积(标准状况下)为 L。
④若电池的效率为50%,该过程中消耗金属铝的质量为 g。
⑶用电解法制取镁时,若原料氯化镁含有水时,在电解温度下,原料会形成Mg(OH)Cl,并发生电离:Mg(OH)C1 = Mg(OH)+ + C1一。
电解时在阴极表面会产生氧化镁钝化膜,此时阴极的反应式为 。
(14分)
⑴ 2H2+O2=2H2O
⑵Al+4OH--3e-=AlO2-+2H2O 负 2Cl-+2H2O 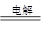 Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-
0.56 0.9
⑶2Mg(OH)++2e-=2MgO+H2↑ (每空2分)
解析试题分析:⑴燃料电池是目前发展势头强劲的优秀绿色环保电池。某新型氢氧燃料电池以H2为燃料,O2为氧化剂,H2SO4溶液为电解液),写出该电池的总反应方程式:2H2+O2=2H2O 。
铝电池性能优越,Al—AgO电池可用作水下动力电源,该电池反应的原理为:
Al+3AgO+2NaOH=2NaAlO2+3Ag+H2O。每消耗1mol铝转移电子是3mol;
①该电池反应的负极是铝,活泼金属能自发和氢氧化钠反应,其电极反应式Al+4OH--3e-=AlO2-+2H2O。
②图中隔膜为阴离子交换膜,溶液中OH-在负极要参与反应,所以向负极移动。
用Al—AgO电池作为电源,使用Pt电极电解500mL饱和NaCl溶液,电解一段时间后,恢复至室温,所得溶液pH=13(假设NaCl溶液足量且电解前后体积不变)。
③使用Pt电极电解NaCl溶液的离子方程式2Cl-+2H2O 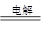 Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-
;500mL饱和NaCl溶液,电解后pH=13,所以产生的氢氧根物质的量浓度是0.1mol/L;其物质的量是0.05mol;由定量关系可知:生成的氢气是0.025mol。所以电解过程中放出氢气的体积V=22.4n=0.56 L(标准状况下)
④若电池的效率为50%,由电子转移守恒可得:电解时转移电子是0.05mol,所以原电池工作时消耗金属铝的质量为0.9g。
⑶用电解法制取镁时,若原料氯化镁含有水时,在电解温度下,原料会形成Mg(OH)Cl,并发生电离:Mg(OH)C1 = Mg(OH)+ + C1一。
电解时在阴极表面会产生氧化镁钝化膜,此时阴极的反应式为2Mg(OH)++2e-=2MgO+H2↑。
考点:燃料电池 电解池 电极反应式
点评:解答此类问题需要注意的是,在原电池和电解池连用时要注意它们之间的唯一联系是电子转移守恒。


 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源: 题型:阅读理解
⑴(5分)随着生活水平的提高,人们越来越关注营养平衡和自身的健康。
①粮食中的淀粉在人体中水解最终转化成 ▲ ,该物质在人体内被氧化,最终生成CO2和H2O,该过程对人体健康的意义是 ▲ 。
②食品添加剂亚硝酸钠的外观像食盐,并有咸味,但亚硝酸钠有很强的毒性。亚硝酸钠属于 ▲ (选填“调味剂”、“防腐剂”或“着色剂”)。
③维生素C也称抗坏血酸。血液中运载氧的血红蛋白中含有Fe2+,人之所以患坏血 病,是因为人体从摄取的食物中吸收的铁主要是Fe3+,Fe3+不能被人体吸收。维生素C的主要摄入途径是 ▲ ,维生素C在抗坏血病方面的作用原理是 ▲ 。
⑵(5分)中国是世界上最早研究和生产合金的国家之一。
①在原子反应堆中得以广泛应用的钠钾合金在常温下呈液态,说明合金的熔点比其成分金属的熔点 ▲ 。
②铜锌合金外观和金(Au)相似,常被误认为黄金。试写出一种鉴别黄铜与黄金的化学方法 ▲ 。铜器表面容易生成一层薄薄的铜绿[主要成份是Cu2(OH)2CO3],请写出铜在潮湿的空气发生电化学腐蚀时的负极反应式 ▲ ;用盐酸可以除去铜器表面的铜绿,该反应的化学方程式为 ▲ 。
③下列对金属制品采取的防护方法不正确的是 ▲ (填序号)。
A.在电线的外面包上一层塑料层
B.在自行车钢圈上镀上一层金属铬
C.在海轮的铁制外壳上焊上铜块
⑶(5分)
①CO2是目前大气中含量最高的一种温室气体,控制和治理CO2是解决温室效应的有效途径。请你写出有利于降低大气中CO2浓度的一项措施 ▲ 。
②水中含有的悬浮颗粒物等杂质,可以加入 ▲ 等混凝剂进行净化处理,利用其溶解后形成的 ▲ 具有吸附作用使水中的悬浮颗粒物沉降。
③最近,国内第一个跨区域日处理垃圾1000吨以上的垃圾焚烧发电厂在江苏如皋投入使用。下面列出了现代生活中的常见垃圾:
A.废纸 B.废电池 C.易拉罐 D.玻璃瓶 E.塑料制品
在焚烧处理前,除废电池外,还有 ▲ (填序号)应剔除并回收,随意丢弃电池造成的主要危害是 ▲ 。
查看答案和解析>>
科目:高中化学 来源:2010—2011学年江苏省扬州中学高二学业水平测试模拟演练化学试卷 题型:填空题
⑴(5分)随着生活水平的提高,人们越来越关注营养平衡和自身的健康。
①粮食中的淀粉在人体中水解最终转化成 ▲ ,该物质在人体内被氧化,最终生成CO2和H2O,该过程对人体健康的意义是 ▲ 。
②食品添加剂亚硝酸钠的外观像食盐,并有咸味,但亚硝酸钠有很强的毒性。亚硝酸钠属于 ▲ (选填“调味剂”、“防腐剂”或“着色剂”)。
③维生素C也称抗坏血酸。血液中运载氧的血红蛋白中含有Fe2+,人之所以患坏血病,是因为人体从摄取的食物中吸收的铁主要是Fe3+,Fe3+不能被人体吸收。维生素C的主要摄入途径是 ▲ ,维生素C在抗坏血病方面的作用原理是 ▲ 。
⑵(5分)中国是世界上最早研究和生产合金的国家之一。
①在原子反应堆中得以广泛应用的钠钾合金在常温下呈液态,说明合金的熔点比其成分金属的熔点 ▲ 。
②铜锌合金外观和金(Au)相似,常被误认为黄金。试写出一种鉴别黄铜与黄金的化学方法 ▲ 。铜器表面容易生成一层薄薄的铜绿[主要成份是Cu2(OH)2CO3],请写出铜在潮湿的空气发生电化学腐蚀时的负极反应式 ▲ ;用盐酸可以除去铜器表面的铜绿,该反应的化学方程式为 ▲ 。
③下列对金属制品采取的防护方法不正确的是 ▲ (填序号)。
A.在电线的外面包上一层塑料层
B.在自行车钢圈上镀上一层金属铬
C.在海轮的铁制外壳上焊上铜块
⑶(5分)
①CO2是目前大气中含量最高的一种温室气体,控制和治理CO2是解决温室效应的有效途径。请你写出有利于降低大气中CO2浓度的一项措施 ▲ 。
②水中含有的悬浮颗粒物等杂质,可以加入 ▲ 等混凝剂进行净化处理,利用其溶解后形成的 ▲ 具有吸附作用使水中的悬浮颗粒物沉降。
③最近,国内第一个跨区域日处理垃圾1000吨以上的垃圾焚烧发电厂在江苏如皋投入使用。下面列出了现代生活中的常见垃圾:
A.废纸 B.废电池 C.易拉罐 D.玻璃瓶 E.塑料制品
在焚烧处理前,除废电池外,还有 ▲ (填序号)应剔除并回收,随意丢弃电池造成的主要危害是 ▲ 。
查看答案和解析>>
科目:高中化学 来源:2014届江苏省南通市海安县高二上学期期末考试化学试卷(解析版) 题型:填空题
(14分)电化学原理在现代生产生活中有着重要应用。
⑴燃料电池是目前发展势头强劲的优秀绿色环保电池。某新型氢氧燃料电池以H2为燃料,O2为氧化剂,H2SO4溶液为电解液),写出该电池的总反应方程式: 。
⑵铝电池性能优越,Al—AgO电池可用作水下动力电源,该电池反应的原理为:
Al+3AgO+2NaOH=2NaAlO2+3Ag+H2O。

①该电池反应的负极电极反应式 。
②图中隔膜为阴离子交换膜,溶液中OH-通过向 极移动(选填“正”或“负”)。
用Al—AgO电池作为电源,使用Pt电极电解500mL饱和NaCl溶液,电解一段时间后,恢复至室温,所得溶液pH=13(假设NaCl溶液足量且电解前后体积不变)。
③使用Pt电极电解NaCl溶液的离子方程式 ;
电解过程中放出氢气的体积(标准状况下)为 L。
④若电池的效率为50%,该过程中消耗金属铝的质量为 g。
⑶用电解法制取镁时,若原料氯化镁含有水时,在电解温度下,原料会形成Mg(OH)Cl,并发生电离:Mg(OH)C1 = Mg(OH)+ + C1一。
电解时在阴极表面会产生氧化镁钝化膜,此时阴极的反应式为 。
查看答案和解析>>
科目:高中化学 来源:2012届江苏省高二学业水平测试模拟演练化学试卷 题型:填空题
⑴(5分)随着生活水平的提高,人们越来越关注营养平衡和自身的健康。
①粮食中的淀粉在人体中水解最终转化成 ▲ ,该物质在人体内被氧化,最终生成CO2和H2O,该过程对人体健康的意义是 ▲ 。
②食品添加剂亚硝酸钠的外观像食盐,并有咸味,但亚硝酸钠有很强的毒性。亚硝酸钠属于 ▲ (选填“调味剂”、“防腐剂”或“着色剂”)。
③维生素C也称抗坏血酸。血液中运载氧的血红蛋白中含有Fe2+,人之所以患坏血 病,是因为人体从摄取的食物中吸收的铁主要是Fe3+,Fe3+不能被人体吸收。维生素C的主要摄入途径是 ▲ ,维生素C在抗坏血病方面的作用原理是 ▲ 。
⑵(5分)中国是世界上最早研究和生产合金的国家之一。
①在原子反应堆中得以广泛应用的钠钾合金在常温下呈液态,说明合金的熔点比其成分金属的熔点 ▲ 。
②铜锌合金外观和金(Au)相似,常被误认为黄金。试写出一种鉴别黄铜与黄金的化学方法 ▲ 。铜器表面容易生成一层薄薄的铜绿[主要成份是Cu2(OH)2CO3],请写出铜在潮湿的空气发生电化学腐蚀时的负极反应式 ▲ ;用盐酸可以除去铜器表面的铜绿,该反应的化学方程式为 ▲ 。
③下列对金属制品采取的防护方法不正确的是 ▲ (填序号)。
A.在电线的外面包上一层塑料层
B.在自行车钢圈上镀上一层金属铬
C.在海轮的铁制外壳上焊上铜块
⑶(5分)
①CO2是目前大气中含量最高的一种温室气体,控制和治理CO2是解决温室效应的有效途径。请你写出有利于降低大气中CO2浓度的一项措施 ▲ 。
②水中含有的悬浮颗粒物等杂质,可以加入 ▲ 等混凝剂进行净化处理,利用其溶解后形成的 ▲ 具有吸附作用使水中的悬浮颗粒物沉降。
③最近,国内第一个跨区域日处理垃圾1000吨以上的垃圾焚烧发电厂在江苏如皋投入使用。下面列出了现代生活中的常见垃圾:
A.废纸 B.废电池 C.易拉罐 D.玻璃瓶 E.塑料制品
在焚烧处理前,除废电池外,还有 ▲ (填序号)应剔除并回收,随意丢弃电池造成的主要危害是 ▲ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com