
常见物质的电离平衡常数如下表,下列离子反应方程式错误的是( )
物质 | H2CO3 | HClO | HAlO2 |
电离常数 (25℃) | Ka1=4.4×10- | Ka=3×10-8 | Ka=6.3×10-13 |
Ka2=4.7×10-11 |
A.NaClO溶液中通入过量CO2:ClO-+CO2+H2O=HClO+HCO3-
B.NaClO溶液中通入少量CO2:2ClO-+CO2+H2O=2HClO+CO32-
C.NaAlO2溶液中加入过量CO2:AlO2-+CO2+2H2O=HCO3-+Al(OH)3↓
D.NaAlO2溶液中通入少量CO2:2AlO2-+CO2+3H2O=CO32-+2Al(OH)3↓
科目:高中化学 来源:2016-2017学年福建省高二上第一次月考化学卷(解析版) 题型:选择题
某学生欲完成2HCl+2Ag═2AgCl+H2↑反应,设计了下列四个实验,你认为可行的实验是
A. B. C. D.
查看答案和解析>>
科目:高中化学 来源:2017届山东省高密市高三上学期10月统考化学试卷(解析版) 题型:选择题
探究铜与浓硝酸的反应,下列装置或操作正确的为

A. 用装置①进行铜和浓硫酸的反应 B. 用装置②收集二氧化硫并吸收尾气
C. 用装置③稀释反应后的混合液 D. 用装置④测定余酸的浓度
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省高二上第一次月考化学试卷(解析版) 题型:填空题
侯氏制碱法曾广泛用于工业制纯碱(Na2CO3),是我国科学家为人类做出的重大贡献.现有25℃时,浓度为0.10mol/LNa2CO3溶液.请回答:
(1)该溶液中c(H+) c(OH﹣) (填“>”、“=”或“<”).
(2)用离子方程式解释(1)的原因: .
(3)下列说法正确的是(填字母) .
a.Na2CO3在水中完全电离
b.c(CO32﹣)+c(HCO3﹣)+c(H2CO3)=0.1mol/L
c.c(Na+)>c(CO32﹣)>c(OH﹣)>c(HCO3﹣)>c(H+)
(4)用石墨作电极电解Na2CO3水溶液时,阴极反应式是 .
(5)Na2CO3溶液中的电荷守恒关系式为:
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省高二上第一次月考化学试卷(解析版) 题型:选择题
常温下,下列三种溶液中,由水电离出的氢离子浓度之比为( )
①1mol/L的盐酸②0.1mol/L的盐酸③0.01mol/L的NaOH.
A.1:10:100 B.0:1:12 C.14:13:12 D.14:13:2
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省高二上第一次月考化学试卷(解析版) 题型:选择题
pH=13的强碱溶液与pH=2的强酸溶液混合,所得溶液的pH=11,则强碱与强酸的体积比( )
A.11:1 B.9 :1 C.1 :11 D.1 :9
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广东实验中学顺德学校高二上阶段质检化学试卷(解析版) 题型:填空题
用酸性KMnO4和H2C2O4(草酸)反应研究影响反应速率的因素。一实验小组欲通过测定单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化):
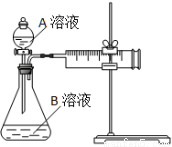
实验序号 | A溶液 | B溶液 |
① | 20 mL 0.1 mol·L-1H2C2O4溶液 | 30 mL 0.01 mol·L-1KMnO4溶液 |
② | 20 mL 0.2 mol·L-1H2C2O4溶液 | 30 mL 0.01 mol·L-1KMnO4溶液 |
(1)该反应的离子方程式 。(已知H2C2O4是二元弱酸)
(2)该实验探究的是 因素对化学反应速率的影响。相同时间内针筒中所得CO2的体积大小关系是 < (填实验序号)。
(3)若实验①在2 min末收集了2.24 mL CO2(标准状况下),则在2 min末, c(MnO4-)=__________mol/L(假设混合液体积为50 mL)
(4)除通过测定一定时间内CO2的体积来比较反应速率,本实验还可通过测定 来比较化学反应速率。(一条即可)
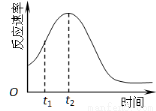 (5)小组同学发现反应速率总是如右图,其中t1~t2时间内速率变快的主要原因可能是:
(5)小组同学发现反应速率总是如右图,其中t1~t2时间内速率变快的主要原因可能是:
① ;② 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广东实验中学顺德学校高二上阶段质检化学试卷(解析版) 题型:选择题
下列说法正确的是( )
A.催化剂不影响反应活化能但能增大单位体积内活化分子百分数,从而增大反应速率
B.升高温度能使化学反应速率增大,主要原因是增加了反应物分子中活化分子的百分数
C.增大反应物浓度,可增大单位体积内活化分子的百分数,从而使有效碰撞次数增大
D.有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增加活化分子的百分数,从而使反应速率增大
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽省高二上第一次月考化学试卷(解析版) 题型:选择题
在一定温度下,下列叙述不是可逆反应A(g)+2B(g)  2C(g)达到平衡状态标志的是
2C(g)达到平衡状态标志的是
①C的生成速率与C的分解速率相等;
②单位时间生成amol A,同时生成2amolB;
③A、B、C的浓度不再变化;
④混合气体平均摩尔质量不再变化
⑤混合气体的总压强不再变化;
⑥混合气体的物质的量不再变化;
⑦单位时间内消耗amol A,同时生成2amol B
⑧A、B、C的分子数比为1:3:2
A.②⑧ B.①⑥ C.②④ D.③⑧
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com