
| A£® | ³ĘČ”Ģ¼ĖįÄĘ¾§Ģå£ØNa2CO3•10H2O£©100gĄ“ÅäÖĘ0.5mol/LµÄNa2CO3ČÜŅŗ1000mL | |
| B£® | ÅäÖĘNH3NO3ČÜŅŗ£¬ŌŚÉÕ±ÖŠČܽāŗóĮ¢¼“×¢ČėČŻĮæĘ棬²¢Į¢¼“½ųŠŠĻĀĆęµÄø÷Ļī²Ł×÷ | |
| C£® | ¶ØČŻŗ󣬽«ČŻĮæĘæÕńµ“¾łŌČ£¬¾²ÖĆŹ±·¢ĻÖŅŗĆęµĶÓŚæĢ¶ČĻߣ¬ÓŚŹĒÓÖ¼ÓČėÉŁĮæĖ®ÖĮæĢ¶ČĻß | |
| D£® | ČŻĮæĘæÓĆÕōĮóĖ®Ļ“¾»ŗóĪ“¾øÉŌļĀķÉĻÓĆĄ“ÅäÖĘČÜŅŗ |
·ÖĪö A£®½įŗĻn=vV”¢m=nM¼ĘĖć£»
B£®ÉÕ±ÖŠČܽāŗó£¬Ó¦»Öø“ÖĮŹŅĪĀŌŁ×ŖŅĘ£»
C£®¶ØČŻŗ󣬽«ČŻĮæĘæÕńµ“¾łŌČ£¬¾²ÖĆŹ±·¢ĻÖŅŗĆęµĶÓŚæĢ¶ČĻߣ¬ĪŖÕż³£ĻÖĻó£¬ŅŗĢåæÉÄܲŠĮōŌŚĘææŚ“¦£»
D£®ČŻĮæĘæÓĆÕōĮóĖ®Ļ“¾»ŗ󣬲»ŠčŅŖøÉŌļ£¬ÓŠÉŁĮæĖ®¶ŌŹµŃéĪŽÓ°Ļģ£®
½ā“š ½ā£ŗA£®ÅäÖĘ0.5mol/LµÄNa2CO3ČÜŅŗ1000mL£¬ŠčŅŖĢ¼ĖįÄĘ¾§Ģå£ØNa2CO3•10H2O£©µÄÖŹĮæĪŖ0.5mol/L”Į1L”Į286g/mol=143g£¬¹ŹA“ķĪó£»
B£®ÉÕ±ÖŠČܽāŗó£¬Ó¦»Öø“ÖĮŹŅĪĀŌŁ×ŖŅʵ½ČŻĮæĘæÖŠ£¬²»ÄÜČܽāŗóĮ¢¼“×¢ČėČŻĮæĘ棬¹ŹB“ķĪó£»
C£®¶ØČŻŗ󣬽«ČŻĮæĘæÕńµ“¾łŌČ£¬¾²ÖĆŹ±·¢ĻÖŅŗĆęµĶÓŚæĢ¶ČĻߣ¬ĪŖÕż³£ĻÖĻó£¬ŅŗĢåæÉÄܲŠĮōŌŚĘææŚ“¦£¬²»ŠčŅŖŌŁ¼ÓČėÉŁĮæĖ®ÖĮæĢ¶ČĻߣ¬¹ŹC“ķĪó£»
D£®ČŻĮæĘæÓĆÕōĮóĖ®Ļ“¾»ŗ󣬲»ŠčŅŖøÉŌļ£¬ÓŠÉŁĮæĖ®¶ŌŹµŃéĪŽÓ°Ļģ£¬ŌņæÉĪ“¾øÉŌļĀķÉĻÓĆĄ“ÅäÖĘČÜŅŗ£¬¹ŹDÕżČ·£»
¹ŹŃ”D£®
µćĘĄ ±¾Ģāæ¼²éÅäÖĘŅ»¶ØÅØ¶ČµÄČÜŅŗ£¬ĪŖøßĘµæ¼µć£¬°ŃĪÕÅäÖĘČÜŅŗµÄ²Ł×÷”¢ŅĒĘ÷µÄŹ¹ÓĆ”¢ŹµŃé¼¼ÄÜĪŖ½ā“šµÄ¹Ų¼ü£¬²ąÖŲ·ÖĪöÓėŹµŃéÄÜĮ¦µÄ漲飬עŅāŃ”ĻīBĪŖŅדķµć£¬ĢāÄæÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
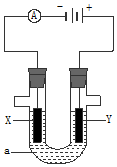 ČēĶ¼±ķŹ¾Ņ»øöµē½ā³Ų£¬Čē¹ūÓƵē½ā·½·Ø¾«Į¶“ÖĶ£¬µē½āŅŗaŃ”ÓĆĮņĖįĶČÜŅŗ£¬ŌņXµē¼«ŹĒ“æĶ£¬YµÄµē¼«·“Ó¦Ź½ŹĒ£ŗCu-2e-=Cu2+£®£®
ČēĶ¼±ķŹ¾Ņ»øöµē½ā³Ų£¬Čē¹ūÓƵē½ā·½·Ø¾«Į¶“ÖĶ£¬µē½āŅŗaŃ”ÓĆĮņĖįĶČÜŅŗ£¬ŌņXµē¼«ŹĒ“æĶ£¬YµÄµē¼«·“Ó¦Ź½ŹĒ£ŗCu-2e-=Cu2+£®£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| Ćū³Ę | ŠŌד | Ļą¶Ō·Ö ×ÓÖŹĮæ | Čܽā¶Č | |||
| ĄäĖ® | ČČĖ® | ŅŅ“¼ | ŅŅĆŃ | |||
| ß»ą«¼×Č© | ĪŽÉ«ŅŗĢå | 96 | Ī¢ČÜ | Ņ×ČÜ | Ņ×ČÜ | »„ČÜ |
| ß»ą«¼×“¼ | ĪŽÉ«ŅŗĢå | 98 | »„ČÜ | »„ČÜ | Ņ×ČÜ | Ņ×ČÜ |
| ß»ą«¼×Ėį | ĪŽÉ«¾§Ģå | 112 | Ī¢ČÜ | Ņ×ČÜ | æÉČÜ | Ņ×ČÜ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| ¶ĢÖÜĘŚŌŖĖŲ“śŗÅ | L | M | Q | R | T |
| Ō×Ó°ė¾¶/nm | 0.160 | 0.143 | 0.089 | 0.104 | 0.066 |
| Ö÷ŅŖ»ÆŗĻ¼Ū | +2 | +3 | +2 | +6”¢-2 | -2 |
| A£® | Ēā»ÆĪļµÄČČĪČ¶ØŠŌ£ŗH2T£¼H2R | |
| B£® | µ„ÖŹÓėĻ”ŃĪĖį·“Ó¦µÄĖŁĀŹ£ŗL£¼Q | |
| C£® | Ąė×Ó°ė¾¶£ŗR2-£¼L2+ | |
| D£® | MÓėTŠĪ³ÉµÄ»ÆŗĻĪļ¼ČÄÜÓėĒæĖį·“Ó¦£¬ÓÖÄÜÓėĒæ¼ī·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | mgøĆ“Å»ĘĢśæóÖŠŗ¬+2¼ŪµÄĢś0.75mol | |
| B£® | 200mLŃĪĖįÖŠHClĪļÖŹµÄĮæÅضČĪŖ4.25mol•L-1 | |
| C£® | Éś³ÉµÄH2SĘųĢåŌŚ±ź×¼×“æöĻĀµÄĢå»żĪŖ16.8L | |
| D£® | øĆ“Å»ĘĢśæóÖŠFe1-nSµÄn=0.15 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| Ń”Ļī | “żĢį“æĪļÖŹ | ŌÓÖŹ | ³żŌÓŹŌ¼Į¼°Ö÷ŅŖ²Ł×÷·½·Ø |
| A | ŅŅĶé | ŅŅĻ© | ĖįŠŌKMnO4ČÜŅŗ£¬Ļ“Ęų |
| B | äå±½ | äå | NaOHČÜŅŗ£¬·ÖŅŗ |
| C | ŅŅĖį | ŅŅ“¼ | ½šŹōÄĘ£¬ÕōĮó |
| D | ŅŅ“¼ | Ė® | ÉśŹÆ»Ņ£¬¹żĀĖ |
| A£® | A | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® |  ½«ŗ£“ų×ĘÉÕ»Ņ»Æ | B£® | 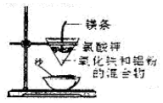 ĀĮČČ·“Ó¦ | ||
| C£® | 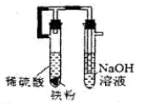 ÖĘČ”ĒāŃõ»ÆŃĒĢś | D£® | 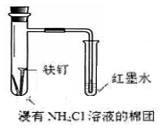 ŃéÖ¤ĢśµÄĪüŃõøÆŹ“ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
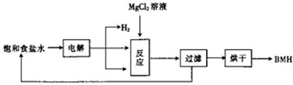 BMH{¼īŹ½“ĪĀČĖįĆ¾}[Mg2ClO£ØOH£©n•H2O]}ŹĒŅ»ÖÖ°×É«·ŪÄ©£®ÄŃČÜÓŚĖ®£¬ŹĒ³£ÓƵÄĪŽ»śæ¹¾ś¼Į£¬ĘäŅ»ÖÖÉś²ś¹¤ŅÕČēĶ¼ĖłŹ¾£®
BMH{¼īŹ½“ĪĀČĖįĆ¾}[Mg2ClO£ØOH£©n•H2O]}ŹĒŅ»ÖÖ°×É«·ŪÄ©£®ÄŃČÜÓŚĖ®£¬ŹĒ³£ÓƵÄĪŽ»śæ¹¾ś¼Į£¬ĘäŅ»ÖÖÉś²ś¹¤ŅÕČēĶ¼ĖłŹ¾£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ±ź×¼×“æöĻĀ£¬33.6 L·ś»ÆĒāÖŠŗ¬ÓŠ·śŌ×ӵďżÄæĪŖ1.5NA | |
| B£® | 5NH4NO3$\frac{\underline{\;\;”÷\;\;}}{\;}$2HNO3+4N2”ü+9H2O·“Ó¦ÖŠ£¬Éś³É28 g N2Ź±£¬×ŖŅʵĵē×ÓŹżÄæĪŖ3.75NA | |
| C£® | 50 mL 18.4 mol•L-1ÅØĮņĖįÓė×ćĮæĶ¼ÓČČ·“Ó¦£¬Éś³ÉSO2·Ö×ӵďżÄæĪŖ0.46NA | |
| D£® | ½«ŗ¬ÓŠ0.1 mol FeCl3µÄ±„ŗĶČÜŅŗµĪČė·ŠĖ®ÖŠ£¬Éś³ÉµÄ½ŗĢåÖŠŗ¬½ŗĢåĮ£×ӵďżÄæĪŖ0.1NA |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com