
| ʵ��Ŀ�� | �Լ������� |
| ����CuSO4��Na2SO4���ַ�ĩ | |
| ��������ˮ���Ƿ���Cl- | |
| ֤��Na2CO3��Һ���м��� | |
| ��ȥþ���л������������� |
| ʵ��Ŀ�� | �Լ������� |
| ����CuSO4��Na2SO4���ַ�ĩ | B |
| ��������ˮ���Ƿ���Cl- | C |
| ֤��Na2CO3��Һ���м��� | A |
| ��ȥþ���л������������� | D |


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���⻯ѧ�����IJ����������ŷŵ�β���й� |
| B�������õ綯���г�����Ħ�г��ǡ���̼���ѡ�����Ϊ |
| C��������ָPHС��7�����Խ�ˮ����Ҫ����ú��ȼ�����µ� |
| D����Cu��O2��ϡH2SO4��Ӧ����Cu��ŨH2SO4��Ӧ�Ƶ����ǡ���ɫ��ѧ�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
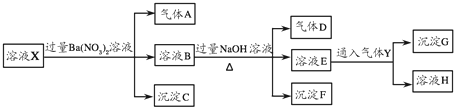
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 1Lij�����Һ�����ܺ��е��������±���
1Lij�����Һ�����ܺ��е��������±���| ���ܴ������е������� | H+��K+��Mg2+��Al3+��NH4+��Fe2+��Fe3+ |
| ���ܴ������е������� | Cl-��Br-��I-��CO32-��AlO2- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����С�մ���Һ�м��������Һ��HCO3-+H+=CO2��+H2O |
| B��������þ��ϡ���ᷴӦ��H++OH-=H2O |
| C������ˮ��Ӧ��������������Na+H2O=Na++OH-+H2�� |
| D��̼��������ᷴӦ��CaCO3+2H+=Ca2++H2O+CO2�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com