
| ||
| ||


 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案科目:高中化学 来源: 题型:
| A、K+:1s22s22p63s23p6 |
| B、F:1s22s22p5 |
| C、S2-:1s22s22p63s23p4 |
| D、Ar:1s22s22p63s23p6 |
查看答案和解析>>
科目:高中化学 来源: 题型:

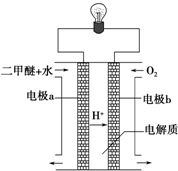


查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图是部分元素在元素周期表中位置,根据下列要求回答问题:
如图是部分元素在元素周期表中位置,根据下列要求回答问题:查看答案和解析>>
科目:高中化学 来源: 题型:
A、金属在潮湿的空气中腐蚀的实质是:M+nH2O═M(OH)n+
| ||
| B、金属的化学腐蚀的实质是:M-ne-=Mn+,电子直接转移给氧化剂 | ||
| C、金属的化学腐蚀必须在酸性条件下进行 | ||
| D、在潮湿的中性环境中,金属的电化学腐蚀主要是析氢腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CH4,CCl4,CO2 |
| B、C2H4,C2H2,C2H5OH |
| C、Cl2,H2,N2 |
| D、NH3,H2O,SO2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com