
【题目】己烯雌酚是一种激素类药物,其结构简式如图所示。下列有关叙述中正确的是()

A.遇FeCl3溶液不能发生显色反应
B.可与NaOH和NaHCO3溶液发生反应
C.1mol该有机物可以与5molBr2发生反应
D.己烯雌酚分子中一定有16个碳原子共平面
 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源: 题型:
【题目】脱硝技术是处理氮氧化物的有效方法之一。在1L的恒容密闭容器中充入2mol NH3、1mol NO和1mol NO2,发生反应:2NH3(g)+NO(g)+NO2(g)![]() 2N2(g)+3H2O(g)△H。在不同温度下发生上述反应,测得N2的物质的量(mol)与时间的关系如下表:
2N2(g)+3H2O(g)△H。在不同温度下发生上述反应,测得N2的物质的量(mol)与时间的关系如下表:
0 | 10 min | 20 min | 30 min | 40 min | |
T1K | 0 | 0.6 | 1.1 | 1.5 | 1.5 |
T2K | 0 | 0.8 | 1.4 | 1.4 | 1.4 |
回答下列问题:
(1)上述反应中___________(填字母)。
A. △S>0,△H>0 B. △S>0,△H<0 C. △S<0,△H>0 D. △S<0,△H<0
(2)T1_______(填“>”“<”或“=”)T2,理由是___________________________________________
(3)T1K下,0~20min内v(NO)=______________
(4)T2K下,NO2的平衡转化率为_____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】应对雾霾污染、改善空气质量需要从多方面入手,如开发利用清洁能源.甲醇是一种可再生的清洁能源,具有广阔的开发和应用前景.回答下列问题:
(1)![]() 与
与![]() 合成甲醇:
合成甲醇:![]() 但是找到合适的催化剂是制约该方法的瓶颈.目前主要使用贵金属催化剂,但是贵金属储量稀少,成本高昂,难以大规模应用,且使用中存在环境污染的风险.最近采用真空封管法制备磷化硼纳米颗粒,在发展非金属催化剂实现
但是找到合适的催化剂是制约该方法的瓶颈.目前主要使用贵金属催化剂,但是贵金属储量稀少,成本高昂,难以大规模应用,且使用中存在环境污染的风险.最近采用真空封管法制备磷化硼纳米颗粒,在发展非金属催化剂实现![]() 电催化还原制备甲醇方向取得重要进展,该反应历程如图所示.
电催化还原制备甲醇方向取得重要进展,该反应历程如图所示.
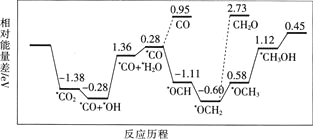
容易得到的副产物有CO和![]() ,其中相对较多的副产物为________________;上述合成甲醇的反应速率较慢,要使反应速率加快,主要降低下列变化中________
,其中相对较多的副产物为________________;上述合成甲醇的反应速率较慢,要使反应速率加快,主要降低下列变化中________![]() 填字母
填字母![]() 的能量变化.
的能量变化.
A.![]() B.
B.![]()
C.![]() D.
D.![]()
(2)恒压![]() 容器的容积可变
容器的容积可变![]() 下,
下,![]() 与
与![]() 在催化剂作用下发生反应
在催化剂作用下发生反应![]()
![]() ,
,![]() 的平衡转化率与温度、压强的关系如图所示.
的平衡转化率与温度、压强的关系如图所示.
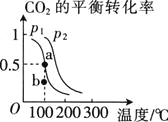
①压强![]() ________
________![]() 填“
填“![]() ”或“
”或“![]() ”
”![]() .
.
②在![]() 、
、![]() 条件下,b点时
条件下,b点时![]() ________
________![]() 填“
填“![]() ”或“
”或“![]() ”
”![]() .
.
③已知:反应速率![]() ,
,![]() 、
、![]() 分别为正、逆反应速率常数,x为物质的量分数,若b点对应的坐标参数为
分别为正、逆反应速率常数,x为物质的量分数,若b点对应的坐标参数为![]() ,计算b处的
,计算b处的![]() ________
________![]() 保留3位有效数字
保留3位有效数字![]() .
.
(3)焦炭与水蒸气在恒容密闭容器中反应制合成气的主要反应![]() Ⅰ
Ⅰ![]() 、
、![]() Ⅱ
Ⅱ![]() 的
的![]() 为以分压表示的平衡常数
为以分压表示的平衡常数![]() 与T的关系如下图所示.
与T的关系如下图所示.
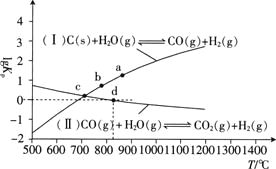
①反应![]() Ⅱ
Ⅱ![]() 的
的![]() ________
________![]() 填“大于”“等于”或“小于”
填“大于”“等于”或“小于”![]() .
.
②![]() 点时,反应
点时,反应![]() 的
的![]() ________
________![]() 填数值
填数值![]() .
.
③在恒容密闭容器中充入![]() 、
、![]() 只发生反应
只发生反应![]() Ⅱ
Ⅱ![]() ,图中d点处达到平衡时,CO的转化率为________;达到平衡时,向容器中再充入
,图中d点处达到平衡时,CO的转化率为________;达到平衡时,向容器中再充入![]() 、
、![]() ,重新达到平衡时,CO的平衡转化率________
,重新达到平衡时,CO的平衡转化率________![]() 填“增大”“减小”或“不变”
填“增大”“减小”或“不变”![]() .
.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列溶液中由水电离的氢离子浓度为1×10-5的是 ( )
A.pH=5的HClO 溶液B.pH=9的氨水
C.pH=5的AlCl3溶液D.pH=5的NaHSO4溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通常检测SO2含量是否达到排放标准的反应原理是SO2 +H2O2 + BaCl2 ===BaSO4↓+ 2HCl。NA表示阿伏伽德罗常数,下列说法正确的是( )
A. 0.1 mol BaCl2晶体中所含微粒总数为0.1NA
B. 25 ℃时,pH =1的HCl溶液中含有H+的数目为0.1NA
C. 17 g H2O2中含有非极性键数目为0.5NA
D. 生成2.33 g BaSO4沉淀时,转移电子数目为0.01NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关醛的说法正确的是
A.分子通式为CnH2nO的有机物与乙醛一定互为同系物
B.用溴水可以检验CH2=CHCHO中含有的碳碳双键
C.对甲基苯甲醛(![]() )可使酸性KMnO4溶液褪色,说明醛基具有还原性
)可使酸性KMnO4溶液褪色,说明醛基具有还原性
D.能发生银镜反应的有机物不一定是醛类
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,有c(HA)+c(A-)=0.1mol/L的一组HA、KA混合溶液,溶液中c(HA)、c(A-)与pH的关系如下图所示。下列叙述不正确的是 ( )
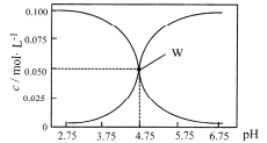
A.pH=5.75的溶液中:c(K+)>c(A-)>c(HA)> c (H+)>c(OH-)
B.欲得W点所示溶液,起始所加溶液应符合c(HA)+c(A-)=0.1mol/L且c(KA)<c(HA)
C.pH=3.75的溶液中:c(K+)+c(H+)-c(OH-)+c(HA)=0.1mol/L
D.若A-的水解常数为Kh,则lgKh=-9.25
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组同学利用下图装置(夹持仪器已省略)制备溴苯,并探究该反应原理。
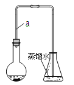
I.制备溴苯
(1)装置中长导管a的作用是______、导出气体,制备溴苯的反应方程式属于______反应,其方程式为________
(2)本实验所获得的溴苯为褐色,是因为________________。
II.分离提纯
已知,溴苯与苯互溶,液溴、苯、溴苯的沸点依次为59℃、80℃、156℃。同学们设计了如下流程:
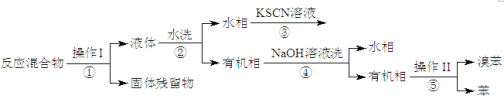
(3)操作Ⅱ为_____________。
(4)流程②和④中,需要用到的玻璃仪器是烧杯、_______;流程③的现象为______,流程④的作用是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组为了研究外界条件对化学反应速率的影响,进行了如下实验:
(实验原理)2KMnO4 + 5H2C2O4 + 3H2SO4 = K2SO4 + 2MnSO4 + 10CO2↑ + 8H2O
(实验内容及记录)
实验编号 | 室温下,试管中所加试剂及其用量 / mL | 室温下溶液颜色褪至无色所需时间 / min | |||
0.6 mol/L H2C2O4溶液 | H2O | 3 mol/L 稀硫酸 | 0.05mol/L KMnO4溶液 | ||
1 | 3.0 | 2.0 | 2.0 | 3.0 | 1.5 |
2 | 2.0 | 3.0 | 2.0 | 3.0 | 2.7 |
3 | 1.0 | 4.0 | 2.0 | 3.0 | 3.9 |
请回答:
(1)根据上表中的实验数据,可以得到的结论是___________________________________。
(2)利用实验1中数据计算,若用KMnO4的浓度变化表示的反应速率为:υ(KMnO4)= ________。
(3)该小组同学根据经验绘制了n(Mn2+) 随时间变化趋势的示意图,如图1所示。但有同学查阅已有的实验资料发现,该实验过程中n(Mn2+) 随时间变化的趋势应如图2所示。该小组同学根据图2所示信息提出了新的假设,并继续进行实验探究。
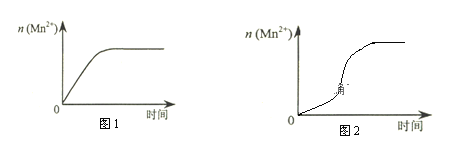
①该小组同学提出的假设是___________________________________________________。
②请你帮助该小组同学完成实验方案,并填写表中空白。
实验编号 | 室温下,试管中所加试剂及其用量 / mL | 再向试管中加入少量固体 | 室温下溶液颜色褪至无色所需时间 / min | |||
0.6mol/L H2C2O4溶液 | H2O | 3mol/L稀硫酸 | 0.05mol/L KMnO4溶液 | |||
4 | 3.0 | 2.0 | 2.0 | 3.0 | _______ | t |
③若该小组同学提出的假设成立,应观察到的现象是_____________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com