
分析 (1)根据m=nM计算;
(2)根据n=$\frac{N}{{N}_{A}}$计算分子的物质的量,再根据分子中质子数分析;
(3)根据n=$\frac{V}{Vm}$=$\frac{m}{M}$计算;
(4)先求出碳酸钠的物质的量,再根据c=$\frac{n}{V}$计算.
解答 解:(1)m=nM=1.5mol×98g/mol=147g;
故答案为:147g;
(2)n=$\frac{N}{{N}_{A}}$=$\frac{9.03×1{0}^{23}}{6.02×1{0}^{23}}$=1.5mol,一个分子中含有10个质子,则1.5mol氨气中含有15mol质子;
故答案为:15mol;
(3)n=$\frac{V}{Vm}$=$\frac{0.672L}{22.4L/mol}$=0.03mol,M=$\frac{m}{n}$=$\frac{1.92g}{0.03mol}$=64g/mol;
故答案为:64g/mol;
(4)71.5g碳酸钠晶体(Na2CO3•10H2O)的物质的量为n=$\frac{m}{M}$=$\frac{71.5g}{286g/mol}$=0.25mol,溶于水,配成500ml溶液,此溶液的物质的量浓度为,c=$\frac{n}{V}$=$\frac{0.25mol}{0.5L}$=0.5 mol/L;
故答案为:0.5 mol/L.
点评 本题考查物质的量的计算,侧重于学生计算能力的考查,注意把握物质的量的相关计算公式的运用,把握分子的构成,为解答该题的关键,难度不大.


 口算题天天练系列答案
口算题天天练系列答案科目:高中化学 来源: 题型:选择题
| A. | 红热的铜丝在氯气中剧烈燃烧,生成棕黄色的烟 | |
| B. | 大量氯气泄漏时,应用浸有弱碱性溶液的毛巾捂住口鼻身向高处跑 | |
| C. | AlCl3、FeCl2、FeCl3均可通过化合反应制得 | |
| D. | 向FeCl2溶液中滴加氯水,溶液颜色变成棕黄色,说明氯水中含有HClO |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 石灰水[Ca(OH)2] | B. | 盐酸 | ||
| C. | 明矾[KAl(SO4)2•12H2O] | D. | 纯碱(Na2CO3) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
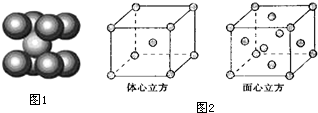
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | A | B | C | D |
| 研究 目的 | 压强对反应的 影响(P2>P1) | 温度对反应的影响 | 平衡体系增加A 对反应的影响 | 催化剂对反应的影响 |
| 图示 | 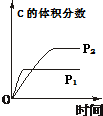 | 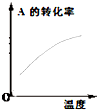 | 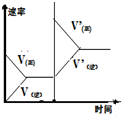 | 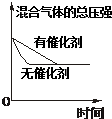 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
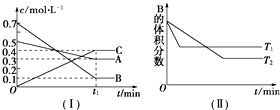 T℃时,A气体与B气体反应生成C气体,反应过程中A、B、C浓度变化如图(Ⅰ)所示,若保持其他条件不变,温度分别为T1和T2时,B的体积分数与时间的关系如图(Ⅱ)所示.根据以上条件,回答下列问题:
T℃时,A气体与B气体反应生成C气体,反应过程中A、B、C浓度变化如图(Ⅰ)所示,若保持其他条件不变,温度分别为T1和T2时,B的体积分数与时间的关系如图(Ⅱ)所示.根据以上条件,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 装置名称:①是原电池,②是电解池 | |
| B. | 电极反应式:①中阳极:4OH--4e-═2H2O+O2↑ ②中正极:2H++2e-═H2↑ | |
| C. | 硫酸浓度变化:①减小,②增大 | |
| D. | 离子移动方向:①中H+向阴极方向移动,②中H+向负极方向移动 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com