
用NA表示阿伏加德罗常数的值,下列说法正确的是
A.常温、常压下,16 g O3中含有的氧原子数为
B.7.8 g Na2O2与水充分反应,转移的电子数为0.2 NA
C.0.1 mol Fe与0.1 mol Cl2充分反应,转移的电子数为0.3NA
D.标准状况下,11.2 L H2O中含有的氢原子数为NA
A
【解析】
试题分析:A选项16 g O3的物质的量为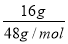 =
= ,故氧原子的数目为
,故氧原子的数目为 ×3 = 1mol,即为1NA,A选项正确;B选项 2 Na2O2+2H2O===4NaOH+O2↑,该反应可知,2mol Na2O2转移的电子为2mol,7.8 g Na2O2为0.1mol,故转移的电子为0.1 NA,故B选项错误;C选项0.1 mol Fe与0.1 mol Cl2充分反应,Cl2有强氧化性,可以把Fe氧化成FeCl3,铁过量,故转移电子按照Cl2计算,故应该转移0.1NA;故C错误;D选项,标准状况下,H2O为冰与水的混合体系,不属于气态物质,不能利用气体的摩尔体积参与计算,所以D错误。
×3 = 1mol,即为1NA,A选项正确;B选项 2 Na2O2+2H2O===4NaOH+O2↑,该反应可知,2mol Na2O2转移的电子为2mol,7.8 g Na2O2为0.1mol,故转移的电子为0.1 NA,故B选项错误;C选项0.1 mol Fe与0.1 mol Cl2充分反应,Cl2有强氧化性,可以把Fe氧化成FeCl3,铁过量,故转移电子按照Cl2计算,故应该转移0.1NA;故C错误;D选项,标准状况下,H2O为冰与水的混合体系,不属于气态物质,不能利用气体的摩尔体积参与计算,所以D错误。
考点:物质的量 阿伏加德罗常数( NA) 微观粒子的计算
点评:本题考查基本的化学计算,同学们熟练掌握物质的量、阿伏伽德罗常数和原子、电子等微观粒子的计算。同时本题陷阱较多,如理解过氧化钠与水反应属于歧化,氯气虽然与变价的铁反应生成了三氯化铁,但是注意“量”的问题。D选项属于常见的陷阱,学生较容易发现。


 课课优能力培优100分系列答案
课课优能力培优100分系列答案 优百分课时互动系列答案
优百分课时互动系列答案科目:高中化学 来源:2014-2015学年陕西省安康市高三上学期第二次教学质量调研化学试卷(解析版) 题型:选择题
某同学为检验溶液中是否含有常见的几种离子,进行了如下图所示的实验操作。其中,检验过程中产生的气体能使湿润的红色石蕊试纸变蓝。由该实验能得到的正确结论是

A.原溶液中一定含有SO42- B.原溶液中不一定含有NH4+
C.原溶液中一定含有Cl- D.原溶液中含Fe2+、Fe3+至少有一种
查看答案和解析>>
科目:高中化学 来源:2014-2015江苏省盐城市高二12月月考化学试卷(解析版) 题型:实验题
16.(10分)实验室有一瓶混有氯化钠的氢氧化钠固体试剂,经测定NaOH的质量分数约为82.0%,为了验证其纯度,用浓度为0.2mol/L的盐酸进行滴定,试回答下列问题:
(1)托盘天平称量5.0g固体试剂,用蒸馏水溶解于烧杯中,并振荡,然后立即直接转入 500mL容量瓶中,恰好至刻度线,配成待测液备用。请改正以上操作中出现的五处错误。
① ,② ,③ ,
④ ,⑤ 。
(2)将标准盐酸装在25.00mL 滴定管中,调节液面位置在 处,并记下刻度。
(3)取20.00mL待测液,待测定。该项实验操作的主要仪器有 。
用 试剂作指示剂时,滴定到溶液颜色由 刚好至 色时为止。
(4)滴定达终点后,记下盐酸用去20.00mL,计算NaOH的质量分数为 。
(5)试分析滴定误差可能由下列哪些实验操作引起的 。
A.移待测液至容量瓶时,未洗涤烧杯
B.酸式滴定管用蒸馏水洗涤后,直接装盐酸
C.滴定时,反应容器摇动太激烈,有少量液体溅出
D.滴定到终点时,滴定管尖嘴悬有液滴
E.读数(滴定管)开始时仰视,终点时俯视
查看答案和解析>>
科目:高中化学 来源:2014-2015河北省高一上学期第二次月考化学试卷(解析版) 题型:填空题
(8分)已知下列氧化还原反应在溶液中均能发生。
①2Fe3++2I-=2Fe2++I2;②2Fe2++Br2=2Fe3++2Br-;③2Br-+Cl2=2Cl-+Br2。
(1)Fe2+、Br-、I-三种微粒按还原性由强到弱的顺序为____________________。
(2)现有某混合溶液中含a mol FeI2和b mol FeBr2,向该混合液中逐渐通入c mol Cl2,试根据以上化学原理分析,当只有I-被氧化时,c的取值范围是______________。
(3)某混合溶液中只含有Fe2+、Cl-、Br-、I-(忽略水的电离),其中Cl-、Br-、I-的个数比为2∶3∶4。向该溶液中通入氯气,使溶液中Cl-和Br-的个数比为3∶1,则通入氯气的物质的量与溶液中剩余Fe2+的物质的量之比为_____________________。
查看答案和解析>>
科目:高中化学 来源:2014-2015河北省高一上学期第二次月考化学试卷(解析版) 题型:选择题
下列对有关实验事实的解释正确的是
A.向某溶液中滴加氯水后,再加入KSCN溶液,溶液呈红色,说明原溶液中含有Fe2+
B.浓硫酸和浓盐酸长期暴露在空气中浓度均降低,原理不相同
C.向某溶液中加入氯化钡溶液,生成白色沉淀,再加入稀盐酸,沉淀不溶解,则原溶液一定含有SO42
D.常温下,浓硫酸可以用铁质容器储运,说明铁与冷的浓硫酸不反应
查看答案和解析>>
科目:高中化学 来源:2014-2015河北省高一上学期第二次月考化学试卷(解析版) 题型:选择题
实验室保存下列试剂的方法不正确的是
A.NaOH溶液存放在带橡胶塞的细口玻璃瓶中
B.氯水存放在棕色细口玻璃瓶中,并置于冷暗处
C.浓硫酸存放在带橡胶塞的细口玻璃瓶中
D.金属钠用煤油液封于广口玻璃瓶中
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省广安市高三“一诊”理综化学试卷(解析版) 题型:填空题
(13分) A、B、C、D、E、F、G、H是核电荷数依次增大的短周期主族元素。元素A的原子半径是所有元素中最小的。A、E同主族,B、C、D同周期,D、G最外层电子数相等,G的质量数为D的2倍,元素B的一种常见单质可做惰性电极材料,其最高价氧化物甲为常见温室气体。B、D、G的质子数之和等于F、H的质子数之和,I单质是日常生活中用量最大的金属,易被腐蚀或损坏。回答下列问题:
(1)I元素在周期表中的位置 。
(2)化合物甲的结构式为 。
(3)根据以上信息,下列说法不正确的是______________。
A.A和B能形成多种化合物
B.热稳定性: H2D< H2G
C.元素G的最高价氧化物对应水化物的酸性比H的弱
D.简单离子半径的大小顺序:rD <rE<rF E.沸点:H2D< H2G
F.同温同压下,将a L CA3和b L AH通入水中,若所得溶液的pH=7,则a>b
(4)常温下,相同浓度F、I简单离子的溶液中滴加NaOH溶液,F、I两元素先后沉淀,F (OH)n完全沉淀的pH是4.7,I (OH)n完全沉淀的pH是2.8,则ksp较大的是: (填化学式)
(5)若在H与I组成的某种化合物的溶液乙中,加入铜片,溶液会慢慢变为蓝色,依据产生该现象的反应原理,所设计的原电池如图所示,其反应中正极电极反应式为 。
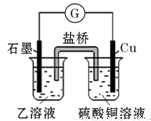
(6)若用石墨电极电解含有0.04 mol CuGD4和0.04 mol EH的混合溶液400 mL,当阳极产生的气体784 mL(标况)时,溶液的pH= (假设电解后溶液体积不变)。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省成都郫县高三第二次阶诊断性考试理综化学试卷(解析版) 题型:选择题
M、X、Y、Z、W为五种短周期元素,原子序数依次递增,X、Y、Z是同周期元素,且最外层电子数之和为15,X与Z可形成气体分子XZ2,Y与M形成的气态化合物密度在相同状况下是氢气的8.5倍,W的质子数是M、X、Y、Z四种元素质子数之和的一半。下列说法正确的是
A.原子半径:M>Z>Y>X>W
B.XZ2、X2M2、W2Z2均为直线型的共价化合物
C.由X、Y、Z、M四种元素形成的化合物不能含有离子键
D.由X元素形成的某种单质能导电,可以做电极
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省南京市、盐城市高三一模化学试卷(解析版) 题型:实验题
(15分)利用废铝箔(主要成分为Al、少量的Fe、Si等)既可制取有机合成催化剂AlBr3又可制取净水剂硫酸铝晶体[A12(SO4)3?18H2O]。
I.实验室制取无色的无水AlBr3(熔点:97.5℃,沸点:263.3~265℃)可用如图所示装置,
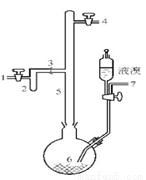
主要实验步骤如下:
步骤l.将铝箔剪碎,用CCl4浸泡片刻,干燥,然后投入到烧瓶6中。
步骤2.从导管口7导入氮气,同时打开导管口l和4放空,一段时间后关闭导管口7和1;导管口4接装有五氧化二磷的干燥管。
步骤3.从滴液漏斗滴入一定量的液溴于烧瓶6中,并保证烧瓶6中铝过剩。
步骤4.加热烧瓶6,回流一定时间。
步骤5.将氮气的流动方向改为从导管口4到导管口l。将装有五氧化二磷的干燥管与导管口1连接,将烧瓶6加热至270℃左右,使溴化铝蒸馏进入收集器2。
步骤6.蒸馏完毕时,在继续通入氮气的情况下,将收集器2从3处拆下,并立即封闭3处。
(1)步骤l中,铝箔用CCl4浸泡的目的是 。
(2)步骤2操作中,通氮气的目的是 。
(3)步骤3中,该实验要保证烧瓶中铝箔过剩,其目的是 。
(4)铝与液溴反应的化学方程式为 。
(5)步骤4依据何种现象判断可以停止回流操作 。
(6)步骤5需打开导管口l和4,并从4通入N2的目的是 。
II.某课外小组的同学拟用废铝箔制取硫酸铝晶体,已知铝的物种类别与溶液pH关系如图所示,实验中可选用的试剂:处理过的铝箔;2.0mol?L-1NaOH溶液:2.0 mol?L-1硫酸

(7)由铝箔制备硫酸铝晶体的实验步骤依次为:
①称取一定质量的铝箔于烧杯中,分次加入2.0 mol?L-1NaOH溶液,加热至不再产生气泡为止。
②过滤 ③ ;
④过滤、洗涤 ⑤ ;⑥ ;
⑦冷却结晶; ⑧过滤、洗涤、干燥。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com