
分析 常见影响化学反应速率的因素有浓度、温度、压强、催化剂以及固体的表面积等,一般来说浓度越大、温度越高、压强越大以及增大固体表面积、加入催化剂等,都可增大反应速率,以此解答.
解答 解:(1)固体参加反应,固体的表面加影响反应速率,将黄铁矿粉碎成细小的矿粒,可增大反应速率,故答案为:反应物的接触面积;
(2)反应中二氧化锰起到催化剂的作用,故答案为:催化剂;
(3)锌与镁的活动性顺序不同,与盐酸反应的剧烈程度不同,
故答案为:反应物本身的性质;
(4)盐酸浓度不同,反应速率不同,故答案为:反应物的浓度;
(5)镁条在燃烧时放出耀眼的白光,氢气和氯气在光照条件下可发生反应,则影响反应速率的因素为光照,故答案为:光照.
点评 本题考查影响化学反应速率的因素,侧重于学生的分析能力和基本概念的理解和运用的考查,为高频考点,注意相关基础知识的积累,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 原子半径:A<B<C<D | |
| B. | 非金属性:A>C | |
| C. | B和D最高价氧化物对应水化物相互不反应 | |
| D. | 单质B常温下能溶于浓硝酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
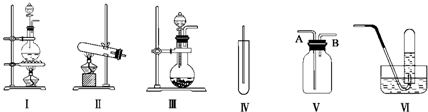
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
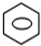 +HNO3(浓)$→_{△}^{浓硫酸}$
+HNO3(浓)$→_{△}^{浓硫酸}$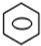 -NO2+H2O
-NO2+H2O ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
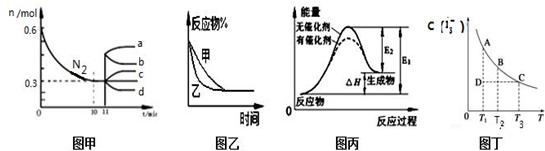
| A. | 图甲表示在 2L 的密闭容器中发生合成氨反应时 N2 的物质的量随时间的变化曲线,从 11min 起其它条件不变,压缩容器的体积为 1L,则 n(N2)的变化曲线为 d | |
| B. | 图乙表示压强对可逆反应 2A(g)+2B(g)?3C(g)+D(g)的影响,乙的压强比甲的压强大 | |
| C. | 图丙表示的反应是吸热反应,该图表明催化剂不能改变化学反应的焓变 | |
| D. | 图丁表示反应:I2(aq)+I-(aq)?I-3(aq)进行到状态 D 时一定有v 逆>v 正 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
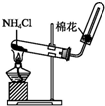
| A. | 氨和铵盐都易溶于水,都能生成NH4+ | |
| B. | 铵态氮肥与碱性物质如草木灰混合施用肥效更高 | |
| C. | 实验室制备氨气的试剂和装置可为如图装置 | |
| D. | 工业上用氨气液化需吸收热量的过程做制冷剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
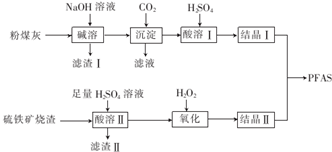
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com