
某温度下纯水中c(H+)=10﹣6mol/L,此温度下pH=5的盐酸与pH=9的氢氧化钡溶液混合后pH=7,则氢氧化钡溶液与盐酸之比为( )
|
| A. | 2:99 | B. | 1:1 | C. | 1:99 | D. | 1:100 |
考点:
pH的简单计算.
专题:
电离平衡与溶液的pH专题.
分析:
某温度下,纯水中c(H+)=10﹣6mol/L,所以水的离子积常数KW=10﹣12,pH=9的氢氧化钡溶液中氢氧根离子的物质的量浓度=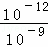 =10﹣3 mol/L,pH=5的盐酸溶液中氢离子的物质的量浓度为10﹣5 mol/L,水的离子积常数Kw=10﹣12,即PH=6时,溶液呈中性,当混合溶液的pH=7时,溶液呈碱性,即氢氧化钡过量.
=10﹣3 mol/L,pH=5的盐酸溶液中氢离子的物质的量浓度为10﹣5 mol/L,水的离子积常数Kw=10﹣12,即PH=6时,溶液呈中性,当混合溶液的pH=7时,溶液呈碱性,即氢氧化钡过量.
解答:
解:当混合溶液的pH=7时,混合溶液中氢氧根离子的物质的量浓度=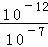 =10﹣5 mol/L.
=10﹣5 mol/L.
设盐酸的体积为X,氢氧化钡的体积为Y,
两种溶液混合后氢氧根离子的物质的量浓度═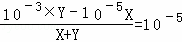 ,解得X:Y=99:2,
,解得X:Y=99:2,
故选A.
点评:
本题考查了混合溶液PH的计算,难度不大,注意该题中中性溶液的PH不等于7而是为6,能灵活运用水的离子积常数是解本题的关键.


科目:高中化学 来源: 题型:
以下物质间的每步转化通过一步反应能实现的
是( )
A.Al → Al2O3→ Al(OH)3 → NaAlO2
B.Si → SiO2 → H2SiO3 → Na2SiO3
C.N 2 → NO→ NO2 → HNO3
2 → NO→ NO2 → HNO3
D.S → SO3 → H2SO4 → MgSO4
查看答案和解析>>
科目:高中化学 来源: 题型:
关于几种分子中的化学键描述不正确的是( )
|
| A. | 苯每个碳原子的未参加杂化的2p轨道形成大π键 |
|
| B. | CH4中的4个C﹣H键都是H的1s轨道与C的2p轨道形成的s﹣p σ键 |
|
| C. | C2H4中,每个碳原子的sp2杂化轨道形成σ键、未杂化的2p轨道形成π键 |
|
| D. | H2分子中存在s﹣s σ键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
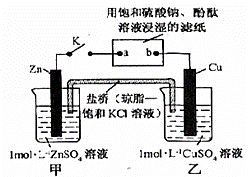
将右图所示实验装置,下列判断正确的是( )
|
| A. | 电子沿Zn→a→b→Cu路径流动 |
|
| B. | 铜电极上发生氧化反应 |
|
| C. | 盐桥中的K+向甲烧杯移动 |
|
| D. | 片刻后可观察到滤纸a点变红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
某研究性学习小组为了探究醋酸的电离情况,进行了如下实验.
实验一配制一定浓度的醋酸溶液
(1)取冰醋酸配制250mL0.2mol/L的醋酸溶液,用0.2mol/L的醋酸溶液稀释成所需浓度的溶液,配制250mL 0.2mol/L醋酸溶液时需要用到的玻璃仪器有量筒、烧杯、玻璃棒、 和 .
实验二 探究浓度对醋酸电离程度的影响
测定25℃时不同浓度的醋酸的pH,结果如下:
| 醋酸浓度(mol•L﹣1) | 0.0010 | 0.100 | 0.0200 | 0.1000 | 0.2000 |
| pH | 3.88 | 3.38 | 3.23 | 2.88 | 2.73 |
(2)表中数据是利用 (填仪器名称)测得的,根据表中数据,可以得出醋酸是 (填“强电解质”或“弱电解质”),你得出此结论的依据是
(3)已知10﹣2.73=1.86×10﹣3,利用此数据可以求得0.2000mol•L﹣1醋酸溶液的电离度α=
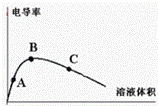
(4)用水稀释冰醋酸,电导率随加入水量的变化如右图所示A、B、C三点的电离度由大到小排列:
实验三 探究 对醋酸电离程度的影响
某同学利用传感器技术(如右下图),将20mL,0.1mol/L醋酸溶液放置在可加热磁力搅拌器上,并用pH传感器测量溶液的pH,利用电脑处理实验数据并作图(如下图)
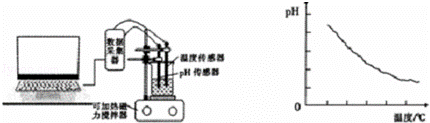
(5)由数据处理结果可以得到的结论是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列五种烃①2﹣甲基丁烷②2,2﹣二甲基丙烷③戊烷④丙烷⑤丁烷,按沸点由高到低的顺序排列的是( )
A. ①>②>③>④>⑤ B. ②>③>⑤>④>① C. ③>①>②>⑤>④ D. ④>⑤>②>①>③
查看答案和解析>>
科目:高中化学 来源: 题型:
为了测定某有机物A的结构,做如下实验:
①将2.3g该有机物完全燃烧,生成0.1mol CO2和2.7g水.
②用质谱仪测定其相对分子质量,得如图一所示的质谱图.
③用核磁共振仪处理该化合物,得到如图二所示图谱,图中三个峰的面积之比是1:2:3.
④用红外光谱仪处理该化合物,得到如图三所示图谱.
试回答下列问题:

(1)有机物A的相对分子质量是 .
(2)有机物A的实验式是 .
(3)能否根据本题信息确定A的分子式 (填“能”或“不能”),若能,则A的分子式是 ,若不能,则此空及(4)均不填.
(4)推测有机物A的结构简式为 ,A中含官能团的名称是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
现有如下两个反应:
A、2NaOH+H2SO4═Na2SO4+2H2O
B、CH4+2O2═CO2+2H2O
(1)根据反应的本质,两个反应都为 反应(放热或吸热),判断两个反应能否设计为原电池?(能或不能)
A B
(2)如果不能,说明其理由
(3)如果能,最好应选择 NaOH 电解质溶液(NaOH或H2SO4).则负极电极反应式: 正极电极反应式: .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com