
分析 (1)Q为氧,非极性分子R为CO2;
(2)将不溶性固体和液体分离通常采用的方法是过滤;由于Na可以与水(或乙醇)发生反应;
(3)根据反应的方程式计算生成Na2SiO3的物质的量,进而计算浓度;
(4)①Na还原CCl4的反应属于置换反应,但Cl2与H2O反应生成HCl和HClO;
②水晶属于原子晶体,而干冰属于分子晶体;
③元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强.
解答 解:(1)由题给信息“碳与Q的单质化合仅能生成两种常见气态化合物,其中一种化合物R为非极性分子”可推知Q为氧,非极性分子R为CO2.根据周期序数=电子层数,主族序数=最外层电子数可以确定碳在周期表中的位置是第二周期第ⅣA族,
故答案为:第二周期第ⅣA族;氧(或O);
(2)金刚石是不溶于CCl4的固体,CCl4是液体,将不溶性固体和液体分离通常采用的方法是过滤;由于Na可以与水(或乙醇)发生反应,而金刚石不与水(或乙醇)反应,所以除去粗产品中少量的钠可用水(或乙醇),
故答案为:过滤;水(或乙醇);
(3)根据硅与NaOH反应的化学方程式Si+2NaOH+H2O═Na2SiO3+2H2↑可写出其离子方程式为Si+2OH-+H2O═SiO32-+2H2↑,
计算溶液中硅酸盐的物质的量浓度需要根据化学方程式进行计算:
Si+2NaOH+H2O═Na2SiO3+2H2↑
28 g 1 mol 2 mol
m(Si) n1(Na2SiO3) 0.1 mol
m(Si)=$\frac{28g×0.1mol}{2mol}$=1.4g,
n1(Na2SiO3)=$\frac{0.1mol}{2}$=0.05 mol,
粗产品中SiO2的质量为m(SiO2)=20.0g-11.4g-1.4 g=7.2 g
SiO2+2NaOH═Na2SiO3+H2O
60g 1mol
7.2g n2(Na2SiO3)
n2(Na2SiO3)=$\frac{1mol×7.2g}{60g}$=0.12mol,
则n(Na2SiO3)=n1(Na2SiO3)+n2(Na2SiO3)=0.12mol+0.05mol=0.17mol,
硅酸盐的物质的量浓度为$\frac{0.17mol}{1L}$=0.17mol/L,
故答案为:Si+2OH-+H2O═SiO32-+2H2↑;0.17 mol•L-1;
(4)①Na还原CCl4的反应属于置换反应,但Cl2与H2O反应生成HCl和HClO,不是置换反应,故①错误;
②水晶属于原子晶体,而干冰属于分子晶体,熔化时克服粒子间作用力的类型不相同,故②错误;
③Na2SiO3溶液与SO3的反应,说明酸性H2SiO3比H2SO4弱,则可用于推断Si与S的非金属性强弱,故③正确;
故答案为:③.
点评 本题综合元素化合物知识,题目难度中等,注意从质量守恒的角度结合反应的化学方程式计算,(3)为易错点.


科目:高中化学 来源: 题型:选择题
| A. | CH3-CH3和CH3-CH2-CH3 | B. | CH2=CH2和CH3-CH3 | ||
| C. | CH3-OH和CH3-CH3 | D. | CH4和H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电解过程中阴极质量不断减少 | |
| B. | 电解过程中溶液的pH不断升高 | |
| C. | 此时向溶液中加入适量的Ag2O固体可使溶液恢复电解前的状况 | |
| D. | 电解后两极产生的气体体积比为2:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
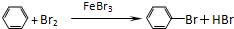 属于取代反应
属于取代反应 属于取代反应
属于取代反应 属于加聚 反应
属于加聚 反应查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  和 和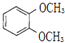 不属于同分异构体的 不属于同分异构体的 | |
| B. | 质量相同的C3H6 和C2H6完全燃烧时消耗氧气的质量较少的是C3H6 | |
| C. | 连接四个不同基团的碳原子为“手性碳原子”,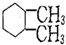 含有两个手性碳原子 含有两个手性碳原子 | |
| D. | 标准状况下22.4 L溴乙烷所含化学键总数为7NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
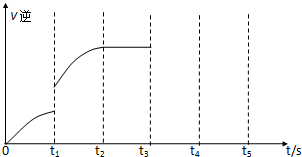
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com