
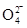 )。
)。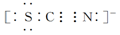
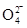 ,请写出该离子反应方程式________________________。
,请写出该离子反应方程式________________________。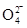 +6Cl-+16H+
+6Cl-+16H+ 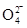 +6Cl-+16H+。
+6Cl-+16H+。

科目:高中化学 来源:不详 题型:单选题
| A.①③ | B.③② | C.①②③ | D.③① |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题


查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
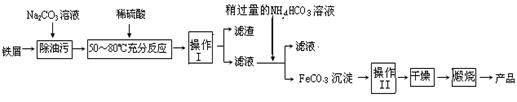
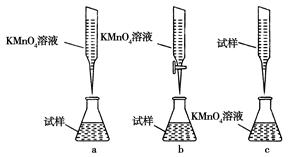
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.若金属有剩余,在溶液中再滴入硫酸后,金属不溶解 |
| B.若金属全部溶解,则溶液中一定含有Fe3+ |
| C.若金属全部溶解,且产生336 mL气体(标准状况),则b = 0.3 |
| D.当溶液中金属离子只有Fe3+、Cu2+时,则a与b的关系为:b≥80y(1-a/3) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| |
| | 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH |
| Fe3+ | 1.9 | 3.2 |
| Fe2+ | 7.0 | 9.0 |
| Cu2+ | 4.7 | 6.7 |
| 提供的药品:Cl2 浓硫酸 NaOH溶液 CuO Cu | ||
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.b >0.3a | B.b <0.2a | C.0.2a<b <0.3a | D.无法确定 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1∶4 | B.2∶7 |
| C.1∶2 | D.8∶31 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com