
利用下图装置做铝热反应实验。下列说法不正确的是( )
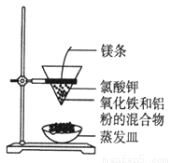
A.该反应的方程式是2Al+Fe2O3  2Fe+Al2O3
2Fe+Al2O3
B.该反应产生高温,发出强光
C.根据铝热反应原理,可以冶炼某些金属
D.若反应中转移3 mol电子,则消耗氧化剂的物质的量是1 mol
 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案 小学学习好帮手系列答案
小学学习好帮手系列答案科目:高中化学 来源:2015-2016学年黑龙江省高一下期末化学试卷(解析版) 题型:选择题
下列各组元素中,属于同一周期的是 ( )
A. H、Na B. N、Cl C. Mg、Si D. F、S
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建省高一下期末化学试卷(解析版) 题型:选择题
同一主族的X、Y、Z三种元素,已知最高价氧化物对应水化物的酸性强弱是H3XO4<H3YO4<H3ZO4,下列推断正确的是( )
A. 原子序数:X<Y<Z
B. 气态氢化物稳定性:XH3<YH3<ZH3
C. 元素的非金属性强弱:X>Y>Z
D. 电子层数:Y>X>Z
查看答案和解析>>
科目:高中化学 来源:2015-2016学年陕西省高一下学期期末化学试卷(解析版) 题型:实验题
葡萄可用于酿酒。
(1)检验葡萄汁含葡萄糖的方法是:向其中加碱调至碱性,再加入新制备的Cu(OH)2,加热,其现象是_______________________________________。
(2)葡萄在酿酒过程中,葡萄糖转化为酒精的过程如下,补充完成下列化学方程式。
C6H12O6(葡萄糖)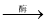 2________+2C2H5OH
2________+2C2H5OH
(3)葡萄酒密封储存过程中生成了有香味的酯,酯也可以通过
化学实验来制备。实验室用下图所示装置制备乙酸乙酯:
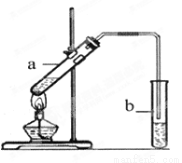
①试管a中生成乙酸乙酯的化学方程式是 ________________________________。
②试管b中盛放的试剂是饱和_________________溶液。
③实验开始时,试管b中的导管不伸入液面下的原因是___________________。
④若分离出试管b中生成的乙酸乙酯,需要用到的仪器是____(填序号)。
a.漏斗 b.分液漏斗 c.长颈漏斗
(4)某有机物的结构简式为HOOC—CH=CHOH。验证该有机物中含有-COOH官能团常采用的方法是 ,产生的现象为 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年陕西省高一下学期期末化学试卷(解析版) 题型:选择题
用NA表示阿伏加德罗常数,下列叙述中正确的是 ( )
A.16g 甲烷中含有的原子数为NA
B.标准状况下,2.24 LCCl4含有的共价键数为0.4NA
C.4.6 g乙醇中含有的C—H键的个数为0.6NA
D.14 g乙烯和丙烯(它是乙烯的同系物,相对分子质量相差14)混合气体中的氢原子数为2NA
查看答案和解析>>
科目:高中化学 来源:2015-2016学年陕西省高一下学期期末化学试卷(解析版) 题型:选择题
下列反应中,属于加成反应的是 ( )
A.
B.
 C.
C.
D.2CH3CH2OH + 2Na → 2CH3CH2ONa + H2↑
查看答案和解析>>
科目:高中化学 来源:2015-2016学年陕西省高一下学期期末化学试卷(解析版) 题型:选择题
下列有关环境保护与绿色化学的叙述不正确的是( )
A.形成酸雨的主要物质是硫的氧化物和氮的氧化物
B.大气污染物主要来自化石燃料燃烧和工业生产过程产生的废气
C.绿色化学的核心就是如何对被污染的环境进行无毒无害的治理
D.水华、赤潮等水体污染主要是由含氮、磷的生活污水任意排放造成的
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省泰安市高二下学期期末化学试卷(解析版) 题型:选择题
某些牙膏中含有茶多酚,茶多酚是茶叶中多酚类物质的总称,是目前尚不能人工合成的纯天然、 多功能、高效能的抗氧化剂和自由基净化剂。其中没食子儿茶素(GC)的结构简式如图所示,下列关于GC的叙述中正确的是( )

A.分子中所有的原子共面
B.1 mol GC与6 mol NaOH恰好完全反应
C.能发生氧化反应、取代反应、消去反应,难发生加成反应
D.遇FeCl3溶液不发生显色反应
查看答案和解析>>
科目:高中化学 来源:2015-2016学年甘肃省通渭县高二下期末理综化学试卷(解析版) 题型:实验题
[化学——选修2化学与技术]高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂=其生产工艺如下:
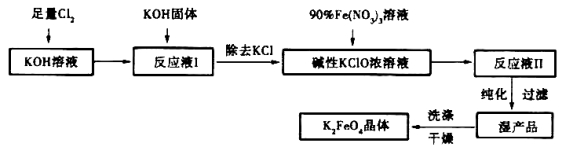
已知:①2KOH + Cl2 = KCl + KClO + H2O(条件:温度较低)
②6KOH + 3C12 = 5KCl + KClO3 +3H2O(条件:温度较高)
③2Fe(NO3)3 +2KC1O + 10KOH = 2K2FeO4 + 6KNO3 +2KCl + 5H2O
回答下列问题:
(1)该生产工艺应在_______(填“温度较高”或“温度较低”)的情况下进行;
(2)写出工业上制取Cl2的化学方程式_________________________;
(3)K2FeO4可作为新型多功能水处理剂的原因____________________;
(4)配制KOH溶液时,是在每100mL水中溶解61.6 g KOH固体(该溶液的密度为1.47 g/mL),它的物质的量浓度为__________
(5)在“反应液I”中加KOH固体的目的是
①_______________,
②______________________________;
(6)从“反应液II”中分离出K2FeO4后,副产品是__________ (写化学式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com