
【题目】下列粒子在相应条件下可大量共存的是( )
A.0.1 mol·L-1FeCl3溶液中:K+、Na+、SO![]() 、AlO
、AlO![]()
B.![]() =1的溶液中:Fe2+、NO
=1的溶液中:Fe2+、NO![]() 、Al3+、Cl-
、Al3+、Cl-
C.0.1 mol·L-1盐酸的澄清透明溶液中:Fe3+、K+、SO![]() 、Br-
、Br-
D.含有0.1 mol·L-1Ca2+的溶液中:Na+、Cu2+、SiO![]() 、NO
、NO![]()
科目:高中化学 来源: 题型:
【题目】利巴韦林是一种成熟的广谱抗病毒药物,临床上证明它对新型冠状病毒有明显抑制作用。其一条合成路线如下:

已知:①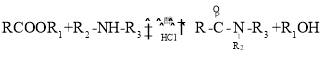 (R代表H或其他基团)
(R代表H或其他基团)
②![]()
回答下列问题:
(1)A的名称为_______________,F中的含氧官能团名称为___________________。
(2)反应I因为反应物用量控制不当,可能会产生副产物,其结构简式为_________,反应I的溶剂使用乙醇而不用甲醇,理由是_______________________________________。
(3)反应II的反应类型为______________。
(4)反应III的反应方程式为_____________________________________________。
(5)G是A的同分异构体,1molG与足量NaHCO3反应生成标准状况下44.8LCO2,符合该条件的G共有_______种。
(6)设计以甘油、乙醇和![]() 为原料制备
为原料制备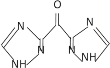 的合成路线_____________(无机试剂任选)。
的合成路线_____________(无机试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丙烯酸甲酯(CH2=CH—COOCH3)是一种重要的有机合成中间体,沸点为80.5℃。某实验小组制取丙烯酸甲酯的装置如图所示:

回答下列问题:
I.丙烯酸甲酯的制备与提纯
步骤1:将10.0g丙烯酸、6.0g甲醇和2mL浓硫酸放置于三颈烧瓶中,连接好冷凝管,用搅拌棒搅拌,水浴加热。
步骤2:充分反应后,冷却,向混合液中加入5%Na2CO3溶液洗至中性,分离出有机相。
步骤3:有机相经无水Na2SO4干燥、过滤、蒸馏,得丙烯酸甲酯。
(1)步骤1装置如图1所示(加热和夹持装置已略去)。三颈烧瓶中进行的可逆反应化学方程式为___,本实验中最容易产生的副产物的结构简式为___。
(2)仪器b的作用为___。
(3)混合液用5%Na2CO3溶液洗涤的目的是___。
(4)实验室配制100g5%Na2CO3溶液需用到的玻璃仪器是___。
(5)关于产品的蒸馏操作(夹持装置未画出)如图2所示。将步骤3(蒸馏)的操作补齐:安装蒸馏装置,加入待蒸馏的物质和沸石,___,弃去前馏分,收集80.5℃的馏分。
II.丙烯酸甲酯含量的测定
步骤1:将油状物质提纯后平均分成5份,取出1份置于锥形瓶中,加入2.5mol·L-1的KOH溶液10.00mL,加热使之完全水解。
步骤2:用酚酞作指示剂,向冷却后的溶液中滴加0.5mol·L-1的HCl溶液,中和过量的KOH,滴到终点时共消耗盐酸20.00mL。
(6)本次酯化反应丙烯酸的转化率为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A是一种常见的单质,B、C为中学常见的化合物,A、B、C均含有元素X,它们有如图所示的转化关系(部分产物及反应条件已略去)。下列判断正确的是( )
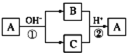
A.X元素可能为AlB.反应①和②互为可逆反应
C.X元素可能为SiD.反应①和②一定为氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“绿色化学”的理想状态是反应物的原子全部转化为目标产物。以下反应不符合绿色化学原则的是( )
A.工业生产环氧乙烷:![]()
B.水煤气合成甲醇:CO + 2H2 CH3OH
CH3OH
C.制取硫酸铜:Cu + 2H2SO4(浓)![]() CuSO4 + SO2↑+ 2H2O
CuSO4 + SO2↑+ 2H2O
D.合成甲基丙烯酸甲酯:CH3C≡CH + CO + CH3OH![]() CH2=C(CH3)COOCH3
CH2=C(CH3)COOCH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在“绿色化学工艺”中,理想状态是反应物中的原子全部转化为欲制得的产物,即原子利用率为100%——即“原子经济性”。下列反应能体现原子经济性的是( )
A. CH3CH3+Br2![]() CH3CH2Br + HBr
CH3CH2Br + HBr
B. CH2=CH2+Br2![]() CH2BrCH2Br
CH2BrCH2Br
C. CH3CH2Br+NaOH![]() CH2=CH2+NaBr+H2O
CH2=CH2+NaBr+H2O
D. CH3CH2OH+CH3COOH![]() H2O+CH3COOCH2CH3
H2O+CH3COOCH2CH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2018年5月美国研究人员成功实现在常温常压下用氮气和水生产氨,原理如下图所示:
下列说法正确的是( )
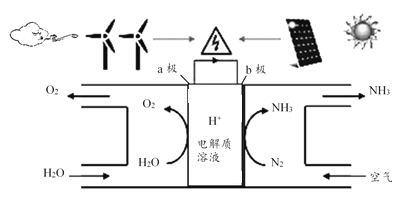
A. 图中能量转化方式只有2种
B. H+向a极区移动
C. b极发生的电极反应为:N2+6H++6e-=2NH3
D. a极上每产生22.4LO2流过电极的电子数一定为4×6.02×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是( )
A.硫酸氢钠与少量氢氧化钡反应:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O
B.硅酸钠溶液与醋酸溶液混合:SiO32-+2H+=H2SiO3↓
C.钠与水反应:Na+2H2O=Na++2OH-+H2↑
D.浓硝酸中加入过量铁粉并加热:Fe+3NO3-+6H+![]() Fe3++3NO2↑+3H2O
Fe3++3NO2↑+3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课题研究小组设计如下图所示装置(电极材料均为铂),该装置可将工业废水中的乙胺(CH3CH2NH2)转化成无毒无害物质。下列分析错误的是
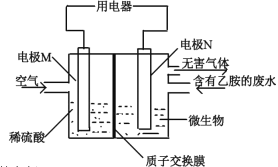
A. 电极N为电池的负极
B. 电池工作时,H+由右极区通过交换膜移动到左极区
C. N电极的电极反应方程式为2CH3CH2NH2+8H2O-30e-=4CO2↑+N2↑+30H+
D. 当空气(假设含氧气20%)的进入量为7.5mol时,可以处理含乙胺9%(质量分数)的废水0.1kg
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com