
| A、NO |
| B、NO2 |
| C、N2 |
| D、N2O3 |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
| A、配制5%NaCl溶液时,将已准确称量的NaCl放入烧杯中并加适量的水搅拌溶解 |
| B、过滤时可用温度计代替玻璃棒 |
| C、分液时球形和梨形分液漏斗的活塞可以放在相同的位置 |
| D、分液操作时,先将分液漏斗中的下层液体放出,然后再将上层液体放出 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 某研究性学习小组对过量炭粉与氧化铁(Fe2O3)反应的气体产物成分进行研究.
某研究性学习小组对过量炭粉与氧化铁(Fe2O3)反应的气体产物成分进行研究.查看答案和解析>>
科目:高中化学 来源: 题型:
| 浓度(mol/L) 时间(min) | NO | N2 | CO2 |
| 0 | 0.100 | 0 | 0 |
| 10 | 0.058 | 0.021 | 0.021 |
| 20 | 0.040 | 0.030 | 0.030 |
| 30 | 0.040 | 0.030 | 0.030 |
| 40 | 0.032 | 0.034 | 0.017 |
| 50 | 0.032 | 0.034 | 0.017 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、所含分子数之比为1:1:1 |
| B、所含氢原子数之比为4:2:3 |
| C、摩尔质量之比为1:1:1 |
| D、质量之比为16:18:17 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、25℃时,2LpH=1的H2SO4溶液中,SO42-数目为0.1NA | ||
| B、300 mL 2 mol/L蔗糖溶液中所含分子数为0.6 NA | ||
C、标准状况下,V L CHCl3含有的碳原子数为
| ||
| D、1 mol OH-参与电解,反应过程中转移的电子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、按系统命名法, 命名为2,3,4-三甲基-5-丙基庚烷 命名为2,3,4-三甲基-5-丙基庚烷 |
| B、邻羟基苯甲醛和对羟基苯甲醛是同分异构体,但邻羟基苯甲醛的熔、沸点比对羟基苯甲醛的熔、沸点高 |
C、塑化剂的种类很多,其中一种塑化剂的结构简式如图所示.可知该塑化剂该塑化剂在人体内会彻底水解产生2种有机物 |
D、用甘氨酸(HN2-CH2-COOH)和丙氨酸( )缩合最多可形成3种二肽 )缩合最多可形成3种二肽 |
查看答案和解析>>
科目:高中化学 来源: 题型:
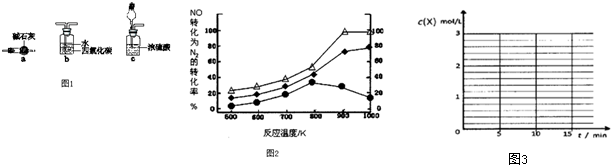
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com