
| A. | 丁烷 | B. | 环丙烷 | C. | 乙烯 | D. | 2-甲基丙烯 |
分析 选项中各物质都是烃,与丁烯具有相同的碳、氢百分含量,则具有相同的最简式CH2,与丁烯既不是同系物又不是同分异构体,则满足分子式与丁烯不同,分子中不含碳碳双键,据此结合选项判断.
解答 解:A、丁烷的分子式为C4H10,与丁烯的最简式不同,故所含C、H元素的百分含量不等,故A错误;
B、环丙烷的最简式为CH2,分子式为C3H6,分子中不含碳碳双键,与丁烯既不是同系物也不是同分异构体,故B正确;
C、乙烯与丁烯互为同系物,故C错误;
D、2-甲基丙烯的分子式为C4H10,最简式为CH2,与丙烯的碳、氢百分含量相同,但结构中含碳碳双键,故和丁烯互为同系物,故D错误.
故选:B.
点评 考查同系物、同分异构体的概念与区别,难度不大,注意概念的内涵与外延.


科目:高中化学 来源: 题型:解答题
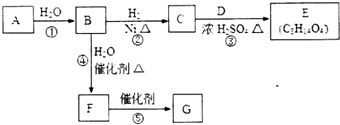 烃的含氧衍生物A是一种重要的有机合成中间体,分子式为C4H2O3,具有五元环结构.由A可以合成有机物E和高分子化合物G,有关物质的转化关系如图所示:
烃的含氧衍生物A是一种重要的有机合成中间体,分子式为C4H2O3,具有五元环结构.由A可以合成有机物E和高分子化合物G,有关物质的转化关系如图所示: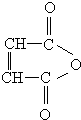 ,B中所含官能团的名称是羧基、碳碳双键;③和⑤的反应类型分别是取代反应、缩聚反应.
,B中所含官能团的名称是羧基、碳碳双键;③和⑤的反应类型分别是取代反应、缩聚反应.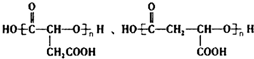 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 图为丙烷的球棍模型: | B. | 某有机物的名称是:2,3二甲基戊烷 | ||
| C. | 乙烯的结构简式CH2CH2 | D. | 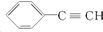 的最简式为:C4H3 的最简式为:C4H3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铜跟稀硝酸反应:3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O | |
| B. | 实验室用大理石和稀盐酸制取CO2:2H++CO32-═CO2↑+H2O | |
| C. | 金属铁与稀硫酸反应:2Fe+6H+═2Fe3++3H2↑ | |
| D. | 钠与水反应:Na+H2O═Na++OH-+H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 高纯度的硅可用于制造计算机芯片 | B. | 自然界中存在大量单质硅 | ||
| C. | 地壳中硅的含量稀少 | D. | 光导纤维的主要成分是Si |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com