
”¾ĢāÄæ”æ³£ĪĀŹ±£¬Ksp[Mg£ØOH£©2]=1.1”Į10©11 £¬ Ksp£ØAgCl£©=1.8”Į10©10 £¬ Ksp£ØAg2CrO4£©=1.9”Į10©12Ksp£ØCH3COOAg£©=2.3”Į10©3 £¬ ĻĀĮŠŠšŹö²»ÕżČ·µÄŹĒ£Ø £©
A.ÅØ¶Č¾łĪŖ0.2 molL©1µÄAgNO3ČÜŅŗŗĶCH3COONaČÜŅŗµČĢå»ż»ģŗĻŅ»¶Ø²śÉśCH3COOAg³Įµķ
B.½«0.001 molL©1µÄAgNO3ČÜŅŗµĪČė0.001 molL©1µÄKClŗĶ0.001 molL©1µÄK2CrO4µÄ»ģŗĻČÜŅŗÖŠ£¬ĻČ²śÉśAg2CrO4³Įµķ
C.c£ØMg2+£©ĪŖ0.11 molL©1µÄČÜŅŗÖŠŅŖ²śÉśMg£ØOH£©2³Įµķ£¬ČÜŅŗµÄpHŅŖæŲÖĘŌŚ9ŅŌÉĻ
D.ŌŚĘäĖūĢõ¼ž²»±äµÄĒéæöĻĀ£¬Ļņ±„ŗĶAgClĖ®ČÜŅŗÖŠ¼ÓČėNaClČÜŅŗ£¬Ksp£ØAgCl£©²»±ä
”¾“š°ø”æB
”¾½āĪö”æ½ā£ŗA£®µČĢå»ż»ģŗĻÅØ¶Č¾łĪŖ0.1molL©1 £¬ c£ØCH3COO©£©”Įc£ØAg+£©=0.01£¾2.3”Į10©3 £¬ Ņ»¶Ø²śÉśCH3COOAg³Įµķ£¬¹ŹAÕżČ·£»
B£®0.001 molL©1µÄKClČÜŅŗÖŠŠĪ³ÉAgCl³ĮµķŹ±£¬ŅųĄė×ÓµÄÅضČĪŖc£ØAg+£©= ![]() =1.8”Į10©7mol/L£¬0.001 molL©1µÄK2CrO4ČÜŅŗÖŠŠĪ³ÉAg2CrO4³ĮµķŹ±£¬c£ØAg+£©=
=1.8”Į10©7mol/L£¬0.001 molL©1µÄK2CrO4ČÜŅŗÖŠŠĪ³ÉAg2CrO4³ĮµķŹ±£¬c£ØAg+£©= ![]() =
= ![]() ”Į10©5mol/L£¬ŌņKClČÜŅŗÖŠŠĪ³ÉAgCl³ĮµķŹ±ŅųĄė×ÓÅØ¶ČŠ”£¬¼“AgClĻČ“ļµ½±„ŗĶ£¬Ó¦ĻČÉś³ÉAgCl³Įµķ£¬¹ŹB“ķĪó£»
”Į10©5mol/L£¬ŌņKClČÜŅŗÖŠŠĪ³ÉAgCl³ĮµķŹ±ŅųĄė×ÓÅØ¶ČŠ”£¬¼“AgClĻČ“ļµ½±„ŗĶ£¬Ó¦ĻČÉś³ÉAgCl³Įµķ£¬¹ŹB“ķĪó£»
C£®Ksp”²Mg£ØOH£©2”³=c£ØMg2+£©”Įc2£ØOH©£©£¬c£ØOH©£©”Ż ![]() =10©5 molL©1 £¬ ČÜŅŗµÄpHÖĮÉŁŅŖæŲÖĘŌŚ9ŅŌÉĻ£¬¹ŹCÕżČ·£»
=10©5 molL©1 £¬ ČÜŅŗµÄpHÖĮÉŁŅŖæŲÖĘŌŚ9ŅŌÉĻ£¬¹ŹCÕżČ·£»
D£®Ksp£ØAgCl£©Ö»ŹÜĪĀ¶ČµÄÓ°Ļģ£¬ÓėÅضČĪŽ¹Ų£¬ĖłŅŌŌŚĘäĖūĢõ¼ž²»±äµÄĒéæöĻĀ£¬Ļņ±„ŗĶAgClĖ®ČÜŅŗÖŠ¼ÓČėNaClČÜŅŗ£¬Ksp£ØAgCl£©²»±ä£¬¹ŹDÕżČ·£»
¹ŹŃ”B£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠø÷×é·“Ó¦ÖŠ¹ŲÓŚÄÜĮæµÄ±Č½ĻÕżČ·µÄŹĒ£Ø £©
¢ŁH2£Øg£©+Cl2£Øg£©=2HCl£Øg£©”÷H1£» ![]() H2£Øg£©+
H2£Øg£©+ ![]() Cl2£Øg£©=HCl £Øg£©”÷H2£»”÷H1£¾”÷H2
Cl2£Øg£©=HCl £Øg£©”÷H2£»”÷H1£¾”÷H2
¢Ś2H2O£Øl£©=2H2£Øg£©+O2£Øg£©”÷H1£» 2Na£Øs£©+2H2O£Øl£©=2NaOH£Øaq£©+H2£Øg£©”÷H2£»”÷H1£¾”÷H2
¢ŪCH3OH£Øg£©+ ![]() O2£Øg£©=CO2£Øg£©+2H2O£Øl£©”÷H1£»CH3OH£Øl£©+
O2£Øg£©=CO2£Øg£©+2H2O£Øl£©”÷H1£»CH3OH£Øl£©+ ![]() O2£Øg£©=CO2£Øg£©+2H2O£Øg£©”÷H2£»”÷H1£¼”÷H2
O2£Øg£©=CO2£Øg£©+2H2O£Øg£©”÷H2£»”÷H1£¼”÷H2
¢Üt”ꏱ£¬ŌŚŅ»¶ØĢõ¼žĻĀ£¬½« 1mol N2ŗĶ 3mol H2 ·Ö±šÖĆÓŚŗćČŻŗĶŗćŃ¹µÄĮ½øöĆܱÕČŻĘ÷ÖŠ£¬“ļµ½Ę½ŗāדĢ¬Ź±·Å³öµÄČČĮæ·Ö±šĪŖ Q1”¢Q2£» Q1£¼Q2 £®
A.¢Ł¢Ū¢Ü
B.¢Ł¢Ś¢Ü
C.¢Ś¢Ū¢Ü
D.¢Ł¢Ū
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĪļÖŹÖŠ£¬²»ŹōÓŚøß·Ö×Ó»ÆŗĻĪļµÄŹĒ
A. ĻĖĪ¬ĖŲB. µ°°×ÖŹC. ÓĶÖ¬D. ĖÜĮĻ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĒā»ÆøĘ£ØCaH2£©¹ĢĢåŹĒµĒɽŌĖ¶ÆŌ±³£ÓƵÄÄÜŌ“Ģį¹©¼Į£®Ä³ŠĖȤŠ”×éÄāŃ”ÓĆČēĻĀ×°ÖĆÖʱøĒā»ÆøĘ£ØŌĄķĪŖ£ŗH2+Ca ![]() CaH2£©£®²éŌÄ׏ĮĻæÉÖŖ£ŗ
CaH2£©£®²éŌÄ׏ĮĻæÉÖŖ£ŗ
¢ŁøĘŅ×ÓėĖ®·“Ӧɜ³É¼īŗĶĘųĢå
¢ŚĒā»ÆøĘŅŖĆÜ·ā±£“ę£¬½Ó“„µ½Ė®¾Ķ·“Ӧɜ³ÉĒāŃõ»ÆøĘŗĶĒāĘų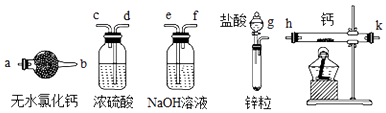
Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©Ēė“ÓŅŌÉĻ×°ÖĆÖŠŃ”ŌńŗĻŹŹµÄ×°ÖĆ½ųŠŠŹµŃ飬Ēė°“ĘųĮ÷·½ĻņĮ¬½ÓĖ³Šņg”ś”ś”ś”ś”ś”śk”śa£ØĢīŅĒĘ÷½ÓæŚµÄ×ÖÄø±ąŗÅ£©£®
£Ø2£©Š“³öøĆŹµŃéÖŠÖʱøĒāĘųµÄĄė×Ó·½³ĢŹ½²¢±źĆ÷µē×Ó×ŖŅʵķ½ĻņŗĶŹżÄæ
£Ø3£©ĪŽĖ®ĀČ»ÆøʵÄ×÷ÓĆŹĒ £®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £©
A.ÓƶĘĪżĢś×ö¹ŽĶ·ŗŠ£¬µ±¶Ę²ćĘĘ»µŗóĪżÄܶŌĢśĢį¹©±£»¤
B.ÓĆĶ×÷µē¼«µē½āĻ”ĮņĖį£¬·¢Éś·“Ó¦£ŗCu+H2SO4 ![]() CuSO4+H2”ü
CuSO4+H2ӟ
C.ijŌµē³ŲµÄµē¼«²ÄĮĻ·Ö±šĪŖMgŗĶAl£¬ŌņMgŅ»¶Ø×öøŗ¼«
D.ijæÉÄ귓ӦɿøßĪĀ¶Č£¬»ī»ÆÄÜ“óµÄ·½Ļņ»Æѧ·“Ó¦ĖŁĀŹŌö“ó³Ģ¶ČŠ”
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŃÖŖ³£ĪĀĻĀKsp£ØAgCl£©=1.6”Į10©10”¢Ksp£ØAgI£©=2.0”Į10©16 £¬ ĻĀĮŠĖµ·ØÖŠÕżČ·µÄŹĒ£Ø £©
A.ŗ¬ÓŠ“óĮæCl©µÄČÜŅŗÖŠæĻ¶Ø²»“ęŌŚAg+
B.AgIŠü×ĒŅŗÖŠ¼ÓČėÉŁĮæKI·ŪÄ©£¬Ę½ŗāAgI£Øs£©?Ag+£Øaq£©+I©£Øaq£©Ļņ×óŅĘ¶Æ£¬ČÜŅŗÖŠĄė×ÓµÄ×ÜÅØ¶Č»į¼õŠ”
C.AgClŠü×ĒŅŗÖŠÖš½„¼ÓČėKI¹ĢĢåÖĮc£ØI©£©= ![]() mol?L©1Ź±£¬AgClæŖŹ¼ĻņAgI³Įµķ×Ŗ»Æ
mol?L©1Ź±£¬AgClæŖŹ¼ĻņAgI³Įµķ×Ŗ»Æ
D.ĻņÅØ¶Č¾łĪŖ0.01 mol?L©1µÄKClŗĶKIµÄ»ģŗĻČÜŅŗÖŠµĪ¼ÓAgNO3ČÜŅŗ£¬µ±Cl©æŖŹ¼³ĮµķŹ±£¬ČÜŅŗÖŠI©µÄÅضČĪŖ1.25”Į10©8 mol?L©1
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĖ«°²Ķ×Ć÷½į¹¹¼ņŹ½ČēĶ¼ĖłŹ¾ ![]() £¬æÉÓĆÓŚ½µµĶŃŖŅŗÖŠµÄµØ¹Ģ“¼£¬øĆĪļÖŹŗĻ³ÉĻßĀ·ČēĶ¼ĖłŹ¾£ŗ
£¬æÉÓĆÓŚ½µµĶŃŖŅŗÖŠµÄµØ¹Ģ“¼£¬øĆĪļÖŹŗĻ³ÉĻßĀ·ČēĶ¼ĖłŹ¾£ŗ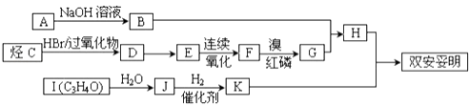
ŅŃÖŖ£ŗ¢ń£® ![]()
¢ņ£®RCHØTCH2 ![]() RCH2CH2Br
RCH2CH2Br
¢ó£®ŅŃÖŖ£ŗCµÄĆܶȏĒĶ¬ĪĀĶ¬Ń¹ĻĀH2ĆܶȵÄ28±¶£¬ĒŅÖ§Į“ÓŠŅ»øö¼×»ł£»IÄÜ·¢ÉśŅų¾µ·“Ó¦ĒŅ1mol I£ØC3H4O£©ÄÜÓė2mol H2·¢Éś¼Ó³É·“Ó¦£»KµÄ½į¹¹¾ßÓŠ¶Ō³ĘŠŌ£®ŹŌ»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©Š“³öĖ«°²Ķ×Ć÷µÄ·Ö×ÓŹ½ £®
£Ø2£©CµÄ½į¹¹¼ņŹ½ĪŖ£»HµÄ½į¹¹¼ņŹ½ĪŖ £®
£Ø3£©·“Ó¦D”śEµÄ·“Ó¦Ģõ¼žŹĒ £¬ ·“Ó¦I”śJµÄĄąŠĶŹĒ £®
£Ø4£©·“Ó¦”°H+K”śĖ«°²Ķ×Ć÷”±µÄ»Æѧ·½³ĢŹ½ĪŖ £®
£Ø5£©·ūŗĻĻĀĮŠ3øöĢõ¼žµÄHµÄĶ¬·ÖŅģ¹¹ĢåÓŠÖÖ£®¢ŁÓėFeCl3ČÜŅŗĻŌÉ«£»¢Ś±½»·ÉĻÖ»ÓŠĮ½øöČ”“ś»ł£»¢Ū1moløĆĪļÖŹ×ī¶ąĻūŗÄ3mol NaOH£¬ĘäÖŠĒāŌ×Ó¹²ÓŠĪåÖÖ²»Ķ¬»·¾³µÄŹĒ£ØŠ“½į¹¹¼ņŹ½£©£®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚŅ»ĆܱÕČŻĘ÷ÖŠÓŠHCHO”¢H2”¢O2 »ģŗĻĘųĢå¹²20gŗĶ×ćĮæµÄNa2O2£¬ÓƵē»š»ØŅżČ¼£¬Ź¹ĘäĶźČ«·“Ó¦£¬Na2O2ŌöÖŲ8g£¬ŌņŌ»ģŗĻĘųĢåÖŠO2µÄÖŹĮæ·ÖŹżŹĒ£Ø£©
A. 40% B. 33% C. 60% D. 36%
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŃÖŖ£ŗO2£Øg£©+2H2£Øg£©=2H2O£Øg£©”÷H=©483.6kJmol©1
C£Øs£¬ŹÆÄ«£©+O2£Øg£©=CO2£Øg£©”÷H=©393.5kJmol©1
CO2£Øg£©+C£Øs£¬ŹÆÄ«£©=2CO£Øg£©”÷H=+172.5kJmol©1
£Ø1£©ĒėŠ“³öCOÓėĖ®ÕōĘū·“Ó¦µÄČČ»Æѧ·½³ĢŹ½
£Ø2£©ŌŚŅ»Ģå»żĪŖ10LµÄĆܱÕČŻĘ÷ÖŠ£¬ĶØČėŅ»¶ØĮæµÄCOŗĶĖ®ÕōĘū£¬ŌŚ850”ꏱ·¢Éś·“Ó¦£¬ČŻĘ÷ÖŠCOŗĶĖ®ÕōĘūÅØ¶Č±ä»ÆČēĶ¼£¬Ōņ0”«4minµÄĘ½¾ł·“Ó¦ĖŁĀŹv£ØCO£©= £¬ Ēė¼ĘĖć“ĖŹ±µÄĘ½ŗā³£ŹżK= £® 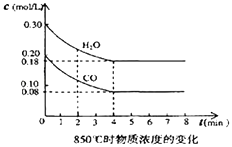
Ź±¼ä/min | CO | H2O | CO2 | H2 |
0 | 0.200 | 0.300 | 0 | 0 |
2 | 0.138 | 0.238 | 0.062 | 0.062 |
3 | c1 | c2 | c3 | c3 |
4 | c1 | c2 | c3 | c3 |
5 | 0.116 | 0.216 | 0.084 | |
6 | 0.096 | 0.266 | 0.104 |
£Ø3£©t”ę£ØøßÓŚ850”ę£©Ź±£¬ŌŚĻąĶ¬ČŻĘ÷ÖŠ·¢ÉśÉĻŹö·“Ó¦£¬ČŻĘ÷ÄŚø÷ĪļÖŹµÄÅØ¶Č±ä»ÆČēÓŅ±ķ£®
¢Ł±ķÖŠ3min”«4minÖ®¼ä·“Ó¦“¦ÓŚ×“Ģ¬£»c1ŹżÖµ0.08mol/L £ØĢī“óÓŚ”¢Š”ÓŚ»ņµČÓŚ£©£®
¢Ś·“Ó¦ŌŚ4min”«5min¼ä£¬Ę½ŗāĻņÄę·½ĻņŅĘ¶Æ£¬æÉÄÜŹĒŅŌĻĀµÄŌŅņ£ØĢī×ÖÄø£©£¬±ķÖŠ5min”«6minÖ®¼äŹżÖµ·¢Éś±ä»Æ£¬æÉÄܵÄŌŅņŹĒ £® £ØĢī×ÖÄø£©
a£®Ōö¼ÓĖ®ÕōĘų b£®½µµĶĪĀ¶Č c£®Ź¹ÓĆ“ß»Æ¼Į d£®Ōö¼ÓĒāĘųÅØ¶Č£®
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com