
【题目】溴乙烷在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物。某同学依据溴乙烷的性质,用如图实验装置(铁架台、酒精灯略)验证取代反应和消去反应的产物,请你一起参与探究。
实验操作Ⅰ:在试管中加入5 mL 1 mol/L NaOH溶液和5 mL溴乙烷,振荡。
实验操作Ⅱ:将试管如图固定后,水浴加热。

(1)用水浴加热而不直接用酒精灯加热的原因是_________;试管口安装一长导管的作用是________________________。
(2)观察到________________现象时,表明溴乙烷与NaOH溶液已完全反应。
(3)鉴定生成物中乙醇的结构,可用的波谱是_____________________。
(4)为证明溴乙烷在NaOH乙醇溶液中发生的是消去反应,在你设计的实验方案中,需要检验的是________________,检验的方法是______________________________说明所用的试剂、简单的实验操作及预测产生的实验现象)。
【答案】 使试管受热均匀 溴乙烷沸点低,减少溴乙烷的损失 试管内溶液静置后不分层 红外光谱、核磁共振氢谱 生成的气体 将生成的气体先通过盛有水的试管,再通入盛有酸性KMnO4溶液的试管,酸性KMnO4溶液褪色(或直接通入溴的四氯化碳溶液)
【解析】分析:(1)溴乙烷沸点低,溴乙烷易挥发,用水浴加热受热均匀,减少溴乙烷的损失。
(2)溴乙烷不溶于水,开始溶液分层,反应后生成的乙醇、溴化钠都溶于水。
(3)根据乙醇分子结构中有三种氢原子选择检测方法。
(4)无论发生取代反应还是消去反应,溶液中都会产生Br-,但生成的有机物不同,故应检验生成的有机物。
(1) 溴乙烷与氢氧化钠反应生成乙醇与溴化钠;溴乙烷沸点低,溴乙烷易挥发,用水浴加热受热均匀,减少溴乙烷的损失;正确答案:使试管受热均匀;溴乙烷沸点低,减少溴乙烷的损失。
(2)溴乙烷不溶于水,开始溶液分层,生成的产物乙醇、溴化钠都易溶于水,当溶液分层消失后,表明溴乙烷与NaOH溶液已完全反应;正确答案:试管内溶液静置后不分层。
(3)乙醇分子结构中有三种氢原子,它们的比为3:2:1,利用核磁共振氢谱可检测,也可用红外光谱检测;正确答案:红外光谱;核磁共振氢谱。
(4)无论发生取代反应还是消去反应,溶液中都会产生Br-,但生成的有机物不同,溴乙烷发生消去反应生成乙烯,所以应检验生成的有机物乙烯:检验乙烯可根据其能使酸性KMnO4溶液或溴水褪色的原理来进行,可以采用洗气的装置,观察到酸性KMnO4溶液褪色且有气泡产生,溴水或溴的四氯化碳溶液褪色即可;正确答案:生成的气体;将生成的气体先通过盛有水的试管,再通入盛有酸性KMnO4溶液的试管,酸性KMnO4溶液褪色(或直接通入溴的四氯化碳溶液)。


 全能练考卷系列答案
全能练考卷系列答案科目:高中化学 来源: 题型:
【题目】在无色透明的溶液中可以大量共存的离子组是()
A.OH-、K+、Al3+、SO42-B.OH-、NH4+、Cl-、Na+
C.Cu2+、NO3-、Cl-、SO42-D.Mg2+、K+、Cl-、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在①蛋白质 ②维生素C ③葡萄糖 ④纤维素四种物质中
(1)不能水解的糖类是_________(填序号,下同);
(2)能水解生成氨基酸的是_________;
(3)在人体中不能直接被消化吸收的是_________;
(4)广泛存在于新鲜蔬菜和水果中,称为抗坏血性酸的是_________,其结构简式为, 则分子式为_________。
则分子式为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是
A. 丙烯分子所有原子均在同一平面上
B. 向溴水中分别通入乙烯加入苯,都能观察到溴水褪色现象,但原因不同
C. C4H4只有![]() 和CH
和CH![]() C—CH=CH2两种同分异构体
C—CH=CH2两种同分异构体
D. 芳香烃![]() 和
和![]() 的一氯代物都只有2种
的一氯代物都只有2种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)曲酸是一种非常有潜力的食品添加剂,经测定曲酸的分子式为C6H6O4,结构简式为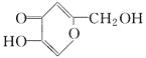 ,其所含有的官能团有(写结构简式) __________。
,其所含有的官能团有(写结构简式) __________。
(2)L­多巴用于帕金森综合症的治疗,其结构简式为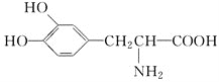 。这种药物的研制是基于获得2000年诺贝尔生理学和医学奖的研究成果。L­多巴分子中所含的官能团的名称是__________。
。这种药物的研制是基于获得2000年诺贝尔生理学和医学奖的研究成果。L­多巴分子中所含的官能团的名称是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下列实验装置和方法进行相应实验,能达到实验目的的是
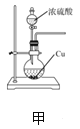



A. 用装置甲制备SO2
B. 用装置乙制备氨气
C. 用装置丙除去粗盐溶液中混有的沙子
D. 用装置丁蒸干溶液获得(NH4)2CO3晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子在溶液中可以大量共存的是( )
A.K+、Na+、HCO3-、OH-B.Fe2+、NO3-、Cl-、Na+
C.Al3+、Mg2+、NO3-、OH-D.H+、K+、Cl-、CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢气是未来最理想的能源之一,科学家最近研制出利用太阳能产生激光,并在二氧化钛(TiO2)表面作用使海水分解得到氢气的新技术:2H2O![]() 2H2↑+O2↑。制得的氢气可用于燃料电池。试回答下列问题:
2H2↑+O2↑。制得的氢气可用于燃料电池。试回答下列问题:
(1)海水分解生成的氢气用于燃料电池时,实现____能转变为____能。水分解时,断裂的化学键为____键,(填极性共价,非极性共价或离子)分解海水的反应属于_____反应(填“放热”或“吸热”)。
(2)某种氢氧燃料电池是用固体金属氧化物陶瓷作电解质,两极上发生的电极反应分别为:A极:2H2+2O2--4e-===2H2O;B极:O2+4e-===2O2-,则A极是电池的____极;电子从该极_____(填“流入”或“流出”)。电流从该电极_____(填“流入”或“流出”)
(3)有人以化学反应:2Zn+O2+4H+===2Zn2++2H2O为基础设计出一种原电池,移入人体内作为心脏起搏器的能源,它们靠人体内血液中溶有一定浓度的O2、H+、Zn2+进行工作。则原电池的负极材料是____,正极上发生反应的电极反应式为____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com