
| A. | 该磁黄铁矿中FexS的x=0.425 | |
| B. | 生成的H2S气体在标准状况下的体积为2.24L | |
| C. | 100mL的盐酸中HCl物质的量浓度为8.5mol/L | |
| D. | 该磁黄铁矿FexS中,Fe2+与Fe3+的物质的量之比为3:1 |
分析 n(S)=$\frac{2.4g}{32g/mol}$=0.075mol,根据转移电子守恒得n(Fe3+)=$\frac{0.075mol×(2-0)}{3-2}$=0.15mol,则n(Fe2+)=0.425mol-0.15mol=0.275mol,所以Fe2+与Fe3+的物质的量之比=0.275mol:0.15mol=11:6,
A.根据转移电子守恒计算n(Fe3+),根据铁原子守恒计算n(Fe2+),根据氢原子守恒及硫单质计算硫原子的物质的量,从而得出x值;有
B.根据氢原子守恒计算硫化氢的体积;
C.根据氯原子守恒计算盐酸的浓度;
D.根据转移电子守恒计算Fe2+与Fe3+的物质的量之比.
解答 解:A.FexS中n(S)=0.075mol+0.425mol=0.5mol,n(Fe)=0.425mol,所以n(Fe):n(S)=0.425mol:0.5mol=0.85,所以x=0.85,故A错误;
B.根据氢原子、氯原子守恒得n(H2S)=$\frac{1}{2}$n(HCl)=n(FeCl2)=0.425mol,V(H2S)=0.425mol×22.4L/mol=9.52L,故B错误;
C.盐酸恰好反应生成FeCl2 0.425mol,根据氯原子守恒得c(HCl)=$\frac{0.425mol×2}{0.1L}$=8.5mol/L,故C正确;
D.根据转移电子守恒得n(Fe3+)=$\frac{0.075mol×(2-0)}{3-2}$=0.15mol,则n(Fe2+)=0.425mol-0.15mol=0.275mol,所以Fe2+与Fe3+的物质的量之比=0.275mol:0.15mol=11:6,故D错误;
故选C.
点评 本题考查了根据氧化还原反应进行计算,根据反应过程中原子守恒、转移电子守恒进行计算,根据氢原子守恒计算硫化氢体积,根据转移电子守恒计算亚铁离子和铁离子的物质的量之比,计算量较大,难度较大.


 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案 品学双优卷系列答案
品学双优卷系列答案 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案科目:高中化学 来源: 题型:选择题
| A. | 电解精炼铜时当阳极溶解32 g铜时,转移电子数大于NA个(Cu-64) | |
| B. | 向酸性FeSO4溶液中滴入少量NaClO溶液,反应的离子方程式为:2Fe2++ClO-+2H+═Cl-+2Fe3++H2O | |
| C. | 向10 mL 0.1mol•L-1 NH4Al(SO4)2溶液中,滴加等浓度Ba(OH)2溶液20 mL,反应的离子方程式为:2Ba2++4OH-+NH4++Al3++2SO42-=2BaSO4↓+Al(OH)3↓+NH3•H2O | |
| D. | 浓盐酸与KClO3混合受热制Cl2:6HCl+KClO3═3Cl2↑+3H2O+KCl,1molKClO3反应转移6 NA个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
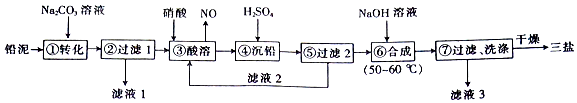
| 化合物 | PbSO4 | PbCO3 |
| 溶解度/g | 1.03×10-4 | 1.81×10-7 |
| Ksp | 1.82×10-8 | 1.46×10-13 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 红陶中体现红色的成分是氧化铁,氧化铁属于碱性氧化物 | |
| B. | 丝绸的主要成分是蛋白质,蛋白质是天然高分子化合物 | |
| C. | 黑火药爆炸时,碳、硫两元素被氧化 | |
| D. | “熬胆矾铁釜,久之亦化为铜”,该过程发生了氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 230Th和232Th的化学性质相同 | B. | Th元素的相对原子质量是231 | ||
| C. | 232Th转化成233U是化学变化 | D. | Th元素的质量数是232 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 液氯较氯水的漂白作用更强 | B. | 液氯与氯水均有酸性 | ||
| C. | 液氯是纯净物,氯水是混合物 | D. | 液氯是无色的,氯水呈黄绿色 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 全部由非金属元素组成的化合物中可含离子键 | |
| B. | H2O中所有原子都满足八电子稳定状态 | |
| C. | 两种元素构成的化合物可以含有非极性共价键 | |
| D. | CH4中所有的电子都参与形成共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 通入澄清的石灰水 | |
| B. | 通入品红溶液 | |
| C. | 依次通过澄清石灰水和酸性KMnO4溶液 | |
| D. | 依次通过小苏打溶液和澄清石灰水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应NH3(g)+HCl(g)?NH4Cl(s)△H<0在任何温度下均能自发进行 | |
| B. | 将AlCl3溶液和NaAlO2溶液分别蒸干后灼烧,所得固体产物均为Al2O3 | |
| C. | 化学平衡向正反应方向移动时,生成物的体积分数一定增加 | |
| D. | 在恒温恒容密闭容器中,反应3A(g)?B(g)+C(g)达到平衡后,再充入一定量的A气体,A的转化率将增大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com