
【题目】下列溶液一定呈酸性的是
A.pH=6.8的溶液
B.常温下,由水电离的OH﹣离子浓度为1×10﹣13mol/L
C.加入酚酞,不显红色的溶液
D.常温下,溶液中的H+离子浓度为5×10﹣7mol/L
 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F六种元素分布在三个不同的短周期,它们的原子序数依次增大,其中B与C为同一周期,D、E、F为同一周期,A与D,C与F分别为同一主族,C元素的原子最外层电子数是次外层电子数的三倍,D是所在周期原子半径最大的元素。又知六种元素所形成的常见单质在常谧常压下有三种是气体,三种是固体。C和D两种元素按个数比l:l形成的化合物M,A和C两种元素按个数比2:1形成化合物N。
请回答下列问题:
(1)写出F在周期表中的位置_______,画出D的离子结构示意图_________。
(2)由A、C两元素可以组成X、Y两种化合物,X在一定条件下可以分解成Y,X的电子式为________。
(3)C与F形成的常见化合物属于_______化合物(填“共价”或“离子”)。
(4)画出B单质的结构式_________。科学家合成出了B元素形成的B5n+电子式![]() ,则n值为__________。
,则n值为__________。
(5)化合物M属于_______化合物(填“共价”或“离子”),如何证明?___________。用电子式表示其形成过程______________。
(6)化合物M和化合物N反应的化学方程式:________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】七铝十二钙是新型的超导材料和发光材料,用白云石(主要含CaCO3和MgCO3)和废Al片制备七铝十二钙的工艺如下:
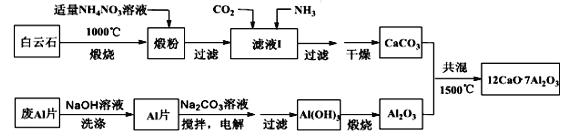
(1)煅粉主要含__________,该工艺中不能用(NH4)2SO4代替NH4NO3,原因是_________。
(2)滤液I中主要的阴离子有_________;若滤液I中仅通入CO2,会生成________,从而导致CaCO3产率降低。
(3)用NaOH溶液可除去废Al片表面的氧化膜,反应的离子方程式为______________。
(4)电解制备Al(OH)3时,电极分别为Al片和石墨,电解总反应方程式为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某温度时CH3COOH的电离平衡常数为K。该温度下向20 mL 0.1 mol·L-1 CH3COOH溶液中逐滴加入0.1 mol·L-1 NaOH溶液,pH变化曲线如图所示(忽略温度),以下叙述正确的是
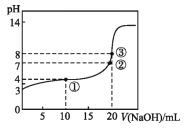
A.根据图中数据可计算出K值约为1×10-5
B.①②③点水的电离程度由大到小的顺序为:②>③>①
C.点①所示溶液中:c(CH3COO-)+c(OH-)=c(CH3COOH)+c(H+)
D.点③时c(CH3COOH)+c(CH3COO-)=0.1 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将Cu投入足量的FeCl3的水溶液中,两者发生反应的化学方程式如下:2FeCl3+Cu2FeCl2+CuCl2
(1)请用双线桥法标出电子转移的方向和数目_______。
(2)当有0.3 mol电子发生转移时,发生反应的Cu的质量为_________。
(3)请将以上反应改写为离子方程式___________________。
(4)配平下列方程式: FeCl2+ H2O2+ HCl— FeCl3+ H2O
______________________
(5)高锰酸钾和氢溴酸溶液可以发生下列反应:2KMnO4+16HBr5Br2+2MnBr2+2KBr+8H2O,若消耗15.8 g氧化剂KMnO4,则被氧化的还原剂的质量是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述错误的是( )
A.任何可逆反应都有一定的限度
B.化学反应达到平衡状态时,正、逆反应速率相等
C.化学反应达到平衡状态与时间的长短无关
D.化学平衡状态是不可改变的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如下图所示,A为银白色金属,A、B、C、D、E、F中均含有同一种元素。常温下G为液态,H为气态。

试回答:
(1)写出化学式:C________,D________,F________,H________。
(2)A与水反应的化学方程式为___________________________________________________。
(3)写出F→E的化学方程式:___________________________________________________。
(4)若向E的饱和溶液中通入足量的H,实验现象为_________________________________。
(5)写出F的一种用途___________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中的一定量混合气体发生反应:xA(g)+yB(g)![]() zC(g)平衡时测得A的浓度为0.50 mol/L,保持温度不变,将容器的容积扩大到原来的二倍,再达平衡时,测得A的浓度降低为0.24 mol/L。下列有关判断错误的是
zC(g)平衡时测得A的浓度为0.50 mol/L,保持温度不变,将容器的容积扩大到原来的二倍,再达平衡时,测得A的浓度降低为0.24 mol/L。下列有关判断错误的是
A.x+y<z B.B的转化率降低
C.平衡向正反应方向移动 D.C的体积分数增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 可用铝罐贮运浓硝酸 B. 弱酸一定不能制备强酸
C. 复分解反应可能也是氧化还原反应 D. 炼铁高炉的高度越髙,尾气中CO的含量越少
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com