
| A. | 元素周期表有七个横行,也是七个周期 | |
| B. | 元素周期表有十八个纵行,也是十八个族 | |
| C. | 表中所含元素种类最少的周期是第一周期 | |
| D. | 表中所含元素种类最多的族是ⅢB族 |
 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案科目:高中化学 来源: 题型:解答题

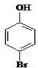 .
. 是化合物 B 的一种同分异构体,用1H 核磁共振谱可以证明该化合物中有2种氢处于不同的化学环境.
是化合物 B 的一种同分异构体,用1H 核磁共振谱可以证明该化合物中有2种氢处于不同的化学环境. .
. .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 .有关该物质的说法正确的是( )
.有关该物质的说法正确的是( )| A. | 它属于芳香烃 | B. | 它是苯的同系物的含氧衍生物 | ||
| C. | 它可发生消去反应 | D. | 它可与NaOH溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | R2+>X2+>Z2+>Y2+ | B. | X2+>R2+>Y2+>Z2+ | C. | Y2+>Z2+>R2+>X2+ | D. | Z2+>X2+>R2+>Y2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 物质的量就是物质的数量 | |
| B. | 1 mol任何物质都含有6.02×1023个原子 | |
| C. | 1 mol水中含有1 mol氢分子和1 mol氧原子 | |
| D. | 1 mol H2分子中含有2 mol H |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蛋白质溶液遇CuSO4后产生的沉淀能重新溶解 | |
| B. | 淀粉水解的最终产物是葡萄糖 | |
| C. | 葡萄糖能发生氧化反应和水解反应 | |
| D. | 植物油不能使溴的四氯化碳溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铝跟氢氧化钠溶液反应 2Al+3H2O+6OH-=2 Al(OH)3+3H2↑ | |
| B. | 铁钉放入硫酸铁溶液中 Fe+Fe3+=2Fe2+ | |
| C. | 铜和稀硝酸反应 Cu+4H++2NO3-=2NO2↑+Cu2++2H2O | |
| D. | 氯气与烧碱溶液反应 Cl2+2OH-=Cl-+ClO-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com