
| A、Ag+、K+、NO3-、S2- |
| B、Fe3+、NH4+、SO42-、NO3- |
| C、Fe2+、Na+、Cl-、ClO- |
| D、H+、Cl-、SO42-、AlO2- |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
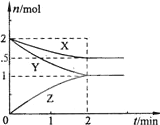 在容器固定的2L密闭容器中,一定条件下,发生如下反应X(g)+2Y(g)?n Z(g),反应过程中各物质的物质的量与时间的关系如图所示,则下列有关叙述中正确的是( )
在容器固定的2L密闭容器中,一定条件下,发生如下反应X(g)+2Y(g)?n Z(g),反应过程中各物质的物质的量与时间的关系如图所示,则下列有关叙述中正确的是( )| A、②③⑤⑥ | B、②④⑤ |
| C、②③④⑥ | D、①③④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、澄清石灰水跟盐酸反应:OH-+H+=H2O |
| B、金属钠跟水反应:Na+2H2O=Na++2OH-+H2↑ |
| C、碳酸钡与醋酸反应:BaCO3+2H+=CO2↑+Ba2++H2O |
| D、碳酸氢钠溶液和氢氧化钠溶液反应:HCO3-+OH-=CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将含硫酸的废液倒入水槽,用水冲入下水道 |
| B、做氢气还原氧化铜实验时,先通氢气再加热 |
| C、配制稀硫酸时,可先在量筒中加一定体积的水,再边搅拌边慢慢加入浓硫酸 |
| D、点燃酒精灯时可以拿燃着的酒精灯引燃另一只酒精灯 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Cu2+、Ag+、NO3-、Cl- |
| B、K+、Fe3+、SO42-、OH- |
| C、Ba2+、CO32-、NO3-、H+ |
| D、Mg2+、Cl-、NO3-、Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在pH=0的溶液中:Na+、Fe2+、Cl-、NO3- |
| B、由水电离出的c(H+)=1×10-14mol?L-1的溶液:K+、NH4+、Cl-、CO32- |
| C、c(H+)<c(OH-)溶液:Na+、K+、SO32-、AlO2- |
| D、某无色透明溶液:Na+、Al3+、SO42-、HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③ | B、③⑤ | C、③④ | D、②⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、3P能级有一个空轨道的基态原子和核外电子的排布为1S22S22p63S23P4的原子 |
| B、2P能级有一个未成对电子的基态原子和价电子排布为2S22p5的原子 |
| C、M层全充满而N层为4S2的原子和核外电子排布为1S22S22p63S23P63d64S2的原子 |
| D、最外层电子数是核外电子总数的1/5的原子和价电子排布为4S24p5 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、N5+与H2S是等电子体 |
| B、N5+中氮氮原子间以共用电子对结合 |
| C、N5AsF6化合物是共价合物 |
| D、N5AsF6是极性分子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com