
【题目】用如图所示的装置进行电解.通电一会儿,发现用NaCl溶液湿润的淀粉KI试纸的C端变为蓝色. 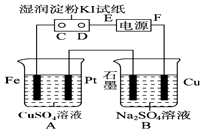
(1)E为电源的极,Fe为极.
(2)A中发生反应的离子方程式为 , B中发生反应的化学方程式为 .
(3)在B中观察到的现象是
(4)若此电源为铅蓄电池,电池总反应式为: Pb+PbO2+4H++2SO42﹣ ![]() PbSO4+2H2O
PbSO4+2H2O
则放电时:正极的电极反应式是;充电时:阴极的电极反应式是;当外电路通过1mol电子时,理论上负极板的质量增加g,此时若要使A池中的溶液复原,应加入g的CuO固体.
【答案】
(1)负;阴
(2)2Cu2++2H2O ![]() 2Cu+4H++O2↑;2Cu+2H2O
2Cu+4H++O2↑;2Cu+2H2O ![]() 2Cu(OH)2+H2↑
2Cu(OH)2+H2↑
(3)铜片溶解,石墨电极上有气体生成,溶液中有蓝色沉淀生成
(4)PbO2+2e﹣+4H++SO42﹣=PbSO4+2H2O; PbSO4+2e﹣=Pb+SO42﹣;40;40
【解析】解:通电一会儿,发现湿润的淀粉KI试纸的C端变为蓝色,说明C端是阳极,则E是负极,F是正极,铁作阴极,铂丝作阳极,电解硫酸铜溶液时,阴极上铜离子放电,阳极上氢氧根离子放电,(1)E为电源的 负极,铁电源负极相连,所以Fe为阴极,
所以答案是:负;阴;(2)A池中为惰性电极电解硫酸铜溶液,反应的离子方程式为:2Cu2++2H2O ![]() 2Cu+4H++O2↑;B中铜为阳极电解硫酸钠溶液,发生反应的化学方程式为:2Cu+2H2O
2Cu+4H++O2↑;B中铜为阳极电解硫酸钠溶液,发生反应的化学方程式为:2Cu+2H2O ![]() 2Cu(OH)2+H2↑,
2Cu(OH)2+H2↑,
所以答案是:2Cu2++2H2O ![]() 2Cu+4H++O2↑;2Cu+2H2O
2Cu+4H++O2↑;2Cu+2H2O ![]() 2Cu(OH)2+H2↑;(3)在B中观察到的现象是铜片溶解,石墨电极上有气体生成,溶液中有蓝色沉淀生成,
2Cu(OH)2+H2↑;(3)在B中观察到的现象是铜片溶解,石墨电极上有气体生成,溶液中有蓝色沉淀生成,
所以答案是:铜片溶解,石墨电极上有气体生成,溶液中有蓝色沉淀生成;(4)电池总反应式为:Pb+PbO2+4H++2SO42﹣2PbSO4+2H2O,负极电解反应为:Pb﹣2e﹣+SO42﹣=PbSO4 ,正极电极反应为:PbO2+2e﹣+4H++2SO42﹣=PbSO4+2H2O;放电时:正极的电极反应式是PbO2+2e﹣+4H++2SO42﹣=PbSO4+2H2O;
当外电路通过1mol电子时,依据电子守恒计算理论上负极板增加质量增为:0.5mol×303g/mol﹣0.5mol×207g/mol=48g,此时若要使A池中的溶液复原,应加入0.5molCuO固体,其质量为:0.5mol×80g/mol=40g,
所以答案是:PbO2+2e﹣+4H++2SO42﹣=PbSO4+2H2O;PbSO4+2e﹣=Pb+SO42﹣;48;40.


 优质课堂快乐成长系列答案
优质课堂快乐成长系列答案科目:高中化学 来源: 题型:
【题目】三氟化硼是平面正三角形,因此是非极性分子,推断三氯甲烷(碳原子位于分子结构中心)的结构和分子的极性情况是( )
A. 四面体,极性分子 B. 平面三角形,非极性分子
C. 正四面体,非极性分子 D. 平面三角形,极性分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原子序数依次增大的A、B、C、D、E、F六种元素。其中A的基态原子有3个不同的能级,各能级中的电子数相等;C的基态原子2p能级上的未成对电子数与A原子的相同;D为它所在周期中原子半径最大的主族元素;E和C位于同一主族,F的原子序数为29。
(1)F基态原子的核外电子排布式为______________________。
(2)在A、B、C三种元素中,第一电离能由小到大的顺序是___________(用元素符号回答)。
(3)元素B的简单气态氢化物的沸点___________(填“高于”或“低于”)元素A的简单气态氢化物的沸点,其主要原因是______________________。
(4)由A、B、C形成的离子CAB与AC2互为等电子体,则CAB的结构式为___________。
(5)由B、C、D三种元素形成的化合物晶体的晶胞如图所示,则该化合物的化学式为___________。

(6)FC在加热条件下容易转化为F2C,从原子结构的角度解释原因______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是一个化学过程的示意图.请回答下列问题: 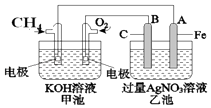
(1)甲池是装置(填“原电池”或“电解池”),B(石墨)电极的名称 是 .
(2)写出电极反应式: 通入CH4的电极;A(Fe)电极 .
(3)甲池中反应的离子方程式为 .
(4)乙池中反应的化学方程式为 .
(5)若乙池溶液体积为500mL,且忽略电解过程中溶液体积的变化,当乙池中 A极的质量增加5.40g时: ①甲池中理论上消耗O2体积为(标准状况下);
②乙池中所得溶液的pH= .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验装置正确且能达到实验目的的是( )
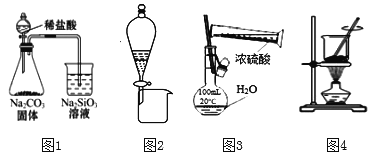
A. 用图1装置证明非金属性Cl>C>Si
B. 利用图2装置,用饱和碳酸钠溶液分离乙醇和乙酸乙酯混合液
C. 图3为配制100 mL一定浓度硫酸溶液
D. 用图4装置灼烧海带
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向20.00mL0.1000molL﹣1的醋酸溶液中逐滴加入0.1000molL﹣1的NaOH溶液,pH随NaOH溶液体积的变化如图所示.下列说法不正确的是( ) 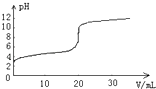
A.在反应过程中始终,c(Na+)+c(H+)=c(CH3COO﹣)+c(OH﹣)
B.pH=4时,c(CH3COO﹣)>c(Na+)>c(H+)>c(OH﹣)
C.pH=6时,c(CH3COO﹣)+c(CH3COOH)=0.1000 molL﹣1
D.pH=7时,消耗NaOH溶液的体积小于20.00mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F均为有机物,其中A 常用来衡量一个国家石油化工发展水平的标志性物质,它们之间有如下转化关系。已知醛基在氧气中易氧化成羧基,请回答下列问题:
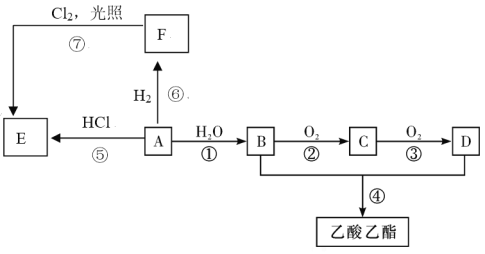
(1)A的分子式是_________,B中官能团的名称_____________。在反应①~④中,属于加成反应的是__________(填序号)。
(2)写出反应②的化学方程式:______________________________________________。
写出反应④的化学方程式:_________________________________________________。
(3)写出与F互为同系物的含5个碳原子的所有同分异构体中一氯代物种类最少的结构简式_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】吲哚昔酚 (idoxifene)可用于治疗骨质疏松症,它的合成路线如 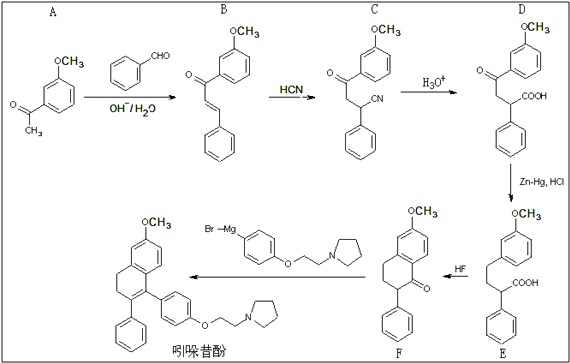
(1)反应类型:B→C;D→E
(2)D中的含氧官能团为(写名称)
(3)满足下列四个条件的A的同分异构体数目有种. ①苯的衍生物,且苯环上只有两个互为对位的取代基;②能发生银镜反应;③与FeCl3溶液作用不显色;④不与氢氧化钠水溶液反应
(4)E→F中还有一种副产物G生成,G与F互为同分异构体,且含有三个六元环,G结构简式为
(5)2,2﹣二甲基戊酸[CH3CH2CH2C(CH3)2COOH]是有机合成中间体,请设计合理的方案以丙酮(CH3COCH3)为唯一有机原料合成2,2﹣二甲基戊酸异丙酯(用合成路线流程图表示,并注明反应条件) 提示:①合成过程中无机试剂任选;②丙酮分子间能发生如图合成路线中A→B的类似反应;③合成路线流程图示例:CH3CH2OH ![]() CH2═CH2
CH2═CH2 ![]() CH2Br﹣CH2Br.
CH2Br﹣CH2Br.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com