
ЁОЬтФПЁПФГгаЛњЛЏКЯЮяAОРюБШЯЃЗЈВтЕУЦфжаКЌЬМЮЊ70.6%ЁЂКЌЧтЮЊ5.9%ЦфгрКЌгабѕЁЃЯжгУЯТСаЗНЗЈВтЖЈИУгаЛњЛЏКЯЮяЕФЯрЖдЗжзгжЪСПКЭЗжзгНсЙЙЁЃ
ЗНЗЈвЛ:гУжЪЦзЗЈЗжЮіЕУжЊAЕФжЪЦзЭМШчЭМЯТЃК
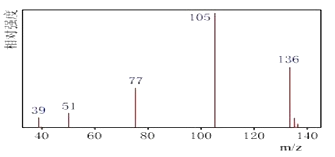
ЗНЗЈЖў: КЫДХЙВеёвЧВтГіAЕФКЫДХЙВеёЧтЦзШчЭМЁЃ
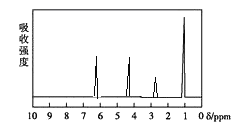
ЗНЗЈШ§: РћгУКьЭтЙтЦзвЧВтЕУAЗжзгЕФКьЭтЙтЦзЃЌШчЯТЭМЁЃ
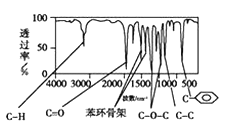
вбжЊЃКAЗжзгжаБНЛЗЩЯжЛгавЛИіШЁДњЛљЃЌЪдЛиД№ЯТСаЮЪЬтЁЃ
ЃЈ1ЃЉAЗжзгЕФЯрЖдЗжзгСПЪЧ_______________ЁЃЦфга____________жжЛЏбЇЛЗОГВЛЭЌЕФЧтдзгЁЃ
ЃЈ2ЃЉAЕФЗжзгЪНЮЊ_______________________ЁЃ
ЃЈ3ЃЉИУгаЛњЮяКЌгаЕФЙйФмЭХЪЧ______________________ЁЃ
ЃЈ4ЃЉAЕФЗжзгжажЛКЌвЛИіМзЛљЕФжБНгвРОнЪЧ________________(ЬюађКХ)ЁЃ
aЃЎAЕФЯрЖдЗжзгжЪСП bЃЎAЕФЗжзгЪН
cЃЎAЕФКЫДХЙВеёЧтЦзЭМ dЃЎAЗжзгЕФКьЭтЙтЦзЭМ
ЃЈ5ЃЉAЕФНсЙЙМђЪНЮЊ_______________________________ЁЃ
ЁОД№АИЁП136 4 C8H8O2 ѕЅРр bc ![]()
ЁОНтЮіЁП
ЃЈ1ЃЉгЩAЕФжЪЦзЭМПЩжЊЃЌAЕФЯрЖдЗжзгСПЮЊ136ЃЌгЩAЕФКЫДХЙВеёЧтЦзЭМПЩжЊЃЌAга4ИіЗхЃЌдђAжага4жжЛЏбЇЛЗОГВЛЭЌЕФЧтдзгЃЌЙЪД№АИЮЊЃК136ЃЌ4ЃЛ
ЃЈ2ЃЉN(C)ЁУN(H)ЁУN(O)=70.6%/12ЁУ5.9%/1ЁУ(1-70.6%-5.9%)/16=4ЁУ4ЁУ1ЃЌдђAЕФЪЕбщЪНЮЊC4H4OЃЌЩшAЕФЗжзгЪНЮЊ(C4H4O)nЃЌгжMr(A)=136ЃЌПЩЕУn=2ЃЌдђAЕФЗжзгЪНЮЊЃКC8H8O2ЃЛ
ЙЪД№АИЮЊЃКAЕФЗжзгЪНЮЊЃКC8H8O2ЃЛ
ЃЈ3ЃЉгЩAЗжзгЕФКьЭтЙтЦзПЩжЊЃЌAКЌгаБНЛЗЃЌеМ6ИіCдзгЃЌЛЙКЌгаC=OЁЂC-O-CЁЂC-CЁЂC-HЃЌЦфжаC=OЁЂC-O-CПЩзщКЯЮЊ![]() ЃЌЫљвдИУЮяжЪЮЊѕЅРрЁЃ
ЃЌЫљвдИУЮяжЪЮЊѕЅРрЁЃ
ЙЪД№АИЮЊЃКѕЅРрЃЛ
ЃЈ4ЃЉНсКЯЩЯЪіЃЈ2ЃЉЕФНтЮіЃЌдйНсКЯAЗжзгЕФКЫДХЙВеёЧтЦзЃЌга4жжЧтдзгЃЌЧвЦфБШР§ЮЊ1ЃК1ЃК1ЃК3ЃЌгжгЩгк-CH3ЩЯЧтдзгЪ§ЮЊ3ЃЌЫљвджЛФмгавЛИі-CH3ЃЌЫљвдAЕФЗжзгжажЛКЌвЛИіМзЛљЕФвРОнЮЊbcЃЌЙЪД№АИЮЊЃКbcЃЛ
(5)гЩAЗжзгЕФКьЭтЙтЦзЭМПЩжЊЃЌAЗжзгжаКЌгавЛИіБНЛЗЃЌКЌгавЛИіѕЅЛљЃЌжЛКЌгавЛИіМзЛљЃЌИљОнвдЩЯЗжЮіПЩжЊЃЌAЕФНсЙЙМђЪНЮЊЃК![]() ЃЌ
ЃЌ
ЙЪД№АИЮЊЃК![]() ЁЃ
ЁЃ


 ЛЦИдаЁзДдЊНтОіЮЪЬтЬьЬьСЗЯЕСаД№АИ
ЛЦИдаЁзДдЊНтОіЮЪЬтЬьЬьСЗЯЕСаД№АИ Ш§ЕувЛВтПьРжжмМЦЛЎЯЕСаД№АИ
Ш§ЕувЛВтПьРжжмМЦЛЎЯЕСаД№АИ
| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПвЛЖЈСПЕФЛьКЯЦјЬхдкУмБеШнЦїжаЗЂЩњЗДгІ m A (g) + n B (g) ![]() p C (g)ДяЕНЦНКтКѓЃЌЮТЖШВЛБфЃЌНЋШнЦїЬхЛ§ЫѕаЁЕНдРДЕФ1/2ЃЌДяЕНЦНКтЪБЃЌCЕФХЈЖШЮЊдРДЕФ1.5БЖЃЌдђЯТСаЫЕЗЈе§ШЗЕФЪЧ
p C (g)ДяЕНЦНКтКѓЃЌЮТЖШВЛБфЃЌНЋШнЦїЬхЛ§ЫѕаЁЕНдРДЕФ1/2ЃЌДяЕНЦНКтЪБЃЌCЕФХЈЖШЮЊдРДЕФ1.5БЖЃЌдђЯТСаЫЕЗЈе§ШЗЕФЪЧ
A. m + n > pB. CЕФЬхЛ§ЗжЪ§діМг
C. ЦНКтЯђе§ЗДгІЗНЯђвЦЖЏD. A ЕФзЊЛЏТЪНЕЕЭ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПРћгУМзЭщгыТШЦјЗЂЩњШЁДњЗДгІЕФИБВњЦЗЩњВњбЮЫсЕФЩшЯыдкЙЄвЕЩЯвбГЩЮЊЯжЪЕЁЃФГЛЏбЇаЫШЄаЁзщФЃФтЩЯЪіЙ§ГЬЃЌЫљЩшМЦЕФзАжУШчЭМЫљЪОЃК
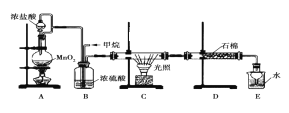
(1)AжажЦШЁCl2ЕФЗДгІЕФЛЏбЇЗНГЬЪНЪЧ_________________________ЁЃ
(2)BзАжУгаШ§жжЙІФмЃКЂйПижЦЦјСїЫйЖШЃЛЂкОљдШЛьКЯЦјЬхЃЛЂл_______________________ЁЃ
(3)DзАжУжаЕФЪЏУоЩЯЮќИНзХГБЪЊЕФKIЃЌЦфзїгУЪЧ________________ЁЃ
(4)EзАжУЕФзїгУЪЧ_______________________ЁЃ
(5)EзАжУжаГ§СЫгабЮЫсЩњГЩЭтЃЌЛЙКЌгагаЛњЮяЃЌДгEжаЗжРыГібЮЫсЕФзюМбЗНЗЈЪЧ______________ЁЃ
(6)НЋ1 mol CH4гыCl2ЗЂЩњШЁДњЗДгІЃЌВтЕУ4жжгаЛњШЁДњВњЮяЕФЮяжЪЕФСПЯрЕШЃЌдђЯћКФЕФТШЦјЕФЮяжЪЕФСПЪЧ_____ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЩшNAЮЊАЂЗќМгЕТТоГЃЪ§ЕФжЕЁЃЯТСаЫЕЗЈе§ШЗЕФЪЧ
A.22.4LCl2ШмгкзуСПЫЎЃЌЫљЕУШмвКжаCl2ЁЂCl-ЁЂHClOКЭClO-ЫФжжЮЂСЃзмЪ§ЮЊNA
B.БъзМзДПіЯТЃЌ38g3H2O2жаКЌга3NAЙВМлМќ
C.ГЃЮТЯТЃЌНЋ5.6gЬњПщЭЖШызуСПХЈЯѕЫсжаЃЌзЊвЦ0.3NAЕчзг
D.БъзМзДПіЯТЃЌ5.6L вЛбѕЛЏЕЊКЭ5.6L бѕЦјЛьКЯКѓЕФЗжзгзмЪ§ЮЊ0.5NA
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПXЁЂYЁЂZЁЂWЮЊЖЬжмЦкдЊЫиЃЌШєWдзгЕФзюЭтВуЕчзгЪ§ЪЧЦфФкВуЕчзгЕФ![]() ЃЌШчЭМЫљЪОЃЌЯТСаЫЕЗЈВЛе§ШЗЕФЪЧ
ЃЌШчЭМЫљЪОЃЌЯТСаЫЕЗЈВЛе§ШЗЕФЪЧ
X | Y | |
Z | W |
A.XдЊЫиЕФЧтЛЏЮяЗжзгМфПЩвдаЮГЩЧтМќ
B.YдЊЫиЕФСНжжЭЌЫивьаЮЬхГЃЮТЯТЖМЪЧЦјЬх
C.вѕРызгАыОЖДгДѓЕНаЁЕФЫГађЮЊX>Y>Z>W
D.зюИпМлбѕЛЏЮяЖдгІЕФЫЎЛЏЮяЕФЫсадЃКW>Z
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПгвЭМЪЧЛЏбЇПЮЭтЛюЖЏаЁзщЩшМЦЕФгУЛЏбЇЕчдДЪЙLEDЕЦЗЂЙтЕФзАжУЪОвтЭМЁЃЯТСагаЙиИУзАжУЕФЫЕЗЈе§ШЗЕФЪЧ( )

A. ЭЦЌЮЊИКМЋЃЌЦфИННќЕФШмвКБфРЖЃЌШмвКжагаCu2ЃЋВњЩњ
B. ШчЙћНЋаПЦЌЛЛГЩЬњЦЌЃЌЕчТЗжаЕФЕчСїЗНЯђНЋИФБф
C. ЦфФмСПзЊЛЏЕФаЮЪНжївЊЪЧЁАЛЏбЇФмЁњЕчФмЁњЙтФмЁБ
D. ШчЙћНЋЯЁСђЫсЛЛГЩФћУЪжЃЌLEDЕЦНЋВЛЛсЗЂЙт
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЂёЁЂФГЮТЖШЪБЃЌдквЛИі 10L ЕФКуШнШнЦїжаЃЌXЁЂYЁЂZ ОљЮЊЦјЬхЃЌШ§жжЮяжЪЕФЮяжЪЕФСПЫцЪБМфЕФБфЛЏЧњЯпШчЭМЫљЪОЁЃИљОнЭМжаЪ§ОнЬюПеЃК
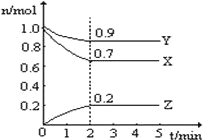
(1)ИУЗДгІЕФЛЏбЇЗНГЬЪНЮЊЃК________________________ЁЃ
(2)ЗДгІПЊЪМжС 2minЃЌвдЦјЬх Z БэЪОЕФЦНОљЗДгІЫйТЪЮЊЃК____________________ЁЃ
(3)НЋ a mol X гы b mol Y ЕФЛьКЯЦјЬхЗЂЩњЩЯЪіЗДгІЃЌЗДгІЕНФГЪБПЬИїЮяжЪЕФСПЧЁКУТњзуЃКn(X)=n(Y)=2n(Z)ЃЌдђдЛьКЯЦјЬхжа aЁУb=________ЁЃ
ЂђЁЂдкКуЮТКуШнЕФУмБеШнЦїжаЃЌЕБЯТСаЮяРэСПВЛдйЗЂЩњБфЛЏЪБЃК
ЂйЛьКЯЦјЬхЕФбЙЧПЃЌЂкЛьКЯЦјЬхЕФУмЖШЃЌЂлЛьКЯЦјЬхЕФзмЮяжЪЕФСПЃЌЂмЛьКЯЦјЬхЕФЦНОљЯрЖдЗжзгжЪСПЃЌЂнЛьКЯЦјЬхЕФбеЩЋЃЌЂоИїЗДгІЮяЛђЩњГЩЮяЕФЗДгІЫйТЪжЎБШЕШгкЛЏбЇМЦСПЪ§жЎБШЁЃ
(1)вЛЖЈФмжЄУї2SO2(g)+O2(g) 2SO3(g)ДяЕНЦНКтзДЬЌЕФЪЧ __________________ЬюађКХЃЌЯТЭЌ)ЁЃ
(2)вЛЖЈФмжЄУї I2(g)+H2(g)2HI(g)ДяЕНЦНКтзДЬЌЕФЪЧ____________________ЁЃ
(3)вЛЖЈФмжЄУї A(s)+2B(g)C(g)+D(g)ДяЕНЦНКтзДЬЌЕФЪЧ_________________(BЁЂCЁЂD ОљЮоЩЋ)ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПгаЛњввХМвіДцдкгкЦЁОЦжаЃЌЪЧОЦРрЕїЯужавЛИіМЋЦфживЊЕФЦЗжжЃЌФГбаОПадбЇЯАаЁзщЮЊШЗЖЈввХМвіЕФНсЙЙЃЌНјааШчЯТЬНОПЁЃ
ВНжшвЛЃКНЋввХМвіеєЦјЭЈЙ§ШШЕФбѕЛЏЭ(ДпЛЏМС)бѕЛЏГЩЖўбѕЛЏЬМКЭЫЎЃЌдйгУзАгаЮоЫЎТШЛЏИЦКЭЙЬЬхЧтбѕЛЏФЦЕФЮќЪеЙмЭъШЋЮќЪеЃЌШчЭМ1ЁЃ2.64 gввХМвіЕФеєЦјбѕЛЏВњЩњ5.28 gЖўбѕЛЏЬМКЭ2.16 gЫЎЁЃ
ВНжшЖўЃКЩ§ЮТЪЙввХМвіЦћЛЏЃЌВтЦфУмЖШЪЧЯрЭЌЬѕМўЯТH2ЕФ44БЖ
ВНжшШ§ЃКгУКЫДХЙВеёвЧВтГіввХМвіЕФКЫДХЙВеёЧтЦзШчЭМ2ЃЌЭМжа4ИіЗхЕФУцЛ§БШЮЊ1ЁУ3ЁУ1ЁУ3ЁЃ
ВНжшЫФЃКРћгУКьЭтЙтЦзвЧВтЕУввХМвіЗжзгЕФКьЭтЙтЦзШчЭМ3ЁЃ



ЃЈ1ЃЉЭМ1зАжУжаСНжЇUаЭЙмВЛФмЛЅЛЛЕФРэгЩЪЧ__________________________ЃЎ
ЃЈ2ЃЉввХМвіЕФФІЖћжЪСПЮЊ____________ЁЃ
ЃЈ3ЃЉввХМвіЕФЗжзгЪНЮЊ____________________ЁЃ
ЃЈ4ЃЉввХМвіЕФНсЙЙМђЪНЮЊ ________________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПХ№УОФрЪЧвЛжжЙЄвЕЗЯСЯЃЌжївЊГЩЗнЪЧMgOЃЈеМ40%ЃЌжЪСПЗжЪ§ЃЉЃЌЛЙгаCaOЁЂMnOЁЂFe2O3ЁЂFeOЁЂAl2O3ЁЂSiO2ЕШдгжЪЃЌвдДЫЮЊдСЯжЦШЁЕФСђЫсУОЃЌПЩгУгкгЁШОЁЂдьжНЁЂвНвЉЕШЙЄвЕЁЃДгХ№УОФржаЬсШЁMgSO47H2OЕФЙЄвеСїГЬШчЯТЃК
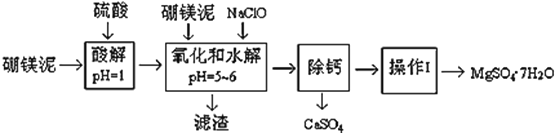
ЃЈ1ЃЉЪЕбщжаашвЊ1 mol/LЕФСђЫс800 mLЃЌШєгУ 98% ЕФХЈСђЫсЃЈІб= 1.84 g/mLЃЉРДХфжЦЃЌСПШЁХЈСђЫсашвЊЪЙгУСПЭВЕФЙцИёЮЊ__________ЃЈЬюаДбЁЯюзжФИЃЉ
AЃЎ10 mL BЃЎ20 mL CЃЎ50 mL DЃЎ100 mL
ЃЈ2ЃЉМгШыЕФNaClOПЩгыMn2+ ЗДгІЃКMn2+ + ClO + H2O = MnO2Ё§+ 2H+ + Cl ЃЌдкИУВНжшжаЛЙгавЛжжРызгвВЛсБЛNaClOбѕЛЏЃЌИУЗДгІЕФРызгЗНГЬЪНЮЊ___________________ЁЃ
ЃЈ3ЃЉТЫдќЕФжївЊГЩЗжГ§КЌгаFe(OH)3ЁЂAl(OH)3ЭтЃЌЛЙКЌга__________ЃЌ___________ЁЃ
ЃЈ4ЃЉдкЁАГ§ИЦЁБЧАЃЌашМьбщТЫвКжаFe3+ ЪЧЗёБЛГ§ОЁЃЌМђЪіМьбщЗНЗЈ___________________ЁЃЃЈаДГіВйзїЁЂЯжЯѓКЭНсТлЃЉ
ЃЈ5ЃЉвбжЊMgSO4ЁЂCaSO4 ЕФШмНтЖШЃЈЕЅЮЛЮЊ g/100 g ЫЎЃЉШчЯТБэЃК
ЮТЖШЃЈЁцЃЉ | 40 | 50 | 60 | 70 |
MgSO4 | 30.9 | 33.4 | 35.6 | 36.9 |
CaSO4 | 0.210 | 0.207 | 0.201 | 0.193 |
ЁАГ§ИЦЁБЪЧНЋMgSO4КЭCaSO4ЛьКЯШмвКжаЕФCaSO4Г§ШЅЃЌИљОнЩЯБэЪ§ОнЃЌМђвЊЫЕУїВйзїВНжш______ЁЃЁАВйзїЂёЁБЪЧНЋТЫвКМЬајеєЗЂХЈЫѕЃЌРфШДНсОЇЃЌ______ЃЌБуЕУЕНСЫMgSO47H2O
ЃЈ6ЃЉЪЕбщжаЬсЙЉЕФХ№УОФрЙВ100 gЃЌЕУЕН MgSO47H2OЮЊ172.2 g ЃЌдђMgSO47H2O ЕФВњТЪЮЊ___ЁЃ
ВщПДД№АИКЭНтЮі>>
АйЖШжТаХ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com