
【题目】过氧化氢是重要的氧化剂、还原剂,它的水溶液又称为双氧水,常用作消毒、杀菌、漂白等。某化学兴趣小组取一定量的过氧化氢溶液,准确测定了过氧化氢的含量,并探究了过氧化氢的性质。
测定过氧化氢的含量请填写下列空白:
(1)移取10.00 m密度为ρ g·mL-1的过氧化氢溶液至250mL______________(填仪器名称)中,加水衡释至刻度,摇匀。移取稀释后的过氧化氢溶液25.00mL至锥形瓶中,加入稀硫酸酸化,用蒸馏水稀释,作被测试样。
(2)用高锰酸钾标准溶液滴定被测试样,己知MnO4-被还原成Mn2+。写出反应的离子方程式:_____________________________
(3)滴定时,将高锰酸钾标准溶液注入_________(填“酸式”或“碱式”)滴定管中。滴定到达终点的现象是_______________________________________。
(4)反复滴定三次,平均耗用c mol·L-1 KMnO4标准溶液V mL,则原过氧化氢溶液中过氧化氢的质量分数为__________________。
(5)若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则测定结果_________(填“偏高”或“偏低”或“不变”)。
【答案】 容量瓶 2MnO42-+5H2O2+6H+=2Mn2++8H2O+5O2↑ 酸式 滴入最后一滴高锰酸钾溶液,溶液呈紫红色,且30秒内不褪色 ![]() 偏高
偏高
【解析】(1)仪器的选用根据题意应该选用容量瓶;(2)残缺方程式配平首先确定缺什么,分析可知缺的是O2,根据电子转移守恒,配平化学方程式为:2MnO42-+5H2O2+6H+=2Mn2++8H2O+5O2↑;(3)由于高锰酸钾标准溶液具有强氧化性,所以只能使用酸式滴定管。滴定到达终点的现象是:滴入最后一滴高锰酸钾溶液,溶液呈浅红色,且30秒内不褪色;(4)根据反应2MnO42-+5H2O2+6H+=2Mn2++8H2O+5O2↑可知:2MnO42-![]() 5H2O2,则过氧化氢的质量分数=
5H2O2,则过氧化氢的质量分数=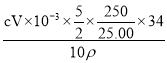 =
=![]() ;(5)若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,有一部分溶液占据了气泡的体积,并没有滴入锥形瓶,则测定结果偏高。
;(5)若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,有一部分溶液占据了气泡的体积,并没有滴入锥形瓶,则测定结果偏高。


科目:高中化学 来源: 题型:
【题目】增强铝的耐腐蚀性,现以铅蓄电池以外电源,以Al作阳极、Pb作阴极,电解稀硫酸,使表面表面的氧化膜增厚。反应原理如下:电池:Pb(s)+PbO2(s)+2H2SO4(aq)═2PbSO4(s)+2H2O(I)
电解池:2Al+3H2O![]() Al2O3+3H2↑
Al2O3+3H2↑
电解过程中,以下判断正确的是
电池 | 电解池 | |
A | H+移向Pb电极 | H+移向Pb电极 |
B | 每消耗3molPb | 生成2molAl2O3 |
C | 正极:PbO2+4H++2e-═Pb2++2H2O | 阳极:2Al+3H2O-6e-═Al2O3+6H+ |
D |
|
|
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 对于1mol·L-1的NH4Cl溶液,升高温度,溶液pH上升
B. 向蒸馏水中滴加浓硫酸,水的离子积常数Kw不变
C. 常温下,能证明乙酸是弱电解质的事实是0.1mol·L-1CH3COONa溶液pH大于7
D. 强电解质溶液的导电能力一定比弱电解质溶液的导电能力强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【2015海南卷】17.(11分)工业上,向500—600℃的铁屑中通入氯气生产无水氯化铁;向炽热铁屑中通入氯化氢生产无水氯化亚铁。现用如图所示的装置模拟上述过程进行试验。

回答下列问题:
(1)制取无水氯化铁的实验中,A中反应的化学方程式为 ,装置B中加入的试剂是 。
(2)制取无水氯化亚铁的实验中,装置A用来制取 。尾气的成分是 。若仍用D的装置进行尾气处理,存在的问题是 、 。
(3)若操作不当,制得的FeCl2 会含有少量FeCl3 ,检验FeCl3常用的试剂是 。欲制得纯净的FeCl2 ,在实验操作中应先 ,再 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1 g氢气燃烧生成液态水放出142.9 kJ热量,该反应的热化学方程式表示正确的是( )
A. 2H2(g)+O2(g)===2H2O(l) ΔH =-142.9 kJ·mol-1
B. H2(g)+![]() O2(g)===H2O(l) ΔH =-285.8 kJ·mol-1
O2(g)===H2O(l) ΔH =-285.8 kJ·mol-1
C. 2H2+O2===2H2O ΔH =-571.6 kJ·mol-1
D. H2(g)+![]() O2(g)===H2O(g) ΔH = -285.8 kJ·mol-1
O2(g)===H2O(g) ΔH = -285.8 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某含有铝电极的原电池工作时,电子从铝电极上流出,下列有关该电池另一电极的材料与电解质溶液的说明中一定错误的是( )
A. 镁、NaOH溶液 B. 铜、浓硝酸
C. 铜、稀硫酸 D. 银、FeCl3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25 ℃时,向20.00 mL浓度均为0.100 0 mol·L-l的三种酸HX、HY、HZ中分别逐滴加入0.100 0 mol·L-l的NaOH溶液,所得溶液的pH随加入NaOH溶液的体积关系如图所示。

下列说法正确的是( )
A. V(NaOH)=0 mL时,三份溶液相比较c(X-)>c(Y-)>c(Z-)
B. 当三份溶液pH均等于7时,反应消耗的n(HX)=n(HY)=n(HZ)
C. 当V(NaOH)=10 mL时,反应后溶液中各离子浓度由大到小的顺序为c(X-)>c(Y-)>c(Z-)>c(Na+),且在HZ溶液中:c(Z-)>c(H+)>c(Na+)>c(OH-)
D. HY与HZ混合溶液中:c(H+)=c(Y-)+c(Z-)+![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列过程或现象与盐类水解无关的是
A.纯碱溶液去油污
B.加热稀醋酸溶液其pH 稍有减小
C.配置FeCl3溶液时,加入少量HCl,以防止溶液浑浊
D.水中加入明矾可以净化水
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com