
【题目】CuCl晶体呈白色,熔点为430℃,沸点为1490℃,见光分解,露置于潮湿空气中易被氧化,难溶于水、稀盐酸、乙醇,易溶于浓盐酸生成H3CuCl4,反应的化学方程式为CuCl(s)+3HCl(aq)H3CuCl4(aq).
(1)实验室用如图1所示装置制取CuCl,反应原理为:
2Cu2++SO2+8Cl﹣+2H2O═2CuCl43﹣+SO![]() +4H+
+4H+
CuCl43﹣(aq)CuCl(s)+3Cl﹣(aq)
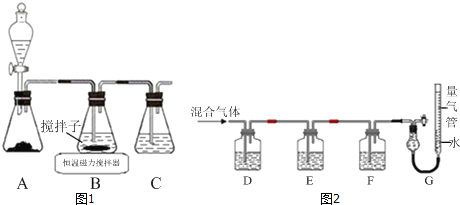
①装置C的作用是_____.
②装置B中反应结束后,取出混合物进行如图所示操作,得到CuCl晶体.
混合物![]()
![]()
![]()
![]()
![]() CuCl晶体
CuCl晶体
操作ⅱ的主要目的是_____
操作ⅳ中最好选用的试剂是_____.
③实验室保存新制CuCl晶体的方法是_____.
④欲提纯某混有铜粉的CuCl晶体,请简述实验方案:_____.
(2)某同学利用如图2所示装置,测定高炉煤气中CO、CO2、N2和O2的百分组成.
已知:
i.CuCl的盐酸溶液能吸收CO形成Cu(CO)ClH2O.
ii.保险粉(Na2S2O4)和KOH的混合溶液能吸收氧气.
①D、F洗气瓶中宜盛放的试剂分别是_____、_____.
②写出保险粉和KOH的混合溶液吸收O2的离子方程式:_____.
【答案】吸收SO2尾气,防止污染空气 促进CuCl析出、防止CuCl被氧化 水、稀盐酸或乙醇 避光、密封保存 将固体溶于浓盐酸后过滤,取滤液加入大量水,过滤、洗涤、干燥 氢氧化钡溶液 CuCl的盐酸溶液 2S2O42﹣+3O2+4OH﹣=4SO42﹣+2H2O
【解析】
试题(1)①A装置制备二氧化硫,B中盛放氯化铜溶液,与二氧化硫反应得到CuCl,C装置盛放氢氧化钠溶液,吸收未反应的二氧化硫尾气,防止污染空气。
②操作ⅱ倒入溶有二氧化硫的溶液,有利于CuCl析出,二氧化硫具有还原性,可以防止CuCl被氧化;CuCl难溶于水、稀盐酸和乙醇,可以用水、稀盐酸或乙醇洗涤,减小因溶解导致的损失。
③由于CuCl见光分解、露置于潮湿空气中易被氧化,应避光、密封保存。
④提纯某混有铜粉的CuCl晶体实验方案是将固体溶于浓盐酸后过滤,取滤液加入大量的水稀释,过滤、洗涤、干燥得到CuCl。
(2)①氢氧化钾会吸收二氧化碳,盐酸挥发出的HCl会影响氧气的吸收、二氧化碳的吸收,所以D中盛放氢氧化钠溶液吸收二氧化碳,E中盛放保险粉(Na2S2O4)和KOH的混合溶液吸收氧气,F中盛放CuCl的盐酸溶液吸收CO,G测定氮气的体积。
②Na2S2O4在碱性条件下吸收氧气,发生氧化还原反应生成硫酸钠与水,反应离子方程式为:2S2O42-+3O2 +4OH-==4SO42-+2H2O。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】在一定温度下,将2molA和2molB两种气体相混合于容积为2L的某密闭容器中,发生如下反应:3A(g)+B(g)![]() xC(g)+2D(g),2min末反应达到平衡状态, 生成了0.8molD,并测得C的浓度为0.4mol/L,请填写下列空白:
xC(g)+2D(g),2min末反应达到平衡状态, 生成了0.8molD,并测得C的浓度为0.4mol/L,请填写下列空白:
(1)x值等于_____________
(2)A的转化率为_______________
(3)生成D的反应速率为_____________
(4)如果增大反应体系的压强,则平衡体系中C的质量分数 _________(填增大、减小或不变)
(5)在此温度下,该化学反应的平衡常数k=__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钛镍形状记忆合金(TiNi)被广泛用于人造卫星和宇宙飞船的天线,在临床医疗领域内也具有广泛的应用。回答下列问题:
(1)写出基态Ti原子的电子排布式:_________,Ni在元素周期表中的位置是_________。
(2)钛镍合金能溶于热的硫酸生成Ti(SO4)2、NiSO4,二者阴离子的立体构型为______,中心原子的轨道杂化类型是_______。
(3)与钛同周期的另一种元素钴(Co)可形成分子式均为Co(NH3)5BrSO4的两种配合物,其中一种化学式为[Co(NH3)5Br]SO4,往其溶液中加BaCl2溶液时,现象是____________;往另一种配合物的溶液中加入BaCl2溶液时,无明显现象,若加入AgNO3溶液时,产生淡黄色沉淀,则第二种配合物的化学式为 _______________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种高分子化合物(Ⅵ)是目前市场上流行的墙面涂料之一,其合成路线如下(反应均在一定条件下进行):
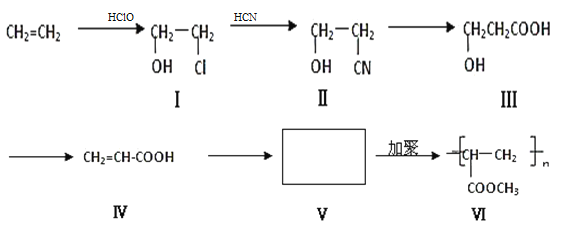
回答下列问题:
(1)化合物I中所含官能团的名称是_____________,由CH2=CH2生成化合物Ⅰ的反应类型是__________。
(2)分别写出合成线路从化合物Ⅰ到Ⅱ、从化合物Ⅳ到Ⅴ的化学方程式_______________________________、_______________________________。
(3)化合物Ⅲ在一定条件下可生成环状化合物C3H4O2,请写出该化合物的结构简式_______________。
(4)下列关于化合物Ⅲ、Ⅳ和Ⅴ的说法中,正确的是_____________。
A.化合物Ⅲ可以发生氧化反应
B.化合物Ⅲ不可以与NaOH溶液反应
C.化合物Ⅳ能与氢气发生加成反应
D.化合物Ⅲ、Ⅳ均可与金属钠反应生成氢气
E.化合物Ⅳ和Ⅴ均可以使溴的四氯化碳溶液褪色
(5)与化合物V具有相同官能团的V的同分异构体有_________种(不包括化合物V本身,且不考虑立体异构)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸亚铁在工农业生产中具有广泛的应用。该物质不稳定,受热易分解产生氧化物,具有较强的还原性。
Ⅰ.某学习小组利用如下装置米探究FeSO4受热分解的产物。
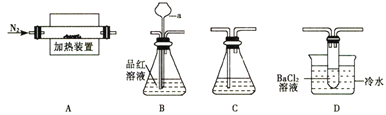
(1)甲组同学利用“A接B接C”的装置来验证产物中含有SO2气体。
①连接好装置后,接下来的操作是____________________。
②仪器a的名称是_______________;其作用是____________________。
(2)乙组同学查阅资料得:硫酸亚铁分解的气体产物中除SO2外还有SO3;SO3的熔点为16.8℃,沸点是46.8℃,溶于水放出大量的然,易形成酸雾。为此设计了“A接D接C”的装置验证产物中含有SO3。
①装置D中的现象是_________________,BaCl2溶液不能用Ba(NO3)2溶液代替的原因是______________________。
②装置A中固体变为经红棕色,结合两组同学的实验,写出硫酸亚铁分解的化学方程式______________________。
③取硫酸亚铁样品18.20g,加热分解至恒重时测得固体质量为11.00g(假设杂质不反应),该硫酸亚铁样品的纯度为__________%(保留小数点后两位,下同),样品中铁元素的质量分数为_____________。
Ⅱ.用硫酸亚铁碱性试纸可检验食品中是否含有CN-,方案如下:

已知:蓝色染料普鲁士蓝的合成方法如下:
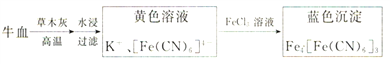
(3)若试纸变蓝则证明食品中含有CN-,基于普鲁士蓝的合成原理,请解释检测时试纸变蓝的原因______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用石墨电极完成下列电解实验
实验一 | 实验二 | |
装置 |
|
|
现象 | a、d处试纸变蓝;b处变红,局部褪色;c处无明显变化 | 两个石墨电极附近有气泡产生;n处有气泡产生…… |
下列对实验现象的解释或推测不合理的是( )
A. a、d处:2H2O+2e-=H2↑+2OH- B. b处:2Cl--2e-=Cl2↑
C. c处发生了反应:Fe-2e-=Fe2+ D. 根据实验一的原理,实验二中m处能析出铜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】连二亚硫酸钠![]() 又称保险粉,是印刷工业中重要的还原剂。某课题小组进行如下实验。
又称保险粉,是印刷工业中重要的还原剂。某课题小组进行如下实验。
Ⅰ.查阅材料
i.连二亚硫酸钠![]() 是一种白色粉末,易溶于水,难溶于乙醇。
是一种白色粉末,易溶于水,难溶于乙醇。
ii.![]()
iii.![]()
II.制备方法
![]() ℃时将甲酸钠和纯碱加入乙醇水溶液中,通入
℃时将甲酸钠和纯碱加入乙醇水溶液中,通入![]() 进行反应,完成其反应方程式:_____
进行反应,完成其反应方程式:_____![]() ______
______ ![]() ______ = ______
______ = ______ ![]() ______
______ ![]() ____,冷却至40℃~45℃,过滤,用 ______ 洗涤,干燥制得
____,冷却至40℃~45℃,过滤,用 ______ 洗涤,干燥制得![]() ;
;
III.![]() 的性质
的性质
(1)![]() 溶液在空气中易被氧化,课题小组测定
溶液在空气中易被氧化,课题小组测定![]()
![]()
![]() 溶液在空气中pH变化如图:
溶液在空气中pH变化如图:![]() 段主要生成
段主要生成![]() ,根据pH变化图,
,根据pH变化图,![]() 的电离平衡 ______ 水解平衡
的电离平衡 ______ 水解平衡![]() 填“
填“![]() ”或“
”或“![]() ”
”![]() ,课题小组推测
,课题小组推测![]() 溶液在空气中易被氧化,
溶液在空气中易被氧化,![]() 发生离子反应方程式为 ______
发生离子反应方程式为 ______ ![]() 时溶液中主要阴离子符号是 ______ 。
时溶液中主要阴离子符号是 ______ 。
(2)隔绝空气加热![]() 固体完全分解得到固体产物
固体完全分解得到固体产物![]() 、
、![]() 和气体为 ______
和气体为 ______ ![]() 填化学式
填化学式![]() 请你设计实验验证产物有
请你设计实验验证产物有![]() 存在,完成下表中内容.
存在,完成下表中内容.![]() 供选择的试剂:稀盐酸、稀硝酸、
供选择的试剂:稀盐酸、稀硝酸、![]() 溶液、
溶液、![]() 溶液
溶液![]()
实验步骤 | 预期的实验现象和结论 |
________ | ________ |

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯气是一种重要的化工原料。
(1)标准状况下,22.4L Cl2的物质的量为________mol。
(2)实验室制取Cl2的化学方程式为 ________________________。
(3)收集Cl2应使用 _________ 法,要得到干燥的Cl2可选用 _______ 做干燥剂。
(4)写出实验室制取漂白液的反应的离子方程式 ______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验设计能够成功的是( )
A.检验亚硫酸钠试样是否变质
试样![]() 白色沉淀
白色沉淀![]() 沉淀不溶解→说明试样已变质
沉淀不溶解→说明试样已变质
B.除去粗盐中含有的硫酸钙杂质
粗盐![]()
![]()
![]() 精盐
精盐
C.检验某溶液中是否含有Fe2+
试样![]() 溶液颜色无变化
溶液颜色无变化![]() 溶液变红色→溶液中含有Fe2+
溶液变红色→溶液中含有Fe2+
D.证明酸性条件H2O2的氧化性比I2强
NaI溶液![]() 溶液变紫色→氧化性:H2O2>I2
溶液变紫色→氧化性:H2O2>I2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com