
【题目】硫、氮、碳的氧化物都会引起环境问题,越来越引起人们的重视,如图1是氮元素的各种价态与物质类别的对应关系
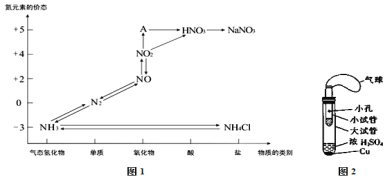
(1)根据A对应的化合价和物质类别,A为 (写分子式),从氦元素的化合价能否发生变化的角度判断,图1中既有氧化性又有还原性的化合物是 ;
(2)浓、稀硝酸的性质相似又有差别,若要除去铁制品表面的铜镀层应选择,反应的化学方程式为 ;
(3)某同学设计了如图2所示的套管实验装置(部分装置未画出)来制备SO2,并利用实验现象来检验其还原性,制备SO2时选用的试剂为Cu和浓H2SO4,回答下列问题.
①写出制取SO2的化学方程式 ;
②该同学利用实验现象来检验SO2的还原性,则选用的试剂为 ;
A 双氧水(H2O2) B品红溶液 C 酸性高猛酸钾溶液
(4)工业上把海水先进行氧化,再吸收溴,达到富集溴的目的.吸收工艺常用的方法是用热空气吹出Br2,用SO2吸收Br2,取吸收后的溶液,向其中加入氯化钠溶液有白色沉淀析出,写出SO2吸收Br2反应的化学方程式 。
【答案】(1)N2O5;NO、NO2;
(2)Cu+4HNO3(浓)![]() Cu(NO3)2+2NO2↑+2H2O;
Cu(NO3)2+2NO2↑+2H2O;
(3)Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O;C
CuSO4+SO2↑+2H2O;C
(4)SO2+Br2+2H2O=H2SO4+2HBr.
【解析】(1)由图可知,A属于氧化物,且氮元素的化合价为+5,因此A为N2O5;根据“高价只具氧化性,低价只具还原性,中间价态两性全”可知,氮元素处于中间价态时即具有氧化性又具有还原性,因此答案是NO、NO2;(2)若要除去铁制品表面的铜镀层应选择浓硝酸,原因是铜和浓硝酸反应,而铁会发生钝化,因此可以在不腐蚀铁制品的前提下,将铜镀层溶解,方程式为Cu+4HNO3(浓)![]() Cu(NO3)2+2NO2↑+2H2O;(3)①Cu与浓H2SO4在加热的条件下发生反应生成SO2,方程式为Cu+2H2SO4(浓)
Cu(NO3)2+2NO2↑+2H2O;(3)①Cu与浓H2SO4在加热的条件下发生反应生成SO2,方程式为Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O;②该同学利用实验现象来检验SO2的还原性,应该选用酸性高锰酸钾,现象是高锰酸钾溶液褪色;(4)SO2吸收Br2发生氧化还原反应,方程式为SO2+Br2+2H2O=H2SO4+2HBr。
CuSO4+SO2↑+2H2O;②该同学利用实验现象来检验SO2的还原性,应该选用酸性高锰酸钾,现象是高锰酸钾溶液褪色;(4)SO2吸收Br2发生氧化还原反应,方程式为SO2+Br2+2H2O=H2SO4+2HBr。


 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列有关叙述正确的是( )
A.28 g乙烯和28g丙烯中均含有6NA对共用电子对
B.在熔融状态下,l mol NaHSO4完全电离出的阳离子数目为2NA
C.标准状况下,NA个SO2分子和NA个SO3分子的体积相同
D.1 mol过氧化钠中含2NA个阴离子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组中的反应,属于同一反应类型的是
A.由溴丙烷水解制丙醇;由丙烯与水反应制丙醇
B.由甲苯硝化制对硝基甲苯;由甲苯氧化制苯甲酸
C.由氯代环己烷消去制环己烯;由丙烯加溴制![]() 二溴丙烷
二溴丙烷
D.由乙酸和乙醇制乙酸乙酯;由苯甲酸乙酯水解制苯甲酸和乙醇
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫代硫酸钠溶液与稀硫酸反应的化学方程式为Na2S2O3+H2SO4==Na2SO4+SO2↑+S↓+H2O,下列各组实验中最先出现浑浊的是( )
选 项 | 反应温度/℃ | Na2S2O3溶液 | 稀H2SO4 | H2O | ||
V/mL | c/mol·L-1 | V/mL | c/mol·L-1 | V/mL | ||
A | 25 | 5 | 0.1 | 10 | 0.1 | 5 |
B | 25 | 5 | 0.2 | 5 | 0.2 | 10 |
C | 35 | 5 | 0.1 | 10 | 0.1 | 5 |
D | 35 | 5 | 0.2 | 5 | 0.2 | 10 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ca(H2PO2)2(次磷酸钙,一元中强酸H3PO2的钙盐)是一种白色结晶粉末,溶于水(常温时,溶解度16.7g/100g水),其水溶液呈现弱酸性。可用作医药、抗氧化剂以及制备次磷酸钠等。由白磷(P4)与石灰乳制备Ca(H2PO2)2的实验步骤如下:

步骤1.在三口烧瓶中加入白磷和石灰乳,先通入N2,然后在约98°C下充分搅拌1h,同时收集产生的PH3。
步骤2.将反应液静置、过滤。
步骤3.向滤液中通入适量CO2,再过滤。
步骤4.用次磷酸溶液调节步骤3滤液的pH,浓缩、冷却结晶、干燥得次磷酸钙。
(1)步骤1先通入N2的目的是 ;搅拌的目的是 。
(2)步骤1石灰乳与 P4(白磷)发生反应的化学方程式为 ;步骤2过滤所得滤渣成分为 。
(3)步骤3的目的是 。
(4)请补充完整由产品进一步制备NaH2PO2·H2O的实验方案:取产品次磷酸钙加入烧杯中,加适量的水溶解, ,干燥得到NaH2PO2·H2O。(已知:在常压下,加热蒸发次磷酸钠溶液会发生爆炸,100℃时NaH2PO2·H2O的溶解度为667g/100g水)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从含铜废料(如:覆铜板、印刷线路板及铅冰铜等)中提取铜,既可提高资源的利用率又可减少重金属污染。
(1)废覆铜板(Cu和Sn组成)可用CuSO4和H2SO4混合溶液作电解质溶液,直接电解回收精铜,阳极上发生的电极反应为 。
(2)废印刷线路板中的铜常用含盐酸的FeCl3溶液或H2O2-HCl- NaCl混合溶液浸取回收。
①用FeCl3溶液浸取铜时发生反应的离子方程式为 ;若加盐酸不足,反应一段时间后线路板表面有红褐色沉淀,产生红褐色沉淀的原因是 。
②将粉碎后的废印刷线路板放入三口烧瓶中,分别加入由0.3mol·L-1盐酸、0.5mol·L-1NaCl及不同浓度的H2O2组成的混合溶液,在温度、搅拌速率及固液比等均相同时,铜的浸取率随H2O2的浓度和时间的变化如图-1所示。当c(H2O2)= 0 mol·L-1时,也有少量的铜被浸出,其原因是 。
③用H2O2-HCl- NaCl混合溶液浸取时,其浸取过程包括:
(Ⅰ)Cu+H2O2+2H+=Cu2++2H2O
(Ⅱ)Cu2++Cu![]() 2Cu+
2Cu+
(Ⅲ)Cu++nCl-![]() CuCln(n-1)-
CuCln(n-1)-
(Ⅳ)2CuCln(n-1)-+2H++H2O2=2Cu2++2H2O+2nCl-
其他条件相同时,增大下列离子浓度可以加速Cu从废电路板中浸出的是 (填序号)。
a.Na+ b.Cu2+ c.Cl- d.OH-

(3)铅冰铜(PbS、Cu2S及FeS的混合物)可用HCl-H2O2混合溶液浸取。
①Cu2S被HCl-H2O2混合溶液浸取得到硫酸铜和氯化铜溶液的化学方程式为 。
②若由H2SO4代替HCl-H2O2中的HCl,其他条件相同,铜的浸取率随硫酸浓度的变化如图-2所示。当H2SO4浓度大于3.1mol·L-1时,硫酸浓度越大,铜的浸取率反而越小,其原因可能是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是病人输液用的葡萄糖(分子式为C6H12O6)注射液的标签上的部分内容。据标签所提供的信息,以下说法错误的是 ( )

A. 该注射液中葡萄糖的质量分数是5%
B. 葡萄糖的摩尔质量为180g·mol-1
C. 该注射液的密度约为1g·mL-1
D. 该注射液中葡萄糖的物质的量浓度约为0.014 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应∶2NO2![]() 2NO+O2在密闭容器中反应,达到平衡状态的标志是
2NO+O2在密闭容器中反应,达到平衡状态的标志是
①单位时间内生成n mol O2的同时生成2n mol NO2 ②单位时间内生成n mol O2 的同时,生成2n mol NO ③用NO2、NO、O2 的物质的量浓度变化表示的反应速率的比为2 : 2 : 1的状态 ④混合气体的颜色不再改变的状态 ⑤混合气体的密度不再改变的状态 ⑥ 混合气体的平均相对分子质量不再改变的状态
A.①④⑥ B.②③⑤ C.①③④ D.①②③④⑤⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com