
| A. | ①④⑤ | B. | ③④⑤ | C. | ①③④ | D. | ①②③④⑤ |
分析 对于N2O4(g)?2NO2(g)(正反应为吸热反应),反应物、生成物都只有一种,加入反应物或生成物,都相当于增大压强,平衡逆向移动,正反应为吸热反应,升高温度,平衡正向移动,以此解答该题.
解答 解:①加压时(体积变小),浓度增大,将使正反应速率增大,故正确;
②保持体积不变,加入少许NO2,平衡逆向移动,反应物浓度增大,将使正反应增大,故错误;
③保持体积不变,加入少许N2O4,平衡正向移动,二氧化氮的浓度增大,再达到平衡时颜色变深,故正确;
④保持体积不变,升高温度,平衡正向移动,再达平衡时颜色变深,故正确;
⑤升高温度,正反应速率增大,故错误.
故选C.
点评 本题考查化学平衡、反应速率的影响因素,把握温度、浓度、压强对反应速率及平衡的影响为解答的关键,侧重分析与应用能力的考查,题目难度不大.


 一课一练课时达标系列答案
一课一练课时达标系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用酒精灯外焰加热铝箔,铝箔熔化但不滴落,说明Al2O3的熔点比Al的熔点高 | |
| B. | 锅炉水垢CaSO4可用Na2CO3溶液浸泡,再用酸溶解去除,说明Ksp:CaCO3>CaSO4 | |
| C. | 用酸性KMnO4溶液验证草酸的还原性 | |
| D. | 向滴有KSCN的FeCl3溶液中加入NaOH溶液以研究反应物浓度对化学平衡的影响 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 实验 序号 | 浓度 时间 温度 | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 1 | 800 | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | c1 | 0.50 |
| 2 | 800 | 1.0 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | T3 | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 卤水点豆腐、明矾净水的原理都是破坏胶体的介稳性 | |
| B. | 铁、铝、铜制容器放置空气中都能在表面形成致密氧化物 | |
| C. | 单晶Ge是半导体,可以作为光电转换材料用于太阳能电池 | |
| D. | 检测酒后驾车者呼出气中的乙醇属于化学检测方法 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
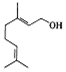
| A. | 分子中含有两种官能团 | |
| B. | lmol该物质与lmolHBr发生加成反应的产物共有5种(不考虑立体异构) | |
| C. | 使溴的四氯化碳溶液和酸性高锰酸钾溶液褪色的原理不同 | |
| D. | 香天竺葵醇能发生加聚反应和氧化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
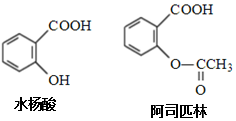
| A. | 阿司匹林分子中存在碳碳双键和碳氧双键 | |
| B. | 阿司匹林的分子式为C9H10O4,能与NaHCO3反应 | |
| C. | 水杨酸可以发生取代反应和加成反应 | |
| D. | 水杨酸的同分异构体中,含有羧基和羟基的只有2种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属钾保存在乙醇中 | |
| B. | 常温下浓硫酸可存放在铁质容器中 | |
| C. | NaOH溶液保存在玻璃塞的试剂瓶中 | |
| D. | FeCl3溶液中加入少量还原铁粉存放 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com