
| A.Q1=Q2=Q3 | B.Q2>Q1>Q3 | C.Q2>Q3>Q1 | D.Q2=Q3>Q1 |
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| A.热裂解形成燃油 | B.露天焚烧 |
| C.作为有机复合建筑材料的原料 | D.直接填埋 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.-44.2kJ·mol-1 | B.+44.2kJ·mol-1 | C.-330kJ·mol-1 | D.+330kJ·mol-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.2ΔH2-ΔH1 | B.2ΔH1-ΔH2 | C.ΔH1-ΔH2 | D.ΔH2-ΔH1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
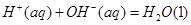
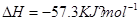
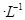 的氢氟酸与0.1mol/L
的氢氟酸与0.1mol/L查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.a<c<0 | B.b>d>0 | C.2a=b<0 | D.2c=d>0 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.2H2(气)+O2(气)=2H2O(气) △H1 2H2(气)+O2(气)=2H2O(液)△H2 |
| B.S(气)+O2(气)=SO2(气)△H1 S(固)+O2(气)=SO2(气)△H2 |
| C.C(固)+1/2O2 (气)=CO(气)△H1C(固)+O2 (气)=CO2(气)△H2 |
| D.H2(气)+Cl2(气)=2HCl(气) △H11/2H2(气) +1/2Cl2(气)=HCl(气)△H2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.S(s)在O2(g)中燃烧的反应是放热反应 |
| B.S(g) + O2(g)= SO2(g);△H=bkJ·mol-1,则a<b |
| C.1mol SO2(g)所具有的能量低于1mol S(s)与1mol O2(g)所具有的能量之和 |
| D.16克固体硫在空气中充分燃烧,可放出148.6kJ的热量 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com