
| ���� |
 �����������������գ��й������б����£�
�����������������գ��й������б����£�
| 57.5ml��0.8g/ml |
| 46g/mol |
| 52mL��1.4g/ml |
| 109g/mol |
| 57.5ml��0.8g/ml |
| 46g/mol |
| 52mL��1.4g/ml |
| 109g/mol |
| 0.668mol |
| 1mol |


 ״Ԫ����ϵ�д�
״Ԫ����ϵ�д� ͬ������ϵ�д�
ͬ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Cl2 |
| B��H2S |
| C��SO2 |
| D��CO2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�������£���0.01 mol/L NHHSO��Һ�еμ�NaOH��Һ�����ԣ�c��Na+����c��SO42-����c��NH4+����c��OH-��=c��H+�� |
| B��0.1 mol/L NaHCO3��Һ��c��Na+����c��OH-����c��HCO3-����c��H+�� |
| C��Na2CO3��Һ��c��OH-��-c��H+��=c��HCO3-��+c��H2CO3�� |
| D��25��ʱ��Ũ�Ⱦ�Ϊ0.1 mol/L��CH3COOH��CH3COONa�����Һ��pH=4.75��c��CH3COO-��+c��OH-����c��CH3COOH��+c��H+�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A��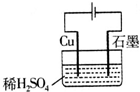 ��ͼ��ʾͨ��һ��ʱ���ʯī�缫�ϻ���ͭ���� |
| B����ԭ��صĸ����͵��ص������϶�����������Ӧ |
| C����⾫��ͭʱ��ͬһʱ���������ܽ�ͭ����������������ͭ������С |
| D���ö��Ե缫���Na2SO4��Һ������������������ʵ���֮��Ϊ2��1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����Mg�� HC03��2��Һ�м��������NaOH��Һ��Mg2++2 HC03-+20H-�TMgC03��+C032-+2H20 |
| B����NH4 Al�� S04��2��Һ�е���Ba�� OH��2��ҺʹSO42-��Ӧ��ȫ��2Ba2++40H-ʮAl3++2 SO42-�T2BaS04��+Al02-+2H20 |
| C���㹻��C02ͨ�뱥��̼������Һ�У�C02+CO32-+H20=2 HC03- |
| D����Fe�� N03��2��Һ�м���ϡ���3Fe2++4H++N03-�T3Fe3++NO��+2H20 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��HCO3-��ˮ�ⷽ��ʽ�ɱ�ʾΪ��HCO3-+H2O?H3O++CO32- |
| B����NaHCO3��Һ�м�������ij���ʯ��ˮ�����ְ�ɫ������2HCO3-+Ca2++2OH-�TCaCO3��+CO32-+2H2O |
| C����NaAlO2��Һ��ͨ�����CO2��Al��OH��3��2AlO2-+CO2+3H2O=2Al��OH��3��+CO32- |
| D����16.8g ����Ͷ��100mL 4.0mol/L��HNO3��Һ�У���ԭ����ֻ��NO��3Fe+8 H++2NO3-=3Fe2++2NO��+4H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| 1 |
| 3 |
| 2 |
| 3 |
| �¶�/�� | 1000 | 1150 | 1300 |
| ƽ�ⳣ�� | 4.0 | 3.7 | 3.5 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com