
已知在一定条件下2SO2(g)+O2(g)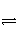
 2SO3(g) ΔH=-Q kJ·mol-1。向一密闭容器中加入2 mol SO2和1 mol O2,达平衡时SO2的转化率为90%,放出的热量为Q1;向另一相同容器中加入2 mol SO3,在相同条件下,达平衡时吸收的热量为Q2,则下列关系中正确的是( )
2SO3(g) ΔH=-Q kJ·mol-1。向一密闭容器中加入2 mol SO2和1 mol O2,达平衡时SO2的转化率为90%,放出的热量为Q1;向另一相同容器中加入2 mol SO3,在相同条件下,达平衡时吸收的热量为Q2,则下列关系中正确的是( )
A.Q>Q1>Q2 B.Q1>Q2>Q C.Q1>Q>Q2 D.Q1=Q2>Q
 小学期末标准试卷系列答案
小学期末标准试卷系列答案科目:高中化学 来源: 题型:
有时候,将氧化还原反应方程式拆开写成两个“半反应”。下面是一个“半反应”式:
___MnO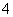 +___H++__e-—___Mn2++__H2O 。该反应方程式的配平化学计量数是( )
+___H++__e-—___Mn2++__H2O 。该反应方程式的配平化学计量数是( )
A.1,8,4,1,4 B.2,16,5,2,8 C.1,6,5,1,3 D.1,8,5,1,4
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组离子在指定溶液中,能大量共存的是( )
①无色溶液中:K+、Cl-、Ca2+、CO32-、SO42-、NO3-
②pH=11的溶液中:CO32-、Na+、[Al(OH)4]-、NO3-、S2-、SO32-
③水电离的[H+]=1×10-12 mol·L-1的溶液中:Cl-、CO32-、NO3-、NH4+、SO32-
④加入Mg能放出H2的溶液中:Mg2+、NH4+、Cl-、K+、SO42-
⑤使石蕊变红的溶液中:Fe2+、MnO4-、NO3-、Na+、SO42-
⑥中性溶液中:Fe3+、Al3+、NO3-、I-、Cl-、S2-
A.①②⑤ B.①③⑥ C.②④ D.①②④
查看答案和解析>>
科目:高中化学 来源: 题型:
在容积为1 L的密闭容器中,加入5 mol A物质,在一定条件下同时发生下列两个反应:(1)2A(g)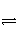
 2B(g)+C(g);(2)A(g)
2B(g)+C(g);(2)A(g)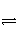
 C(g)+D(g)。当达到平衡时,测得[A]=2.5 mol·L-1,[C]=2.0 mol·L-1。则下列说法中正确的是( )
C(g)+D(g)。当达到平衡时,测得[A]=2.5 mol·L-1,[C]=2.0 mol·L-1。则下列说法中正确的是( )
A.达到平衡时A的总转化率为40%
B.达到平衡时[B]为1.0 mol·L-1
C.达到平衡时[B]=2[D]
D.达到平衡时[D]=2[B]
查看答案和解析>>
科目:高中化学 来源: 题型:
已知在800 K时,反应:CO(g)+H2O(g)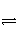
 H2(g)+CO2(g),若初始浓度c0(CO)=2 mol·L-1,c0(H2O)=3 mol·L-1,则反应达到平衡时,CO转化成CO2的转化率为60%,如果将H2O的初始浓度加大为6 mol·L-1,试求此时CO转化为CO2的转化率。
H2(g)+CO2(g),若初始浓度c0(CO)=2 mol·L-1,c0(H2O)=3 mol·L-1,则反应达到平衡时,CO转化成CO2的转化率为60%,如果将H2O的初始浓度加大为6 mol·L-1,试求此时CO转化为CO2的转化率。
查看答案和解析>>
科目:高中化学 来源: 题型:
可确认发生了化学平衡移动的是( )
A.化学反应速率发生了改变
B.有气态物质参加的可逆反应达到平衡后,改变了压强
C.由于某一条件的改变,使平衡混合物中各组分的浓度发生了不同程度的改变
D.可逆反应达到平衡后,使用催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
下图是温度和压强对X+Y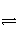
 2Z反应影响的示意图。图中横坐标表示温度,纵坐标表示平衡混合气体中Z的体积分数。下列叙述正确的是( )
2Z反应影响的示意图。图中横坐标表示温度,纵坐标表示平衡混合气体中Z的体积分数。下列叙述正确的是( )
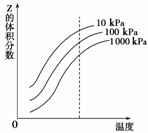
A.上述可逆反应的正反应为放热反应
B.X、Y、Z均为气态
C.X和Y中只有一种为气态,Z为气态
D.上述反应的逆反应的ΔH>0
查看答案和解析>>
科目:高中化学 来源: 题型:
有机合成中常用的钯/活性炭催化剂若长期使用,会被铁、有机化合物等杂质污染而失去活性,成为废催化剂。一种由废催化剂制取PdCl2的工艺流程如下:

(1)“焙烧1”通入空气的目的是使有机化合物、活性炭等可燃物通过燃烧而除掉,通入空气过多反而不利于实现目的,其原因是 。
(2)甲酸在反应中被氧化为二氧化碳,写出甲酸与PdO反应的化学方程式:___ 。
(3)加浓氨水时,钯转变为可溶性[Pd(NH3)4]2+,此时铁的存在形式是 (写化学式)。
(4)加入浓氨水的过程中,需要控制溶液的pH为8~9,实验室检测溶液pH的操作方法是:
。
(5)“焙烧2”的目的是: 。
(6)与焙烧2产生的气体组成元素相同的化合物是 ,该物质与空气形成一种环保型碱性燃料电池,其负极反应式为
(7) Pd中加入王水的反应可以表示为Pd+HCl+HNO3→A+B↑+H2O(未配平)。其中B为无色有毒气体,该气体在空气中不能稳定存在;A中含有三种元素,其中Pd元素的质量分数为42.4%,H元素的质量分数为0.8%。则A的化学式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com